1. 引言
锰是环境水质污染物的重要重金属监测指标之一,国家明文规定工厂排污口含锰及其化合物的最高排放质量浓度为2.0 mg/L [1] 。锰在水体中的价态易发生变化,其毒性随着价态的降低而增强。过量锰的摄入会引起动物和植物中毒,主要表现为对人和动物的神经系统产生毒害。目前重金属废水处理方法主要有:化学沉淀法、生物方法、活性炭吸附法、絮凝法、离子交换法、电解法等[2] 。其中最常用的锰污染治理主要采用化学方法[3] ,即在碱性条件下将溶解性的Mn2+氧化成不溶的MnO2,从而除掉废水中的锰。也有报道用活化沸石降低废水中的锰[4] 。前者易引起二次污染且成本较高,逐渐不被人们所采纳;后者没有深入研究吸附过程中各种因素的影响作用,且去除效果不明显。
腐植酸是一种广泛存在于土壤、湖泊、河流、海洋中的天然高分子化合物,是由相似族类的分子量大小不同、结构组成不一致的高分子羟基芳香羧酸类物质组成的复杂混合物,具有多种活性官能团,具有酸性、亲水性、界而活性、阳离子交换能力、络合作用及吸附分散能力[5] -[9] 。根据腐植酸的结构特点,可以采用不同的制备工艺,将腐植酸与各种单体共聚来制备腐植酸型树脂材料,充分发挥腐植酸独特的功效,扩大其应用领域。聚(N-异丙基丙烯酰胺) (PNIPAAm)属于智能高分子材料。由于其大分子侧链上同时具有强亲水性的酰胺基团(-CONH−)和疏水性的异丙基基团[-CH(CH3)2],具有特殊的吸附性能,在水溶液中呈现出温度敏感的特性[10] 。
本文采用反相悬浮聚合法,以腐植酸钠为主要原料,与N-异丙基丙烯酰胺、丙烯酸共聚合成一种具有较强吸附能力的新型腐植酸-N-异丙基丙烯酰胺交联树脂,通过对树脂在不同温度、不同pH下对Mn2+的吸附效果研究,探索该吸附剂应用于含微量锰废水处理的可行性。
2. 实验部分
2.1. 试剂与主要仪器
腐植酸钠(分析纯,天津市光复精细化工研究所);丙烯酸(分析纯,天津市光复精细化工研究所);N-异丙基丙烯酰胺(分析纯,阿拉丁试剂网);过硫酸钾(分析纯,天津市天大化学实验厂);环己烷(分析纯,天津市文达稀贵试剂化工厂);司盘-65(分析纯,上海试剂四厂);N,N’-亚甲基双丙烯酰胺(化学纯,天津市津科精细化工研究所);氢氧化钠(分析纯,天津市光复精细化工研究所);含Mn2+水溶液:MnCl24H2O(分析纯)溶于去离子水配成不同浓度。
超声清洗机(H66025T),无锡超声电子设备厂;增力电动搅拌器(JJ-2),江苏省金坛市荣华仪器制造有限公司;傅立叶红外光谱仪(AVATAR360),美国尼高力公司;台式干燥箱(202-00),北京中兴伟业有限公司;数显恒温震荡箱(SHA-BA),上海梅香仪器有限公司。
2.2. 腐植酸-N-异丙基丙烯酰胺交联树脂的制备
在装有回流冷凝装置和电动搅拌的三口瓶中,加入1.50 g Span-65和50 ml的环己烷,水浴加热至Span-65溶解作为油相。称取1.0080 g氢氧化钠固体放入50 ml烧杯,加入2.4 ml去离子水溶解,再加入3.40 ml丙烯酸(AA),混匀反应一定时间后按顺序加入0.40 g N-异丙基丙烯酰胺(NIPA),0.20 g过硫酸钾(KPS),0.30 gN,N’-亚甲基双丙烯酰胺(MBA),1.00 g腐植酸钠(HA-Na),混合至固体完全溶解作为水相。将水相慢慢加入到油相中通N2并搅拌30 min后,升温至70℃并保持恒温反应2 h,将产物滤出,用无水乙醇洗涤,干燥,得到直径为0.1~0.5 mm的粒状腐植酸交联树脂。
2.3. 树脂对Mn2+吸附性能测定
2.3.1. Mn2+标准曲线绘制
称取0.1801 g分析纯MnCl24H2O,置于容积为50 ml的烧杯中,用去离子水溶解后转移至容积为1000 mL的容量瓶中并定容至刻度,即得Mn2+浓度为50 mg/L的氯化锰溶液。分别吸取2.5 ml,2.2 ml,2.0 ml,1.8 ml,1.5 ml,1.0 ml,0.5 ml,0 ml于8个容积为50 ml的容量瓶中并用去离子水定容,即Mn2+浓度分别为2.5 mg/L,2.2 mg/L,2.0 mg/L,1.8 mg/L,1.5 mg/L,1.0 mg/L,0.5 mg/L,0 mg/L。按GB 11906-1989高碘酸钾分光光度法方法进行Mn2+吸光度的测定,以吸光度(A)为横坐标,浓度(C)为纵坐标绘制标准浓度曲线并得到标准曲线方程,见图1。
2.3.2. 溶液pH值对吸附性能影响实验
分别移取10 mg/L标准溶液50 ml于100 ml锥形瓶中,加入一定量腐植酸交联树脂,分别用0.2 mol/L的盐酸及氨水调节溶液pH,密封后将锥形瓶置于恒温水浴摇床中振荡,6 h后取出,静置30 min后过滤,按测定标准曲线的方法测定滤液Mn2+吸光度,由标准曲线方程计算吸附后滤液中Mn2+离子浓度Ct,计算树脂对Mn2+吸附量和吸附率。
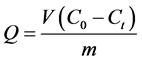 (1)
(1)
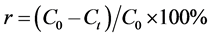 (2)
(2)
式中:
Q——树脂对Mn2+的吸附量,mg/g;
V——滤液体积,L;
C0——吸附前溶液中Mn2+浓度,mg/L;
Ct——吸附饱和后溶液中Mn2+浓度,mg/L;
m——树脂的加入量,g;
r——树脂对Mn2+的吸附率,%。
2.3.3. 吸附温度对吸附性能影响实验
分别移取配置好的Mn2+标准溶液50 ml于100 ml锥形瓶中,加入0.05 g腐植酸树脂,将输液瓶密封后置于恒温水浴摇床中,振荡方式为回旋式,振荡频率为60 r/min。改变水浴摇床的温度分别为15℃,30℃,32℃,35℃,40℃,45℃,50℃,恒温振荡6 h后将试样取出静置。静置30 min后过滤,用分光
H+与Mn2+发生吸附竞争,因H+半径远小于Mn2+的半径,H+的扩散速率比Mn2+大,树脂对H+吸附速率较大,故H+优先被吸附。H+被吸附到树脂颗粒表面后,中和了树脂颗粒表面的负电中心,降低了树脂对光度法分别测定滤液中Mn2+的吸光度,由标准曲线方程计算吸附后滤液中Mn2+离子浓度Ct,计算树脂对Mn2+吸附量和吸附率。
3. 结果与讨论
3.1. 树脂在不同温度下的吸附性能测定
图2为温度对树脂吸附水中Mn2+效应的影响曲线,Mn2+的初始浓度为50 mg/L,溶液pH值为6,树脂的质量浓度为1 g/L。由图可知,在15℃时树脂对Mn2+的吸附率已达98.4%,随着温度升高,吸附率逐渐增高,当温度高于30℃时,吸附率大于99.6%,其中当温度为32℃左右时吸附率达到最大,可达99.9%,继续升温吸附量逐渐变小,但降低幅度不大。这是由于腐植酸交联树脂上含有大量含有酚羟基、醇羟基、羧基、甲氧基、游离的醌基、半醌基等活性基团[11] ,且腐植酸具有疏松的“海绵状”结构与大的表面积和表面能,可与水中Mn2+发生离子交换、络合、鳌合反应及吸附作用[12] ,同时通过氢键与水结合具有较强的吸水功能,尤其聚N-异丙基丙烯酰胺(PNIPA)链段具有独特的吸水温度响应性[13] -[17] 。在32℃左右与水分子通过氢键作用能力最强,吸水能力最大,从而增大Mn2+在树脂中的溶解性,吸附Mn2+能力变强;当温度高于32℃,此时聚N-异丙基丙烯酰胺(PNIPA)链段因氢键的破坏使其与水之间的相互作用下降,但具有亲水性腐植酸链段的空间位阻较大,阻碍水的释放,所以温度升高树脂仍具有较高的吸附水和吸附Mn2+的能力。故与常规吸附性树脂比较,腐殖酸-N-异丙基丙烯酰胺交联树脂具有很宽的吸附温度范围。
3.2. 树脂在不同pH下的吸附性能测定
图3为树脂在不同pH值下对锰离子的吸附量的影响,Mn2+初始浓度为50 mg/L,树脂的质量浓度为1 g/L,吸附时间为6 h,温度30℃。由图可知,pH值在4~8范围内树脂对Mn2+吸附率在99.5%以上,平衡吸附量为1.2967 g/g,吸附效果良好,溶液pH值小于3时树脂对Mn2+的吸附率下降迅速。这是由于树脂中含有大量-COO-,-OH,-NH等基团对Mn2+产生表面吸附、离子交换、静电吸附及螯合等作用[18] ,而树脂表面H+的浓度决定了树脂螯合能力、离子交换能力的大小。当pH值较低时,溶液中存在的大量
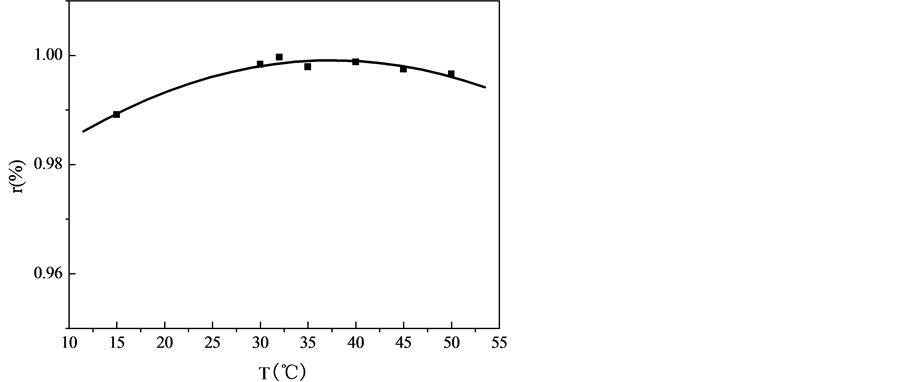
Figure 2. Effect of temperature adsorption quantity of Mn2+
图2. 温度对Mn2+吸附效果的影响
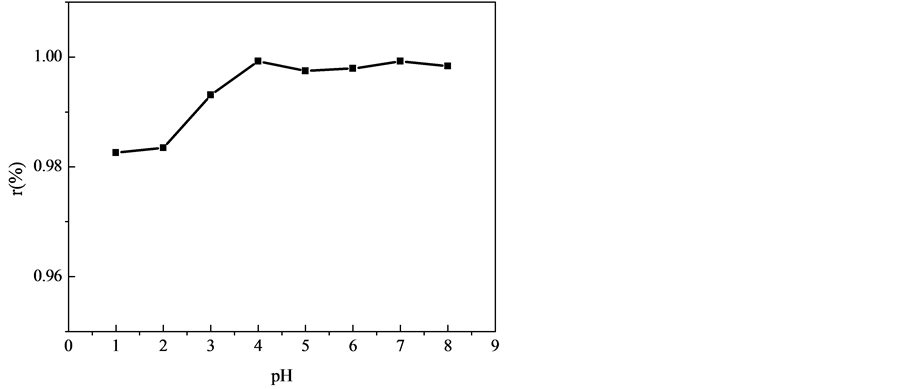
Figure 3. Effect of pH adsorption quantity of Mn2+
图3. pH对Mn2+吸附效果的影响
Mn2+的螯合亲和力,树脂对Mn2+的吸附量降低。随着pH值增高,溶液中H+数量减少,与Mn2+的吸附竞争减弱,树脂对Mn2+螯合吸附量增加。
4. 结语
1) 以腐植酸为原料,N-异丙基丙烯酰胺和丙烯酸为共聚单体,采用反相悬浮法制备的腐植酸-N-异丙基丙烯酰胺交联树脂对Mn2+有较强的吸附能力,其中聚N-异丙基丙烯酰胺(PNIPA)链段使树脂在高温和低温时都具有较好的吸附能力;
2) 用腐植酸树-N-异丙基丙烯酰胺交联脂吸附水中微量Mn2+时,最佳吸附温度为32℃,pH值为4~8,平衡吸附量为1.2967 g/g,Mn2+吸附率可达99.5%以上,在含微量锰废水处理中具有一定的应用价值。
基金项目
2011年河北省科技厅项目,编号11215122D。