1. 引言
随着人类生活水平逐步提高,生活节奏加快,癌症的发病率与日俱增。5-氟尿嘧啶(5-Fu)是一种广谱抗癌药物,因其治疗效果可靠而被广泛应用于临床,主要用于治疗消化道肿瘤,也常用于治疗肝癌、乳腺癌、卵巢癌、宫颈癌、膀胱癌等 [1] [2] 。但其毒性较大,代谢过程过快而使其应用受到了一定程度的限制。其对肿瘤细胞的选择性差,在杀伤癌细胞的同时,也对人体产生了严重的毒副作用。尤其在浓度较大的情况下,对正常细胞的毒副作用更加明显 [3] 。它在体内的半衰期短,仅为5~10分钟,临床上为了达到有效的体内血药浓度,往往采用大剂量、持续给药或反复多次给药等均增加了癌症病人的痛苦 [4] 。以新型高分子为载体的缓释给药系统能够实现减少给药次数,在病人体内持续释药,并降解为具有生物相容性的物质的目的。在增加患者顺应性,提高药物的治疗效果,减少用药的总剂量等方面成为一种潜在的解决途径 [5] [6] [7] [8] 。
壳聚糖(Cs)是天然多糖中唯一的碱性多糖,具有许多独特的物理化学特性和生物学功能。Cs及其分解产物无毒,具有良好的生物相容性和生物可降解性,可选择性地与肿瘤细胞聚集,抑制肿瘤细胞的生长,并可通过活化免疫系统,显示抗癌活性。Cs作为药物的包覆材料,在缓释给药系统中的应用己引起了人们浓厚的兴趣 [9] [10] [11] [12] [13] 。Ohya [11] 首次用水/油(W/O)型乳化剂,以戊二醛为交联剂,运用乳化交联法制备了氟尿嘧啶壳聚糖微球(平均粒径:0.8 ± 0.1 μm),该微球可被细胞表面特殊的受体识别,对SK-ep-1肝癌细胞有特殊亲和力和抗癌作用 [12] 。近年来,国内外以高分子材料为载体,以5-Fu为模型药物的微球制备虽然己有报道,但是所得的微球或者粒径普遍比较大,或者药物包封率和药物含量较低,无法兼顾 [3] [14] - [19] 。本文以壳聚糖作为包封材料,抗癌代表性药物5-Fu为模型药物,制备缓释给药5-氟尿嘧啶/壳聚糖载药微球(5-Fu/Cs微球),进行探讨性的研究,检测微球各项性能指标,包括微观形态、药物包封率、释放性能等,以观察该微球作为药物载体的可行性,为将来的临床应用提供实验依据。
2. 实验部分
2.1. 主要原料及试剂
5-氟尿嘧啶(5-Fu):天津金耀氨基酸有限公司;壳聚糖(Cs):分析纯,国药集团化学试剂上海有限公司;Span80、石蜡油:化学纯,广州市思伽化工有限公司;戊二醛(25%水溶液)、醋酸(36%)、氢氧化钠:分析纯,天津市精细化工研究所;无水乙醇、盐酸、磷酸氢二钠、磷酸二氢钠、氯化钠:分析纯,北京化学试剂公司;汽油、真空泵油(100#):中国石油天然气股份有限公司大连石化分工司。
2.2. 主要仪器
紫外可见分光光度仪:752N,上海瑞科有限公司;气浴恒温震荡器:SHZ-88A,江苏太仓实验设备厂;台式高速冷冻离心机:LGR10-4.2型,北京医用离心机厂;恒速数显电动搅拌器:DSX-90型,杭州仪表电机有限公司;红外光谱仪:V70型,德国Bruker公司;场发射扫描电子显微镜:S-4800型,日本日立公司。
2.3. 制备5-Fu-Cs微球
采用乳液-化学交联法,称取壳聚糖溶于0.2 mol/L的醋酸溶液,配成20 g/L的Cs溶液100 ml,按m(5-Fu):m(Cs)分别为1:1、1:3、1:5、1:6和1:7称取5-Fu加入到25 g上述Cs溶液中,搅拌溶解,慢慢加入到油相中,油相为200 ml含15 g/L司班-80和5 g/L硬脂酸镁的真空泵油与石蜡油混合物,V (真空泵油):V (石蜡油)为1:1,反应容器为三口圆底烧瓶。搅拌至乳液状反应0.5 h缓慢加入戊二醛溶液15 ml。升温至40℃反应2 h,用氢氧化钠溶液(25 wt%)调节pH = 7,再反应1 h后离心分离,产物先用汽油洗涤,然后用无水乙醇洗涤,在50℃条件下真空干燥得到粉末状产品。
2.4. 测试与表征
标准曲线的绘制:取125 mg 5-Fu分别用0.1 mol/L稀HCl溶液、pH = 7.4的缓冲溶液,及pH = 1.2的缓冲溶液,定容至50 ml (2.5 mg/mL),分别取稀释后的溶液2 ml、3 ml、4 ml、5 ml、6 ml再分别定容至50 ml,配制成0.1~0.3 mg/mL的标准溶液,在260 nm处用紫外-可见分光光度计测试吸光度,拟合曲线得标准曲线方程A1 = 1.104C1 − 0.004(R*R = 0.9999) K1 = 1.8,B1 = 0.0;A2 = 1.076C2 − 0.0084(R*R = 0.9998) K2 = 1.9,B2 = 0.0;A3 = 1.072C3 + 0.0076(R*R = 0.9997) K3 = 1.9,B3 = 0.0。
微球药物含量和包封率的测定:准确称取5-Fu/Cs微球20 mg加到锥形瓶中,用0.1 mol/L HCl溶液50 ml溶解24 h后过滤,滤液移至100 ml容量瓶中定容,测试其吸光度,根据工作曲线来求其浓度,按下列公式计算药物含量和包封率 [10] :
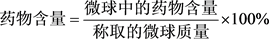

微球缓释性能分析:称取5-Fu/Cs微球50 mg放入透析袋中并封口,分别置于盛有pH = 1.2缓冲溶液和pH = 7.4缓冲溶液的250 ml磨口锥形瓶中,37℃条件下以100 r/min的速率恒温震荡,定时取5 ml释放介质测定其紫外吸光度,同时补充等量释放液,根据工作曲线计算其浓度,并绘制累计释药率-时间曲线。
红外光谱表征:采用溴化钾压片法,扫描范围500~4000 cm−1。
微观形态表征:样品喷金后在场发射扫描电子显微镜下观察并拍照。
3. 结果与讨论
3.1. 红外光谱分析
图1为原料(5-Fu)与产品(Cs微球和5-Fu-Cs微球)的红外光谱图。5-Fu谱图中1682.1 cm−1归属于5-Fu

Figure 1. IR spectra of raw material and product
图1. 原料及产品的红外光谱图
的特征吸收峰(C=O和C=C伸缩振动吸收峰),1488.2 cm−1归属于-CF=CH-中的C-H的面内弯曲振动吸收峰,1238.6 cm−1归属于C-N伸缩振动吸收峰,868.3 cm−1归属于-CF=CH-中的C-H的面外弯曲振动吸收峰,818.4 cm−1和775.6 cm−1归属于-CF=CH-中的C-H的面外变形振动吸收峰。Cs微球谱图中在1663.5 cm−1处出现Cs微球的特征吸收峰,归属于C=O的伸缩振动,1425.2 cm−1处是-CH2-的弯曲振动吸收峰,1084.3 cm−1和1062.7 cm−1归属于CS吡喃环中C-H的弯曲振动吸收峰。5-Fu/Cs微球谱图中在1278.2 cm−1处是5-Fu中的C-N伸缩振动红移吸收峰,900.1 cm−1处出现了5-Fu中的-CF=CH-中的C-H的面外弯曲振动红移吸收峰,吸收峰洪移表明Cs包裹5-Fu后,5-Fu分子之间的作用力被Cs削弱。818.4 cm−1和775.6 cm−1处归属于-CF=CH-中的C-H的面外变形振动吸收峰。在1663.5 cm−1处Cs的吸收峰消失,而在1641.3 cm−1处出现了特征吸收峰,1084.3 cm−1处吸收峰向低波数1062.7 cm−1漂移且变弱,而1030.0 cm−1的吸收峰大大减弱,这些情况说明5-Fu与Cs产生了较强的分子间相互作用力。
3.2. 微球微观形态分析
图2为5-Fu/Cs微球的SEM图。由图可见5-Fu/Cs微球的外观形态规整,无塌陷,为球形,且为单分散性,粒径均匀,微球彼此未发生黏连,粒径在400 nm左右。
3.3. 药物包封率
5-Fu/Cs微球的药物包封率与投料比之间的关系见表1,药物包封率在45.2%~87.6%。由于乳化阶段形成粒径小且分布均匀的微球,此时粒径与搅拌器转速有关,交联剂使微球固化,将模型药固定在壳聚糖骨架中。其次5-Fu在水中的溶解度比较大且呈弱酸性,该工艺与传统方法相比成球固化时间缩短,通过控制体系的PH值及投料比,使药物包封率提高。
3.4. 微球释药性分析
图3为5-Fu和5-Fu/Cs微球在pH = 1.2缓冲溶液中药物释放曲线,5-Fu在1.5 h基本上就释放完全了,而5-Fu/Cs微球在前3h内释放的快,当药物释放率达到50%左右释放逐渐减缓,40 h时释放率达到62%,未释放的还有38%左右,这说明5-Fu/Cs微球的控释性能很好。由于醛氨缩合反应形成键桥使微球固化,将药固定在壳聚糖骨架中,从而达到缓释效果。

Table 1. The relationship between embedding rate of chitosan microspheres and raw material rate
表1. 微球药物包封率与投料比关系

Figure 2. SEM image of 5-Fu/Cs microspheres
图2. 5-Fu/Cs微球的SEM图
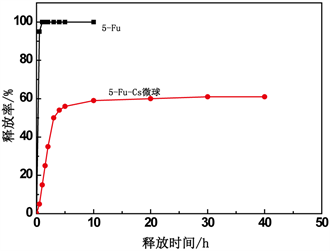
Figure 3. Drug-releasing curves of sample in solution (pH = 1.2)
图3. 在pH = 1.2缓冲溶液中的释放曲线
3.5. 投料质量比对释药性的影响
图4为5-Fu/Cs微球在pH = 1.2缓冲溶液中的释放曲线,m(5-Fu):m(Cs)为1:5的微球在5 h释药已达56%而m(5-Fu):m(Cs)为1:3的微球释药到65%,这是因为CS较多形成的囊壁较厚,所以随着m(5-Fu):mCs)比的减小,微球的缓释效果增强。
3.6. 溶液pH值对微球释药性的影响
图5中在初期(前2 h)微球的释药性基本不受溶液pH值的影响;但2 h后,在pH = 7.4条件下微球的释药速度要比pH = 1.2条件下快,尤其是20 h之后更加明显。两种不同pH值条件下前5 h释药速度快,10 h后趋于平缓,24 h后载药微球在pH = 1.2缓冲溶液中释放率为57%,在pH = 7.4缓冲溶液中释放71%,可见微球的体外释药性与溶液pH值有关,酸性条件下缓释效果更好。
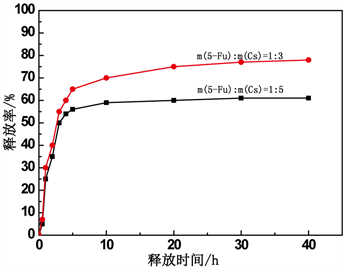
Figure 4. Drug-releasing curves of 5-Fu/Cs microspheres in solution (pH = 1.2)
图4. 5-Fu/Cs微球在pH = 1.2缓冲溶液中的释放曲线

Figure 5. Drug-releasing curves of 5-Fu/Cs microspheres in different solution
图5. 5-Fu/Cs微球在不同pH值缓冲溶液中的释放曲线
4. 结论
以壳聚糖为药物载体,戊二醛为交联剂,真空泵油和石蜡油为混合油相,司班-80和硬脂酸镁为复合乳化剂是一种行之有效的制备5-氟尿嘧啶/壳聚糖载药微球的方法。所得5-Fu/Cs微球的外观形态规整,无塌陷,且为单分散性,粒径均匀,微球彼此未发生黏连。粒径约400 nm,药物包封率在45.2%~87.6%。体外释药性分析表明5-Fu/Cs微球具有良好的缓释性能,随着m(5-Fu):m(Cs)比值的减小,微球的缓释效果增强,酸性环境下缓释效果更好,优越于碱性环境。
基金项目
嘉兴学院SRT资助项目(SRT2016C148),嘉兴学院实验室开放基金(201601),浙江省“十二五”省级实验教学示范中心重点建设项目。