1. 引言
化香树果序为胡桃科植物化香树(Platycarya strobilacea Sieb. et Zucc.)的果序,化香树在我国西北、华东、华中、华南等地均有广阔分布。化香树在我国已有应用,根皮、树皮、叶、果实可以用作生产栲胶,树皮纤维能代替麻;叶可做农药,也可供药用,能顺气,祛风,化痰,止痛,燥湿,杀虫 [1] 。有关文献报道,利用溶剂对化香树果序进行提取,发现化香果序中含有丰富的生物活性物质,例如植物多酚、鞣花酸、黄酮等 [2] [3] 。已有研究表明多酚类化合物具有抑菌、抗病毒、抗肿瘤等生物活性作用,对细菌、真菌、酵母菌等常见的致病菌、病毒有很强的抑制作用 [4] [5] [6] 。作者针对化香果有效成分利用开展研究工作 [7] [8] ,进一步开展化香果多酚物质的提取纯化工艺和多酚抗氧化性能研究,对更好的利用化香果序资源,具有重要的指导意义。大孔吸附树脂具有稳定性高、吸附选择性强、吸附量大、吸附效果明显、解吸条件温和、使用周期长等优点,近年来被广泛用于功能性成分的分离与富集 [9] [10] 。本实验对化香果多酚纯化工艺和抗氧化性能进行研究,以期为化香果多酚类物质的工业化生产和应用提供方法及理论依据。
2. 材料与方法
2.1. 材料与设备
2.1.1. 材料与试剂
化香果提取物,中国林科院林产化学工业研究所单宁实验室制备;没食子酸标准品、福林-酚试剂、DPPH∙试剂、XAD-7型大孔树脂,Sigma公司;生育酚,东京化成工业株式会社;D101、AB-8、NKA-9、ADS-5型大孔树脂,天津和成树脂有限公司;三吡啶三吖嗪(TPTZ),阿拉丁试剂有限公司;2,6-二叔丁基-4-甲基苯酚(BHT)、抗坏血酸、无水碳酸钠、无水乙醇、甲醇、盐酸、氢氧化钠、醋酸钠、三氯化铁、硫酸亚铁,均为国产分析纯。
2.1.2. 仪器与设备
Agilent Cary 8454紫外分光光度计,美国安捷伦公司;PE-20pH计,瑞士梅特勒-托利多公司;BE204E分析天平,梅特勒-托利多公司;SHA-CA水浴恒温振荡器,金坛荣华制造有限公司;层析柱(Ø1.8 cm × 30 cm);SHZ-D (III)循环水式真空泵,巩义裕华。
2.2. 实验方法
2.2.1. 多酚含量测定
采用福林-酚法测定化香果提取物中的多酚含量 [11] [12] 。吸取0.2 mL待测样品溶液于10 mL棕色容量瓶内,依次加入0.5 mL 50%福林-酚、1.5 mL 20%碳酸钠溶液,用一级水定容,避光反应2 h后于760 nm波长下测定吸光度。
2.2.2. 标准曲线绘制
以没食子酸作为标准品,配置不同质量浓度的溶液,按2.2.1节方法测定。以吸光度(y)为纵坐标,没食子酸质量浓度(x)为横坐标绘制标准曲线。得线性回归方程:y = 2.1934x + 0.0244 (R2 = 0.9979)。
2.2.3. 多酚纯度测定
将化香果粗提物和纯化后多酚冻干粉配置成测定液,按照2.2.1节测定溶液的多酚浓度,按公式(1)计算多酚纯度 [13] 。
(1)
式中:C—待测样品溶液的多酚浓度,mg/mL;V—待测溶液体积,mL;m—称取化香果提取物样品的质量,mg。
2.2.4. 大孔树脂预处理
将大孔树脂进行活化,浸泡在无水乙醇中搅拌除去气泡,静置24 h,使用一级水洗至树脂无乙醇味。用5% NaOH溶液浸泡树脂4 h,用一级水洗至中性,再用5% HCl溶液浸泡4 h,后用一级水洗至中性,吸干水分备用 [14] 。
2.2.5. 大孔树脂的筛选
准确称取预处理好的5种大孔树脂AB-8、D101、NKA-9、ADS-5、XAD-7各5.0 g,分别放入锥形瓶中,加入50 mL一定质量浓度的化香果提取物样品溶液,于振荡器中吸附,温度25℃,转速120 r/min。24 h后过滤,吸取上部清液测定其中多酚含量。用一级水清洗吸附饱和后的树脂,加入50 mL乙醇溶液,放入振荡器中解吸,转速120 r/min。24 h后过滤吸取上部清液测定多酚含量。分别按公式(2)、(3)、(4)计算吸附量、吸附率及解吸率 [15] 。
(2)
(3)
式中:C0、C1—吸附前、吸附后试液中的多酚浓度,mg/mL;V—供试液体积,L;M—湿树脂重,g。
(4)
式中:C—洗脱液中的多酚浓度,mg/mL;V1—供试液体积,L;Q—吸附量,mg/g;M1—湿树脂重,g。
2.2.6. 静态吸附-解吸动力学曲线
准确称取预处理好的D101大孔树脂5.0 g,放入锥形瓶中,加入50 mL化香果提取物样品溶液,于振荡器中吸附,温度25℃,转速120 r/min,每隔1 h吸取1.0 mL上部清液测定其中多酚含量,绘制静态吸附动力学曲线。24 h后用一级水清洗已充分吸附多酚的D101大孔树脂,洗至无样品溶液残留,吸干水分后称取5.0 g放入锥形瓶中,加入75%乙醇溶液50 mL,于振荡器中静态解吸12 h,每隔1 h吸取1.0 mL上部清液测定其中多酚含量,并绘制静态解吸动力学曲线。
2.2.7. 静态吸附-解吸实验
取预处理好的D101大孔树脂5.0 g分别放入100 mL锥形瓶中,分别配制质量浓度为0.1、0.2、0.4、0.8、1.6、3.2、6.4 mg/mL的化香果提取物溶液,各加入50 mL至锥形瓶中,于振荡器中吸附,温度25℃,转速120 r/min。吸附完全后取上清液测定多酚含量,并计算多酚吸附量。配置一定浓度的化香果提取物溶液,将pH值分别调至2、3、4、5、6、7、8,在放好树脂的锥形瓶中各加入50 mL不同pH的化香果提取物溶液,于振荡器中吸附,吸附完全后取上清液测定多酚含量,将充分吸附化香果多酚的D101大孔树脂用一级水清洗,吸干水分,分别称取5.0 g于锥形瓶中,考察40%、50%、60%、70%、80%、90%体积分数的乙醇溶液对静态解吸效果的影响。加入不同体积分数的乙醇溶液50 mL,于振荡器中静态解吸完全后,取上清液测定其多酚质量浓度,并计算多酚解吸率。
2.2.8. 大孔树脂吸附的动态吸附与解吸实验
取预处理好的D101型大孔树脂装入Ø1.8 cm × 30 cm玻璃层析柱中。用一级水平衡后,控制样品液分别以不同流速(1、2、3、4 mL/min)上样并收集流出液,每10 mL为一管,检测并计算收集液的多酚浓度,绘制动态吸附曲线。
将已吸附饱和的树脂进行动态解吸实验,用一级水洗至无样品液残留,用70%乙醇以一定的洗脱流速(1、2、3、4 mL/min)进行洗脱,收集洗脱液,计算洗脱液的多酚浓度,绘制动态解吸曲线。
2.2.9. 抗氧化能力测定
1) 清除DPPH∙自由基能力测定
参考文献 [16] 的方法配置质量分数为0.004%的DPPH∙甲醇溶液,避光保存。将待测样品和对照品分别配置成一定浓度的溶液。精确吸取0.1 mL待测溶液样品溶液和3 mL DPPH∙甲醇溶液于10 mL试管中,摇匀后室温放置30 min,以各自溶剂为对照,测定其在517 nm处的吸光度值As。设3个重复。同时测3 mL DPPH∙甲醇溶液与0.1 mL各自试样溶剂混合后的吸光度值A0。样品对DPPH∙的清除能力用抑制率K来表示。K按照公式(5)计算,通过K计算各个样品对DPPH∙的半抑制浓度IC50。
(5)
2) 总抗氧化能力测定(FRAP法)
参考文献 [17] 的方法,将待测样品和对照品分别配置成0.1 mg/mL的溶液。配置10.0 mmol/L TPTZ溶液,0.30 mol/L醋酸钠缓冲液,20.0 mmol/L FeCl3溶液,TPTZ工作液由TPTZ溶液FeCl3溶液,醋酸钠缓冲液组成(1:1:10)。精确吸取待测溶液各0.1 mL,分别加入预热至37℃的1.8 mL TPTZ工作液充分混匀,用一级水补足至5.0 mL,37℃反应20 min;593 nm测定吸光度值。设3个重复。以0.1~1.50 mmol/L的 FeSO4标准溶液做标准曲线,以吸光度(y)为纵坐标,物质的量浓度(x)为横坐标,绘制标准曲线。样品抗氧化活性以达到同样吸光度所需的FeSO4的数值表示。
3. 结果与分析
3.1. 大孔树脂的筛选
由表1可以看出,XAD-7大孔树脂对于化香果多酚的吸附能力最强,D101树脂次之,AB-8和NKA-9大孔树脂的吸附率较低。D101、AB-8、NKA-9大孔树脂的解吸性能较强。综合考虑实际应用的效果和成本,选择D101大孔树脂作为化香果多酚的纯化材料。
3.2. D101大孔树脂的静态吸附-解吸动力学曲线
图1是D101树脂的静态吸附-解吸曲线,由吸附量曲线可知,D101大孔树脂在 2 h达到饱和,之后随着时间的延长,吸附量基本没有增加,所以吸附时间选为2 h。通过解吸曲线可以看出,当处在1 h时树脂解吸量已达到较大,之后解吸量反而有所下降。选择解吸时间1 h。
3.3. D101大孔树脂的静态吸附-解吸实验
3.3.1. 化香果多酚上样质量浓度对吸附效果的影响
由图2可知,多酚浓度较低时随着浓度提高,多酚吸附量迅速增加。当样品液质量浓度为3.2 mg/mL,吸附量达到最大6.67 mg/g。之后随着浓度增大吸附量开始下降。这可能是因为溶液中与多酚竞争吸附的杂质含量随着样品液浓度增高而增高,杂质与多酚对树脂的吸附形成竞争对多酚的吸附量趋于饱和甚至下降[18]。如果样品液质量浓度过低,会造成多酚含量降低,导致吸附动力变小,吸附量降低。因此,样品液质量浓度选为3.2 mg/mL。

Figure 1. Static adsorption-desorption curve of polyphenols
图1. 静态吸附-解吸动力学曲线

Table 1. The static adsortion and desorption analysis of 5 macroporous resins
表1. 5 种大孔树脂静态吸附及解吸性能结果

Figure 2. Influence of sample concentration on adsorption quantity
图2. 样品液质量浓度对吸附量的影响
3.3.2. 样品液pH值对吸附效果的影响
如图3所示,在pH值小于4时,化香果多酚的吸附量与样液pH值呈正相关;这是由于化香果多酚在酸性条件下能够保持容易被吸附的状态此状态,有利于吸附,在pH值为4时吸附量达到最大值3.58 mg/g。样品液pH值大于4时,多酚吸附量开始降低。所以选择pH4作为配置样品液的较佳pH。
3.3.3. 洗脱液体积分数对树脂解吸的影响
如图4所示,随着乙醇体积分数的增大,解吸量也随之提高,当乙醇体积分数达到70%时,解吸量最高达到3.98 mg/g。之后再进一步增加乙醇浓度解析量增加逐渐平缓。由于洗脱液极性变大,含水量变少,多酚不能充分的溶解,解吸量呈下降趋势。考虑到实际应用成本选择70%乙醇作为洗脱剂。
3.4. D101大孔树脂动态吸附-解吸条件优化
3.4.1. 上样流速对树脂吸附效果的影响
将已活化的大孔树脂装入玻璃层析柱,控制化香果多酚样品液分别以1、2、3、4 mL/min的流速上样,收集流出液,测定每收集管中化香果多酚质量浓度,绘制动态吸附曲线。
上样流速主要影响化香果多酚向树脂的扩散效果,为使扩散进行的更加有效,化香果多酚和大孔树脂必须要充分接触。如果流速过快,多酚还没有被吸附就被冲洗下来,部分酚类物质流出柱子,从而导致吸附量低;如果流速过慢,虽然有利于树脂对酚类物质的吸附,但却会降低生产效率 [19] 。由图5可知,在1 mL/min和2 mL/min 2种上样流速下树脂吸附量较优。考虑实际生产效率问题,试验选用2 mL/min为较佳的上样流速。
3.4.2. 洗脱流速对大孔树脂动态解吸效果的影响
将吸附饱和的树脂,用体积分数70%乙醇溶液进行洗脱,控制洗脱流速分别为1、2、3、4 mL/min,收集洗脱液,测定每收集管中化香果多酚质量浓度,绘制动态洗脱曲线。
洗脱流速对解吸效果有一定影响。理论上洗脱流速要求慢,但如果流速过慢,解吸时间会变长,而且洗脱时多酚会被重新吸附,降低解吸量;如果流速过快,洗脱剂不能和的树脂充分接触而快速流出,使得解吸量降低 [20] 。由图6可知,随着洗脱流速的加快,解吸量不断降低,当洗脱流速在2 mL/min 时解吸效果较好,故采用此流速为洗脱流速。
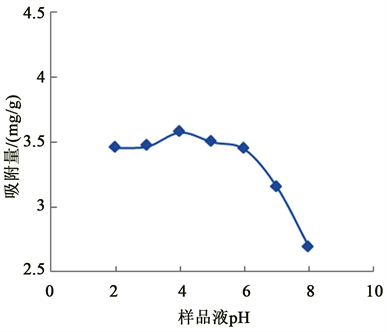
Figure 3. Influence of pH value of sample solution on adsorption quantity
图3. 样品液pH对吸附量的影响
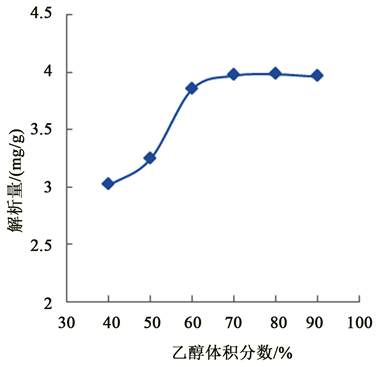
Figure 4. Influence of ethanol concentration on desorption
图4. 乙醇体积分数对解吸量的影响

Figure 5. Influence of sample loading flow rate on adsorption effect
图5. 上样流速对树脂吸附效果的影响
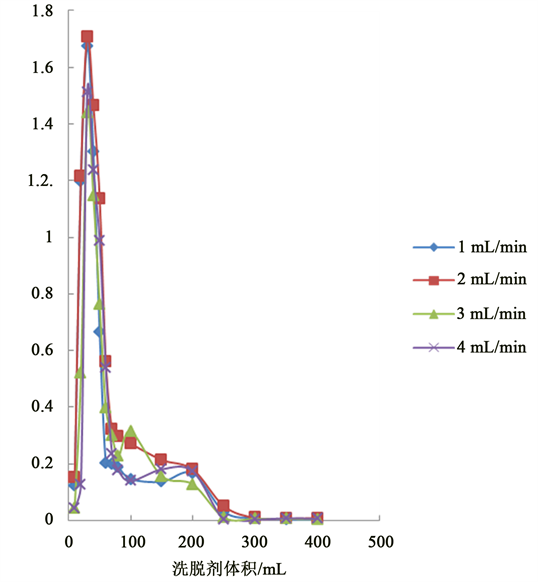
Figure 6. Influence of eluting rate on desorption effect
图6. 洗脱流速对解吸效果的影响
3.5. 化香果多酚纯度的测定结果
以化香果粗提物为原料,使用D101大孔树脂纯化化香果多酚,按照条件:样品液质量浓度3.2 mg/mL、样品液pH 4、上样流速2 mL/min、吸附时间2 h、洗脱剂乙醇体积分数70%、洗脱流速2 mL/min、解吸时间1 h,进行纯化。洗脱液蒸去乙醇,浓缩、冷冻干燥得纯化产物。
分别测定化香果粗提物和树脂纯化后的多酚的纯度。结果表明,经过D101大孔树脂纯化后,化香果提取物中多酚纯度由67.35%提高至87.39%,表明D101大孔树脂吸附纯化化香果多酚效果显著。
3.6. 抗氧化能力测定结果
3.6.1. 清除DPPH∙能力的测定
由表2可见,在相同试验条件下,化香果粗提物和化香果提取物纯化产物对DPPH∙的半抑制浓度IC50分别为104.87 ug/mL,88.86 ug/mL,对比其他三种抗氧化剂,化香果提取物纯化产物的抗氧化能力最强,化香果粗提物的抗氧化能力强于生育酚和BHT。五种实验样品对DPPH∙自由基的抑制能力强弱为:化香果提取物纯化产物 > 抗坏血酸 > 化香果粗提物 > 生育酚 > BHT。纯化后的化香果多酚的清除自由基能力得到进一步增强。
3.6.2. 总抗氧化能力测定
以对照品配制标准溶液得到的回归方程为:y = 0.6284x + 0.0202 (R2 = 0.9967),其中x为FeSO4浓度(mmol/L),y为吸光度值。根据标准曲线计算各样品的FRAP值,如表3所示。
由表3可知,在相同试验条件下,化香果粗提物和纯化产物都具有一定的抗氧化活性,纯化后的化香果提取物抗氧化能力得到增强。化香果纯化产物的抗氧化能力强于生育酚,抗坏血酸和BHT。五种

Table 2. IC50 of scavenging capacities for DPPH∙
表2. 清除DPPH∙能力的IC50测定结果

Table 3. Results of the antioxidant activity by FRAP assay
表3. 总抗氧化能力的测定结果
实验样品总抗氧化能力强弱与清除DPPH自由基能力一致为:化香果提取物纯化产物 > 抗坏血酸 > 化香果粗提物 > 生育酚 > BHT。
4. 结论
本研究通过对比AB-8、D101、XAD-7、ADS-5、NKA-9大孔树脂对化香果多酚提取物吸附-解吸的效果发现,对于化香果多酚物质,D101大孔树脂能够较好地进行纯化,其较佳吸附-解吸工艺条件为:样品液质量浓度3.2 mg/mL、样品液pH 4、上样流速2 mL/min、吸附时间2 h;乙醇体积分数70%、洗脱流速2 mL/min、解吸时间1 h。纯化后化香果多酚纯度由67.35%提高至87.39%。通过体外抗氧化能力的测定,化香果粗提物和化香果提取物纯化产物都具有较强的抗氧化活性。化香果提取物和化香果提取物纯化产物对DPPH·的IC50分别为104.87 ug/mL,88.86 ug/mL,总抗氧化能力(FRAP)值分别为1.268 mmol/L,1.496 mmol/L,表明经过D101大孔树脂吸附纯化以后的化香果多酚的抗氧化能力得到进一步增强。与所选参照物相比抗氧化能力强弱为:化香果提取物纯化产物 > 抗坏血酸 > 化香果粗提物 > 生育酚 > BHT,化香果提取物经过纯化以后表现出较强的抗氧化能力,可以更好的作为抗氧化剂应用。
基金项目
江苏省林业三新工程项目(LYSX[2016]56),国家重点研发计划(2016YFD0600806),中国林科院林产化学工业研究所研究团队建设创新工程项目(LHSXKQ4)资助。
NOTES
*通讯作者。