1. 引言
苜蓿是草食动物的优质饲草,被誉为“牧草之王”。近年来,全球转基因苜蓿种植面积呈逐年上升的趋势(ISAAA, 2020),2019年达到1.30 × 106 hm2,主要种植国为美国,产量居全球首位 [1]。我国进口的苜蓿草主要来自于美国和西班牙,这两个国家已经分别于2004年和2005年批准了转基因苜蓿的种植。
抗草甘膦转基因苜蓿品系J163(商品名 Roundup Ready Alfalfa Events J163)是由美国孟山都公司研制开发的一种转基因苜蓿草品系,具有抗倒伏和控制杂草的特点 [2],在美国、加拿大、墨西哥、日本、菲律宾、澳大利亚等9个国家获得授权(ISAAA, 2021) [3],目前我国尚未批准其进口,但天津、北京口岸多次从美国进口申报为非转基因的苜蓿草及种子中检出J163品系,因此加强对进口苜蓿的转基因筛查力度势在必行。《农业部2122号公告-6-2014转基因植物及其产品成分检测耐除草剂苜蓿J163及其衍生品种定性PCR方法》 [4] 规定了J163品系的普通PCR检测方法,但目前缺乏与该标准配套的标准样品,严重影响了这些方法的标准化应用,给转基因苜蓿品系J163的检测工作带来诸多不便。因此,研制转基因苜蓿品系J163基体定性标准样品,有助于提高转基因苜蓿品系J163检测的科学性和一致性,推广转基因生物标准样品在我国转基因产品检测中的应用,为获得准确、可靠、具有可比性的检测结果提供保障。
2. 材料与方法
2.1. 材料
2.1.1. 试验材料
以本实验室保存的转基因苜蓿J163种子作为研制J163品系标准样品的候选物。
2.1.2. 试剂材料
中国检疫科学研究院植物检验与检疫研究所种子样品直接扩增试剂盒、天根新型植物基因组DNA提取试剂盒、天根PCR MIX、DNA Maker DL2000、ABI TaqMan Universal PCR Master Mix,引物和探针由上海Sangon公司合成,稀释为终浓度为10 µmol/L的工作浓度使用。
2.2. 制备方法
2.2.1. 候选物鉴定
提取本实验室保存的转基因苜蓿J163种子的基因组总DNA,按照《农业部2122号公告-6-2014转基因植物及其产品成分检测耐除草剂苜蓿J163及其衍生品种定性PCR方法》中规定的检测方法进行鉴定。
为确定该候选物中不含有其它已知的转基因成分,本研究依据检验检疫行业标准SN/T 1204-2016《植物及其加工产品中转基因成分实时荧光PCR定性检验方法》 [5] 中规定的实时荧光PCR方法对苜蓿种子进行检测。选择pCaMV 35S、pFMV35S、CTP2-CP4-EPSPS、tNOS、tE9、NPTII等常用的筛选元件对待测材料进行实时荧光PCR筛选。
2.2.2. 标准样品制备
转基因苜蓿J163种子装于透气种子袋中,放置于真空冷冻干燥仪中,干燥24 h。干燥后的转基因苜蓿J163种子装于研磨罐中,液氮预冷,利用冷冻研磨仪进行研磨,研磨程序为30 frequcy/s,运行1分钟,停止2 min,5个循环。研磨后迅速转移至冷冻干燥仪中干燥24 h。使用180目标准筛进行分筛。
2.2.3. 最小取样量的确定
分别称取20 mg、50 mg、100 mg标准样品粉末,提取基因组总DNA,并将总DNA稀释10倍,以提取好的总DNA及稀释10倍的总DNA为模板按照2.2.1规定的普通PCR方法进行扩增。
2.2.4. 均匀性检验
按照GB/T 15000.3-2008《标准样品工作导则(3) 标准样品定值的一般原则和统计方法》 [6] 的规定,进行取样和均匀性检验。本试验从4℃保存制备好的样品中,随机抽取10个样品,采用1.2.1规定的PCR方法对上述样品进行检测,以此验证样品的均匀性。
2.2.5. 稳定性检验
1) 长期贮存稳定性
将制备好的样品置于−20℃、4℃,按先密后疏的原则在不同时间(0天、1个月、3个月、6个月、12个月、18个月、24个月)抽取样品,每次随机抽取3管样品,提取样品总DNA,采用1.2.1规定的普通PCR方法进行检测,每管检测2次,监测样品在储存温度下随时间的变化情况。
2) 短期运输稳定性
考虑到样品的寄送温度和时间,分别将样品置于37℃、室温(20℃~25℃)、4℃和−20℃,分别放置0周、2周、4周、8周,从制备好的样品中,每次随机抽取3管样品,提取样品总DNA,采用2.2.1中规定的普通PCR方法进行检测,每管检测2次,监测样品在储存温度下随时间的变化情况。
2.2.6. 协作定值
本标准样品的定值采用2.2.1中规定的普通PCR方法,与多个实验室合作定值的方式进行。测量时,要求操作者独立地进行操作,并尽可能使用不同的实验仪器。选取8家具有该标准样品定值检测必备条件,且有一定技术权威性的实验室进行合作定值。
3. 结果
3.1. 候选物的鉴定
鉴定结果表明,苜蓿内标准基因ACC的PCR扩增得到154 bp大小的条带,与预期片段大小一致,说明待测材料为苜蓿材料,且提取的DNA质量良好,适合于进行PCR检测分析。J163品系特异性PCR扩增得到241 bp大小的条带,与预期片段大小一致,说明待测材料的基因组中存在J163品系特异性片段,为转基因J163品系苜蓿材料。见图1、图2。

Figure 1. PCR electropherogram of ACC gene. M: DL2000 Marker; 2-21 Alfalfa samples 1-10, with two replicates for each sample; NC: Negative control; PC: Positive control; B: Blank control
图1. ACC基因PCR电泳图。M:DL2000分子量标记;2-21泳道为随机抽取的样品1-10,每个样品两个重复;NC:阴性对照;PC:阳性对照;B:空白对照

Figure 2. PCR electropherogram of J163 event specific gene. M: DL2000 Marker; 2-21 Alfalfa samples 1-10, with two replicates for each sample; NC: Negative control; PC: Positive control; B: Blank control
图2. J163品系特异性基因PCR电泳图。M:DL2000分子量标记;2-21泳道为随机抽取的样品1-10,每个样品两个重复;NC:阴性对照;PC:阳性对照;B:空白对照
将J163品系特异性PCR扩增的产物测序,与抗除草剂苜蓿J163转化体特异性序列进行比对。测序结果见图3,经与《农业部2122号公告-6-2014转基因植物及其产品成分检测耐除草剂苜蓿J163及其衍生品种定性PCR方法》中给出的J163转化体特异性序列比对,扩增片段与抗除草剂苜蓿J163转化体特异性序列的同源性达100%。
依据检验检疫行业标准SN/T 1204-2016《植物及其加工产品中转基因成分实时荧光PCR定性检验方法》中规定的实时荧光PCR方法对苜蓿种子进行检测。实验结果显示pFMV35S、CTP2-CP4-EPSPS、tE9基因均有明显的扩增曲线,pCaMV 35S、tNOS、NPTII基因均无明显扩增曲线,进一步证实该材料为转基因苜蓿J163品系,但不含有其它已知的转基因成分。
3.2. 最小取样量
以20 mg、50 mg、100 mg样品粉末为起始取样量提取的总DNA均能够扩增出241 bp大小的条带,与J163品系特异性片段大小一致,稀释10倍后的总DNA模板也可以清晰扩增出预期大小的条带,见图3。因此确定本研究标准样品最小取样量为20 mg。
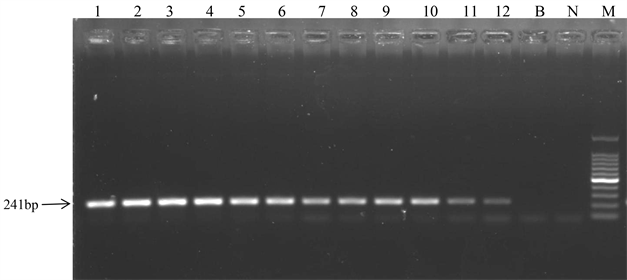
Figure 3. PCR electropherogram of different sampling quantity of samples. 1, 2: 20 mg sample; 3, 4: 50 mg sample; 5, 6: 100 mg sample; 7, 8: 20 mg sample diluted 10 times; 9, 10: 50 mg sample diluted 10 times; 11, 12: 100 mg sample diluted 10 times; M: 100 bp Marker; B: Blank control; NC: Negative control
图3. 不同样品取样量的PCR扩增图。1、2为20 mg样品;3、4为50 mg样品;5、6为100 mg样品;7、8为20 mg样品稀释10倍;9、10为50 mg样品稀释10倍;11、12为100 mg样品稀释10倍;M:100 bp ladder;B:空白对照;N:阴性对照
3.3. 均匀性检验
样品均匀性检测结果见图4,随机抽取的10个样品,每个样品设置2个重复进行J163品系特异性PCR扩增,电泳检测扩增结果。所有样品 J163品系特异性序列均得到扩增,且PCR扩增片段大小与预期片段大小一致,扩增得到241 bp大小的条带且条带亮度相似,表明样品均匀性良好,满足标准样品对均匀性的要求。
3.4. 稳定性检验
3.4.1. 短期运输稳定性
样品短期运输稳定性检测结果见表1,结果表明标准样品在37℃、室温、4℃和−20℃储存8周后,PCR检测仍为转基因苜蓿J163品系阳性,说明冻干粉标准样品在−20℃~37℃的条件下运输均是稳定的。
3.4.2. 长期贮存稳定性
长期保存稳定性检验结果见表2,结果表明,制备好的标准样品在−20℃、4℃储存24个月,PCR检测仍为转基因苜蓿J163品系阳性,说明冻干粉标准样品可于−20℃、4℃稳定储存24个月。
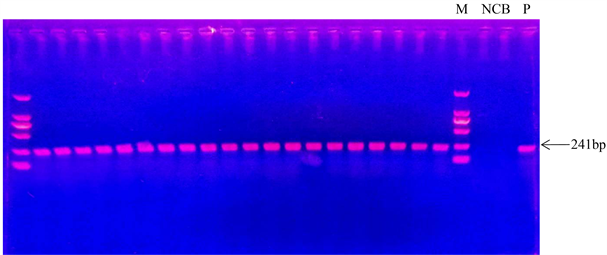
Figure 4. PCR electropherogram of uniformity test. M: DL2000 Marker; 2-21 Alfalfa samples 1-10, with two replicates for each sample; NC: Negative control; PC: Positive control; B: Blank control
图4. 均匀性检测PCR电泳图。M:DL2000分子量标记;2-21泳道为随机抽取的1-10号样品,每个样品两个重复;NC:阴性对照;PC:阳性对照;B:空白对照

Table 1. Results of short-term stability test for GM alfalfa J163
表1. 转基因苜蓿J163品系短期稳定性结果

Table 2. Results of long-term stability test for GM alfalfa J163
表2. 转基因苜蓿J163品系长期稳定性结果
3.5. 协作定值
制备的标准样品经8家权威实验室进行协同定值验证,转基因苜蓿J163品系均为阳性,与研制单位的检测结果相一致,表明该标准样品可用于转基因苜蓿J163品系检测技术的质量控制、检测试剂的验证和评价,实验室能力验证活动。
4. 结果及讨论
转基因生物标准物质是具有一种或多种足够均匀和很好确定的特性值(转基因成分或含量),在转基因产品检测中用以校准测量装置、评价测量方法或给材料赋值的一种材料或物质 [7],是转基因检测工作的基本前提,也是转基因检测工作的核心所在。
转基因基体标准样品是由原始的植物材料(种子、叶片等)制成,是发展最早且应用最广泛的一类标准样品,因其特性与实际检测中的未知样品的特性相近,具有更高的可靠性和准确性 [8]。在转基因检测中,既可以用于基于蛋白质的检测方法,也可以用于基于核酸的检测方法,具有更广的用途。在基体标准样品的制备过程中,植物种子因其具有稳定性好且便于存储的优点,是使用最广泛的候选物。本研究即采用转基因J163品系的苜蓿种子作为候选物,制备了转基因苜蓿J163品系的基体标准样品,并联合8家实验室对标准样品进行了协作定值。结果表明,制备的标准样品均匀性和稳定性均符合国家标准样品的技术要求,并获得了国家标准样品证书,填补了国内转基因苜蓿基体标准样品制备的空白,为推广转基因生物标准样品在转基因产品检测中的应用奠定基础。
基金项目
原质检总局科技计划项目(2017IK142)。
NOTES
*第一作者。
#通讯作者。