1. 引言
对水生生态系统而言,磷酸盐(Pi)含量是一个重要的生态健康指标,在生物系统中发挥着至关重要的作用。然而,工业、农业和生活废水中的磷酸盐过量排放到水生生态系统中,会引起水体富营养化,减少水体中溶解氧,进而导致水质恶化 [1] [2]。因此,很多国家和地区将磷规定为水体有机污染的一种指示物,例如,中国地表水环境质量标准分为五类,其中I类水水质要求总磷(TP)控制在0.02 ppm以下。因此,开发简单、快速、可靠、经济有效的方法,实现对水体中磷酸盐的灵敏和选择性检测具有重要意义。
目前已经建立了诸多用于磷酸盐检测的方法,如比色法、电化学法、荧光传感法、生物传感法和离子色谱法等 [3] [4] [5] [6]。基于磷钼蓝络合物的比色技术是我国规定的检测水环境中可溶性磷酸盐的标准方法,但是该方法易受到硅酸盐的干扰,此外,该方法的检出限仅为0.01 ppm,尚不能满足对清洁地表水和地下水的检测要求。近年来,荧光传感方法因其响应快速、灵敏度高、操作简便和可视化等优点而备受关注 [7] [8]。特别是基于镧系元素的发光材料,由于其较大的斯托克斯位移、长荧光寿命、清晰尖锐的发射曲线等光学特性,被研究者们广泛研究 [9] [10] [11]。目前已开发了多种基于镧系元素荧光的磷酸盐传感方法。在这类荧光检测方法中,镧系离子与磷酸盐的氧原子结合可以抑制配体向镧系离子的能量转移,进而导致镧系离子的荧光猝灭,实现磷酸盐的测定 [12] [13] [14] [15] [16]。然而,这些可有效敏化稀土元素发光的有机桥接配体是有限的,这将限制镧系荧光传感的进一步发展。此外,这些传感方法仍具有操作过程繁琐、成本高和耗时长等问题,因此,急需开发其他简便、快速的镧系荧光传感策略用于磷酸盐检测。
在这项工作中,基于十二烷基苯磺酸钠(SDBS)促进的能量转移过程开发了左氧氟沙星(LFLX)-Eu3+配合物荧光探针用于磷酸盐的灵敏选择性检测。如方案1所示,低浓度的表面活性剂SDBS可作为能量转移的敏化剂显著增强LFLX向Eu3+的能量转移,使Eu3+发出强特征荧光,由此构建了SDBS敏化能量转移的LFLX-Eu3+配合物荧光传感。由于Eu3+离子与磷酸盐中氧原子的强配位结合作用可削弱LFLX向Eu3+的能量转移,因此磷酸盐的加入可淬灭Eu3+的特征荧光,并使LFLX的荧光恢复。基于该探针的双发射荧光响应,可以实现对Pi的荧光检测,并可成功用于废水和地表水中总磷的测定。
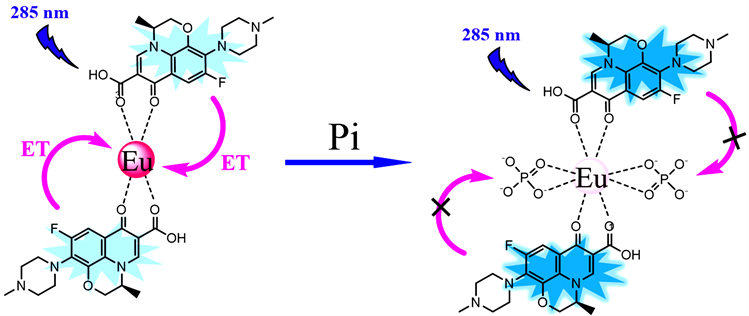
Scheme 1. Schematic illustration of the strategy for the detection of phosphate based on energy transfer mechanism (ET) from LFLX to Eu3+ induced by SDBS
方案1. 基于SDBS引起LFLX-Eu3+的能量转移(ET)机制用于磷酸根检测
2. 实验部分
2.1. 实验试剂与仪器
实验中使用的所有试剂至少是分析纯度。左氧氟沙星(LFLX)、六水合硝酸铕(Eu(NO3)3∙6H2O)、十二烷基苯磺酸钠(SDBS)和磷酸钠(Na3PO4)购自上海阿拉丁化学有限公司。抗坏血酸、钼酸铵((NH4)6Mo7O24∙4H2O)、酒石酸钾(C4H4KO7Sb∙0.5H2O)、硫酸(H2SO4)、氢氧化钠和三羟甲基氨基甲烷(Tris)购自国药集团化学试剂有限公司。其他的无机金属盐类药品均为分析纯,购自国药集团化学试剂有限公司。实验中使用的去离子水(18.25 MΩ∙cm)由UPK/UPT净水系统制备。
样品的荧光光谱由F-7000荧光光谱仪(日立,日本)进行测定,激发光源为氙灯,激发和发射狭缝均为5 nm,光电倍增管电压为400 V。所有pH测量均在FE28标准pH计(Mettler Toledo, Switzerland)上进行。
2.2. 荧光探针的构建及对磷酸盐的定量与选择性检测
在5.0 mL的比色管中,依次加入一定量的如下溶液:200 μL的Tris-HCl缓冲溶液(1 × 10−5 mol∙L−1,pH = 8.0)、160 μL的LFLX溶液(2 × 10−5 mol∙L−1)、160 μL的Eu3+溶液(2 × 10−5 mol∙L−1)和12000 μL的SDBS溶液(5 × 10−4 mol∙L−1),构筑LFLX-Eu3+配合物荧光探针。
向探针中分别加入0 μM、0.1 μM、0.2 μM、0.5 μM、1.0 μM、2.0 μM、5.0 μM、10 μM、15 μM、20 μM、25 μM的Pi,最后用去离子水定容至4.0 mL。样品混合均匀后在室温下静置反应20 min,最后使用荧光光谱仪在激发波长为285 nm,激发狭缝和发射狭缝为5 nm条件下,依次测定各样品在350~680 nm内的荧光光谱。以450 nm处的荧光强度值作为Pi浓度的函数,用于Pi的定量分析。在选择性试验中,用其他可能的干扰物质代替Pi,采用相同的测定方法进行分析检测,探究该荧光探针对Pi的选择性。
2.3. 实际样品预处理及总磷测定
水样采集:水样分别采自南通市河湖地表水和生活废水。
水样预处理:取采集水样25 mL于50 mL锥形瓶中,加入3 mL浓硝酸和数粒沸石,摇匀之后在电热板上加热浓缩至10 mL;如水样仍然浑浊,再加入2 mL浓硝酸继续加热,直至水样变得澄清透明,继续加热水样至近干;冷却后加入10 mL高纯水溶解残余物,并用NaOH溶液(1.0 mol∙L−1)调水样pH至中性,然后将其转移至25 mL比色管中,用高纯水定容至25 mL。
水样测定:向荧光探针中加入一定量的预处理水样样品,采用与上述定量分析相同的测定过程,分析样品中总磷含量。此外,采用国标中的钼酸铵分光光度法对水样中总磷含量进行测定。
3. 实验结果与讨论
3.1. 荧光探针的构建及对磷酸盐的传感机制
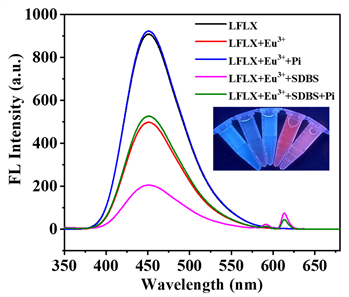
Figure 1. Fluorescence spectra of LFLX, LFLX + Eu3+, LFLX + Eu3+ + Pi, LFLX + Eu3+ + SDBS, LFLX + Eu3+ + SDBS + Pi. Theinset is the corresponding fluorescence color images under 365 nm UV lamp. LFLX: 20 μM, Eu3+: 20 μM, SDBS: 500 μM, Pi: 10 μM, Tris-HCl buffer: 50 mM (pH = 8.0), λex = 285 nm
图1. LFLX、LFLX + Eu3+、LFLX + Eu3+ + Pi、LFLX + Eu3+ + SDBS、LFLX + Eu3+ + SDBS + Pi的荧光光谱图。插入图片是各体系在365 nm紫外灯下的荧光颜色图。LFLX:20 μM,Eu3+:20 μM,SDBS:500 μM,Pi:25 μM,Tris-HCl buffer:50 mM (pH = 8.0),λex = 285 nm
该传感体系的荧光表征和发光机理如图1所示。由荧光光谱图(图1)可以看出,在SDBS加入之前, LFLX在450 nm处具有显著明亮的蓝色荧光,当Eu3+加入到LFLX溶液中时,LFLX的荧光强度被淬灭,这是由于LFLX-Eu3+配合物的形成,LFLX向Eu3+进行了能量转移。然而,Eu3+在615 nm处没有发出特征荧光,说明LFLX向Eu3+的能量转移较弱,不能有效敏化Eu3+发光。当向LFLX-Eu3+体系中加入Pi后,由于Eu3+与磷酸根中的氧原子具有强亲和作用,从而削弱了LFLX到Eu3+的能量转移过程,导致LFLX的部分荧光恢复 [17] [18]。
一般来说,当表面活性剂的浓度达到临界胶束浓度(CMC)时,可以极大地改变体系的微环境,减少分子碰撞过程中的非辐射能量损失,所以表面活性剂通常作为敏化剂应用于荧光体系中,此外,胶束的疏水环境也有利于提高体系的荧光量子产率 [19]。当表面活性剂SDBS加入到LFLX-Eu3+体系时,LFLX的荧光被显著淬灭,Eu3+在615 nm处的特征荧光明显增强,且LFLX-Eu3+体系荧光颜色由蓝色变为红色(图1中插入图片)这表明SDBS可以促进LFLX向Eu3+的能量转移,这是关于表面活性剂作用的一个有趣新发现。当向SDBS调控的LFLX-Eu3+体系中加入一定量的磷酸根后,LFLX的荧光又基本恢复,Eu3+的特征荧光显著降低,这可能是由于SDBS可促进Eu3+与磷酸根中氧原子的结合,阻断了LFLX向Eu3+的能量转移。因此基于Pi引起的LFLX和Eu3+双荧光信号变化,可以实现对Pi的荧光检测。此外,可在紫外灯照射下裸眼观察LFLX-Eu3+配合物体系加入磷酸根前后的荧光颜色变化,表明该荧光探针可用于Pi的快速可视化检测。
3.2. 荧光探针构建及传感条件优化
为构建对Pi具有灵敏性响应的LFLX-Eu3+荧光探针,对探针体系中LFLX和Eu3+的组成比(LFLX/ Eu3+)、SDBS浓度、pH以及该探针对Pi的响应时间等实验条件进行了优化。
3.2.1. LFLX浓度的优化
在LFLX-Eu3+荧光探针中,LFLX和Eu3+的组成比(LFLX/Eu3+)可直接影响该探针的发光特性。如图2所示,在Eu3+浓度为20 μM时,探究了不同LFLX/ Eu3+值对该探针在加入Pi前后荧光光谱的影响。在加入Pi之前,探针体系中LFLX特征荧光较弱,随着LFLX相对浓度增加,其荧光逐渐增强,且Eu3+具有显著的特征荧光(图2(A))。加入Pi之后,由于Pi与Eu3+的配位结合,LFLX荧光恢复(图2(B));当LFLX/ Eu3+值为1:1,即LFLX浓度为20.0 μM时,LFLX的荧光强度恢复最为显著(图2(C)),且Eu3+荧光被显著淬灭,说明此时荧光探针对Pi具有灵敏性荧光响应。因此,选择LFLX/ Eu3+组成比1:1进行荧光探针的构筑。
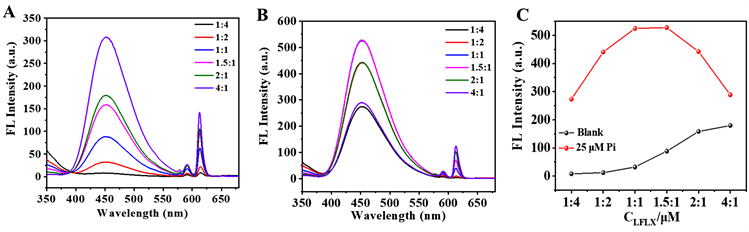
Figure 2. Effect of LFLX/Eu3+ on fluorescence spectra of the fluorescent probe before (A) and after (B) addition of 25 μM Pi, respectively. (C) Effect of LFLX/Eu3+ on fluorescence intensity of LFLX before and after addition of Pi
图2. LFLX/Eu3+对荧光探针在加入25 μMPi前(A)、后(B)的荧光光谱影响;(C) LFLX/Eu3+对探针在加入Pi前后的LFLX荧光强度影响
3.2.2. SDBS浓度的优化
表面活性剂可作为敏化剂来增强某些体系的荧光强度。但是,本工作发现表面活性剂SDBS并非增强了探针的发光强度,而是作为能量转移的敏化剂促使LFLX向Eu3+的能量转移,从而增强Eu3+荧光,并使LFLX荧光淬灭,由此构建具有Eu3+特征荧光的LFLX-Eu3+配合物荧光探针。SDBS浓度对LFLX-Eu3+探针体系荧光光谱的影响结果如图3所示。结果表明,当SDBS浓度为1.0 × 10−4 mol∙L−1时,LFLX向Eu3+向的能量转移效率最高,Eu3+特征荧光增强最为显著(图3(A))。这是由于SDBS可以通过形成胶束改变溶液体系的微环境,从而促进LFLX向Eu3+向的能量转移,敏化Eu3+发光。当向探针体系中加入Pi后,Eu3+荧光淬灭,LFLX荧光恢复(图3(B)),且当SDBS浓度为1.0 × 10−4 mol∙L−1时,LFLX的荧光恢复效率(F−F0)/F0达到最大值(图3(C)),说明此时荧光探针对Pi具有灵敏性荧光响应。因此选取浓度为1.0 × 10−4 mol∙L−1的SDBS用于LFLX-Eu3+配合物荧光探针的构筑。
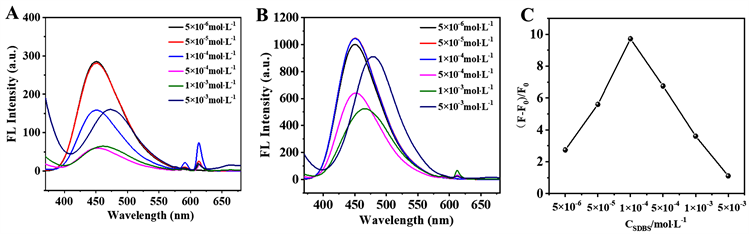
Figure 3. Effect of SDBS concentration on fluorescence spectra of the fluorescent probe before (A) and after (B) addition of 25 μM Pi, respectively. (C) Effect of SDBS concentration on the fluorescence recovery efficiency of LFLX after the addition of Pi. F0 and F represent the LFLX fluorescence intensity of the probe before and after the addition of Pi, respectively
图3. SDBS浓度对荧光探针在加入25 μM Pi前(A)、后(B)的荧光光谱影响。(C) SDBS浓度对探针LFLX荧光恢复效率的影响。F0和F分别是探针加入Pi前后的LFLX荧光强度值
3.2.3. pH优化
pH值对荧光传感体系具有显著的影响,特别是对于含有酸性或者碱性基团的因荧光化合物。从图4(A)可以看出,pH的变化对LFLX-Eu3+体系中LFLX的荧光强度并未产生明显影响,但是在不同pH值条件下,LFLX-Eu3+体系对Pi的荧光响应结果却出现显著性差异,该结果表明,用于Pi检测的CIP-Eu3+体系具有显著地酸碱依赖性。造成上述现象的原因可能是在酸性条件下,
和
与Eu3+离子有微弱的相互作用,而在碱性条件下,Eu3+可以与-OH配位形成不溶性的水合氧化物Eu(OH)3。由图4(B)可以看出,当pH = 8时,磷酸根可以使LFLX的荧光恢复效率
达到最大值,因此选择pH = 8作为传感条件。
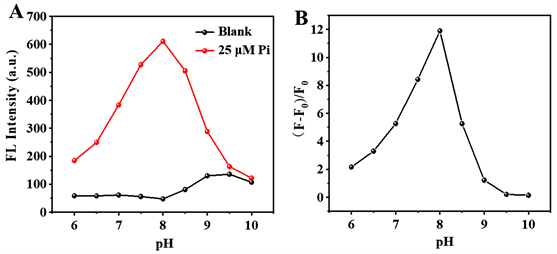
Figure 4. (A) Effect of pH on LFLX fluorescence intensity of the fluorescent probe before and after addition of 25 μM Pi. (B) Effect of pH on the fluorescence recovery efficiency of LFLX after the addition of Pi. F0 and F represent the LFLX fluorescence intensity of the probe before and after the addition of Pi, respectively
图4. (A) pH对荧光探针在加入25 μM Pi前、后的LFLX荧光强度影响。(B) pH对探针LFLX荧光恢复效率的影响。F0和F分别是探针加入Pi前后的LFLX荧光强度值
3.2.4. 响应时间优化
响应时间是影响荧光传感方法的一个重要因素。如图5所示,当向LFLX-Eu3+体系中加入Pi并充分混合后,LFLX的荧光强度逐渐增强,且其荧光强度在15 min后达到最大,并可在60 min内保持稳定,因此选择平衡时间20 min用于Pi的分析检测。

Figure 5. Effect of equilibration time on the LFLX fluorescence intensity of the LFLX-Eu3+ system after addition of Pi
图5. 响应时间对探针体系加入Pi后的LFLX荧光恢复影响
3.3. 荧光探针对磷酸盐的定量分析
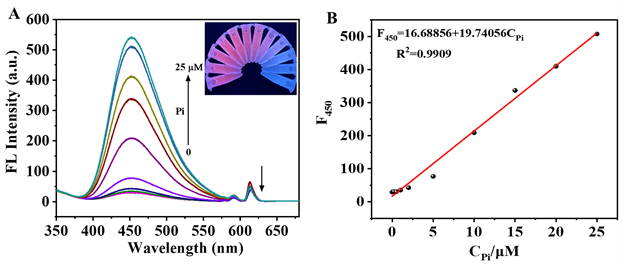
Figure 6. (A) The fluorescence spectra of LFLX-Eu3+ system in the presence of Pi with different concentrations. Inset is the corresponding fluorescence images under 302 nm UV lamp. (B) Linear relationship between fluorescence intensity of LFLX (F450) and Pi concentration
图6. (A) LFLX-Eu3+荧光探针对不同浓度Pi的荧光响应光谱。插入图片为302 nm紫外灯下的荧光图。(B) LFLX荧光强度(F450)与Pi浓度之间的线性关系图
在优化条件下,探究了LFLX-Eu3+荧光传感体系对不同浓度Pi的荧光响应。如图6(A)所示,随着探针体系中磷酸盐浓度的增加,Eu3+的特征荧光被淬灭,而LFLX的荧光逐渐增强(图6(A))。如图6(B)所示,在0.1~25 µM的浓度范围内,磷酸根浓度和左氧氟沙星的荧光强度呈良好的线性关系,线性方程式为F450 = 19.74056 + 16.68856CPi (R2 = 0.9909),方法检出限(S/N = 3, n = 11)为0.027 µM (以P计为0.84 µg/L),远低于我国环境质量标准中地表水I类水质标准(总磷 ≤ 0.02 mg/L)。且该方法检测灵敏度远高于目前已报道的其他磷酸盐分析方法(表1),此外,随着磷酸盐加入浓度的增加,探针体系的荧光颜色逐渐由红色变为蓝色(图6(A)中插入图片),因此根据探针荧光颜色变化可实现对磷酸盐的可视化半定量检测,方法检测简便、快速。

Table 1. Comparison of the analytical performance of LFLX-Eu3+ system and other analytical methods for the determination of Pi
表1. LFLX-Eu3+配合物荧光探针与其他Pi分析方法的比较
a每种方法的最大相对标准偏差值。
3.4. 荧光探针对磷酸盐的选择性分析
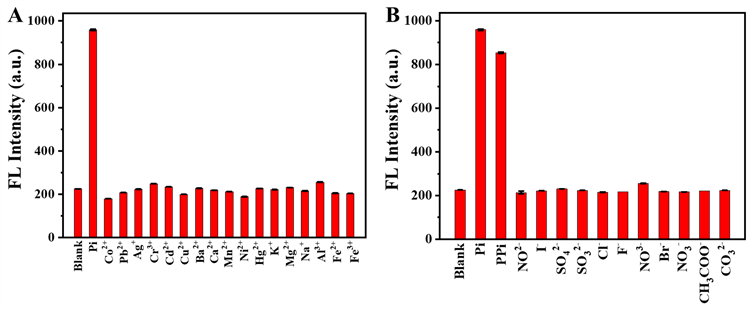
Figure 7. Selective response of LFLX-Eu3+ fluorescent probe to different cations (A) and anions (B)
图7. LFLX-Eu3+荧光探针对不同阳(A)、阴离子(B)的选择性响应结果
实现对实际样品中目标物的高选择性检测是荧光传感方法应用的前提。考虑到该荧光探针主要应用于环境样品检测,因此考察了LFLX-Eu3+探针体系对环境样品中其他可能共存的阴、阳离子的荧光响应,以评价其对磷酸盐检测的选择性。如图7所示,除焦磷酸根(PPi)对LFLX-Eu3+荧光探针体系有干扰外,荧光探针对其他常见的金属离子如Ni2+、Mn2+、Cu+、Hg2+、K+、Ca2+、Na+、Mg2+、Pb2+、Ag+、Cd2+、Co2+、Al3+、Ba2+、Fe2+、Fe3+,以及常见的阴离子如
、NO3−、
、CH3COO−、F−、Cl−、Br−、I−、
均没有明显的荧光响应。这是由于Eu3+离子与磷酸根或焦磷酸根中氧原子之间具有较强的特异性亲和作用。对环境样品中总磷的检测,需要将样品中各种化学形式的磷转化为正磷酸盐,在样品消解过程中,焦磷酸盐可转化为正磷酸盐,因此可以忽略焦磷酸盐的干扰。对于其他有机化合物,由于其存在浓度很低(ng/L水平),并且在样品消解过程中几乎所有的有机化合物会被去除,因此不干扰磷酸盐的测定。上述结果表明LFLX-Eu3+探针体系对磷酸盐具有较高的选择性,可应用于实际水样中总磷的测定。
3.5. 水样中总磷的测定

Table 2. Total phosphase detection in real water samples using the proposed method and the phosphomolybdenum blue spectrophotometric method
表2. 本方法与磷钼蓝分光光度法对水样中总磷的分析测定
在自然环境中,不同磷的化合形态之间可以相互转化,而总磷通常作为水体富营养化的污染指标,因此对于环境样品来说,总磷的检测似乎更有意义。为了了解总磷在环境介质中的局部污染情况,采集了污水、河水、湖水,将这些样品中的含磷物质通过浓硝酸消解法转化成正磷酸根,然后将本方法应用于消解水解的测定,并将测定得到的磷酸根浓度转换为总磷浓度,测定结果如表2所示。结果表明,本方法的检测标准偏差(RSD)介于2.1%~5.8%,且测得的总磷浓度与国标中规定的磷钼蓝分光光度法检测结果具有较好的一致性,表明该荧光传感方法的检测准确性。此外,通过标准加入法考察了该方法对样品中总磷的回收率情况,测定结果如表3所示。荧光探针对样品中总磷的回收率为90.0%~102.0%,RSD小于5.3%,说明本方法可实现对样品中总磷的可靠检测。因此,本工作开发的荧光探针在评估环境样品中总磷含量方面具有一定的应用前景。

Table 3. Total phosphase detection in spiked water samples
表3. 加标水样中总磷含量的同时检测
4. 结论
本论文工作基于表面活性剂对天线效应的敏化作用,构建了一种用于环境样品中磷酸盐灵敏选择性检测的LFLX-Eu3+配合物荧光传感体系。该荧光探针可实现0.1~25 μM磷酸盐的定量检测,检测限为0.027 μM,且环境样品中常见的阴、阳离子对磷酸盐的检测未产生明显干扰。总磷含量是样品经消解后将各种形态的磷转变成正磷酸盐后测定的结果,本方法已成功应用于废水和地表水中总磷的测定,在评估环境样品中总磷含量方面具有一定应用前景。本工作不仅为环境样品中总磷的测定提供了快速、简便方法,而且为基于能量转移的荧光探针构建提供了新的思路。
基金项目
本项目由国家自然科学基金(批准号:22106076)和南通大学博士科研启动基金支持。
NOTES
*通讯作者。