1. 引言
扑热息痛是一种退烧和缓解疼痛的药物,主要成分是对乙酰氨基酚(APAP),可用于治疗成人和儿童的发烧、神经痛和关节炎等病症 [1] 。据报道,每年以片剂、糖浆和注射剂的形式消耗的APAP大约3~3.5万吨之多。然而,过量消耗APAP产生排放问题,导致严重的水污染 [2] 。更值得注意的是,其在水中的自然降解会产生有害化合物,人体摄入会引发急性肝肾衰竭,甚至会导致人类、动物或其他水生生物死亡。例如,APAP通过水解而产生的4-氨基苯酚对肾脏的毒害效果明显,甚至会导致肾脏畸形 [3] 。因此,对人类体液和环境中的APAP的检测关乎人类健康。目前的检测的技术有质谱 [4] 、滴定 [5] 、电泳 [6] 、高效液相色谱 [7] 、化学发光 [8] 、电化学 [9] 和光电化学传感器 [10] 等。在这些方法中,电化学传感法由于其高效、低成本、便携、灵敏和小巧等优点而前景广阔。
在电化学传感器的构建过程中,修饰电极的材料选择是十分重要的。通常使用的材料有金属、金属氧化物、导电聚合物或不同的纳米碳等 [11] 。Campos等 [12] 制备了尺寸较大的碳球壳,将这些碳球壳均匀地涂在玻碳电极上,用于构建高效的电化学传感器检测汗液、唾液和尿液中的APAP,结果令人满意。Kushwaha的课题组 [13] 采用壳聚糖接枝聚苯胺包裹氧化铁来研究扑热息痛的电化学传感。线性范围是5 μM~100 μM,检测限为5.7 μM。虽然先前制备的多孔碳材料效果不错,但也有一些优缺点,如稳定性和再现性稍差。通过控制材料的尺寸,对材料复合、掺杂加以改善。具有纳米颗粒的复合材料提高了功能性、灵活性和相互作用等特性 [14] 。
本工作中,以胡萝卜为碳前驱体,采用化学活化法制备的多孔碳PCMC。活化剂是KOH,可以与碳反应,刻蚀部分碳骨架,生成的K2CO3并不稳定,分解产生CO2帮助造孔,增加了材料的比表面积。通过条件优化,得到了一种能检测APAP的化学修饰电极。
2. 实验部分
2.1. 试剂及仪器
对乙酰氨基酚购于阿拉丁化学试剂公司。实验涉及的其他化学品均为分析纯,直接使用。实验过程中去离子水来自UIUPURE (UPC-I-10T)系统。
实验使用的是上海辰华CHI660E电化学工作站。在室温下(约300 K),在含有10 mL PBS溶液的电解槽中进行。采用传统三电极系统,工作电极为裸或修饰的玻碳电极(上海辰华,d = 3 mm),对电极选取铂丝,参比电极则是饱和甘汞电极。用pH-3c数字pH计(上海雷磁)测量缓冲液的pH值。X射线光电子能谱(XPS)在扫描X射线微探针PHI Quantera II (Ulvac-PHI, INC)和C60枪上进行。用X射线衍射仪(XRD,Bruker-D8-advance,Cu k α辐射k = 0.15418 nm)和拉曼光谱仪(Raman, Renishaw invia)研究了其结构。用扫描电子显微镜(SEM, Gemini SEM 300)和透射电子显微镜(TEM, je-2100hr)对其形貌进行了表征。BET测量由TriStar II 3020 Version 3.02 (Micromeritics Instrument Corporation)执行。
2.2. 修饰电极的制备
将胡萝卜洗净切成1立方厘米左右的小块,放入烘箱中120℃干燥36 h。将干燥的胡萝卜用研钵碾碎,过筛备用。称取一定质量的KOH也用研钵碾碎,按照质量比KOH:C = 3:1的放置在瓷舟中,在氮气环境下,管式炉中进行直接碳化。升温速率为5℃ min−1,氮气的流速为15 mL min−1。碳化结束先后用2 M HCI和超纯水清洗3次,干燥24 h。将制备的材料命名为PCMC,取5 mg超声分散到5 mL DMF中。经优化,最佳的修饰量为5 μL。控制其它因素不变,将不加入KOH制得的材料记作未活化PCMC。
将5 μL浓度为1 mg mL−1的PCMC均匀悬液滴到抛光后的玻碳电极上,室温下干燥备用。
3. 结果与讨论
3.1. PCMC的表征
图1(a)、图1(b)分别为扫描电镜与透射电镜图。显示PCMC呈片状结构。

Figure 1. (a) SEM and (b) TEM of PCMC
图1. PCMC的(a) 扫描电镜和(b) 透射电镜
扫描电镜图可以看到材料表面的褶皱和塌陷,这样疏松的结构有利于目标分析物从缓冲溶液中吸附到电极表面。透射电镜图进一步确认PCMC为具有多孔形态的非均匀结构。这种结构有大的比表面积,以便更好地用于传感。透射电镜图中可以观察到片状碳的厚薄不均一,孔隙分布均匀。
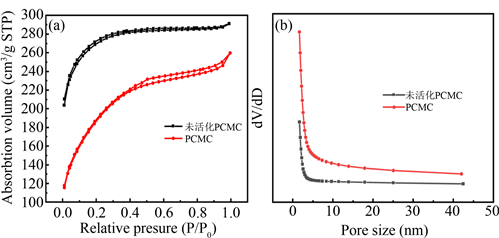
Figure 2. (a) N2 adsorption-desorption isotherms; (b) Pore size distribution
图2. (a) 氮气吸附–解吸等温线和;(b) 孔径分布图
图2(a),从氮气吸附和脱附等温线来看,无论活化与否,均为可逆吸附,材料以微孔结构为主。图2(b)为孔径分布图,经测试得平均孔径分别为1.82 nm和1.12 nm。比表面积分别为251.51 m2g−1和640.12 m2g−1。比表面积大可能是分子内氢键的相互作用,保证了结构的稳定性,改善了2维的平面化程度,增大活性面积。
PCMC和未活化PCMC的XRD曲线如图3所示。峰的演化表明,活化剂KOH的加入,对PCMC的002和100晶面影响不大。材料仍以无定形为主。
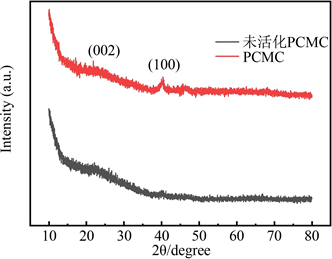
Figure 3. XRD patterns of PCMC and unactivated PCMC
图3. PCMC和未活化PCMC的XRD图谱
图4为PCMC的XPS图。XPS的图谱表明材料表面氧含量较低,C主要以C = C-C、C-O、C-N等形式存在,O主要以水,酚羟基,羰基羧基等形式存在。

Figure 4. (a) XPS spectra of PCMC; (b) XPS C 1s spectra of PCMC; (c) XPS O 1s spectra of PCMC
图4. (a) PCMC的XPS图;(b) C 1s的分峰图和(c) O 1s的分峰图
3.2. 不同电极的电化学行为研究
以循环伏安法(CV)研究了APAP在不同电极上的电化学响应。如图5(a)所示,APAP在裸GCE上的氧化还原峰非常弱峰(曲线a),PCMC修饰的GCE表现出一对明显的氧化还原峰,对应于APAP的氧化(0.35 V)和还原(0.25 V) (曲线c),修饰后电极在不含APAP的PBS中没有任何峰出现(曲线b)。此外,当制备的PCMC被修饰到GCE表面时,这对氧化还原峰的电流响应也大大增加,且背景电流也有一定程度的增加,这可能是由于PCMC的大表面积和更好的电导率。PCMC能进一步增加APAP的电极反应的原因主要是由于两个方面。首先,APAP在PCMC/GCE上,可能发生表面包膜行为与单层吸附的结合过程。因此,PCMC可以在电极表面吸附更多的APAP分子,从而获得更高的灵敏度 [15] 。其次,将PCMC引入电极表面可以通过在多孔碳和APAP分子之间形成超分子配合物来提高检测灵敏度 [16] 。因此,PCMC/GCE为对APAP的电化学测量提供了一个优越的反应界面。
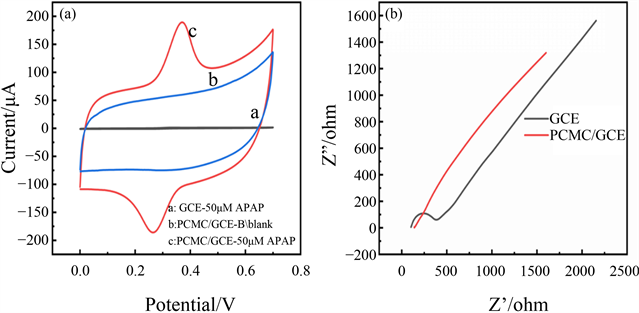
Figure 5. (a) Cyclic voltammetry of the PCMC/GCE and GCE in PBS containing 50 μM APAP; (b) Nyquist plots of impedance spectra of different electrodes
图5. (a) 修饰电极PCMC/GCE与裸电极GCE在50 μM APAP的PBS中的CV图;(b) 不同电极的交流阻抗图
使用电化学阻抗谱(EIS),在含5 mM Fe [(CN)6]3−/4−的0.1 M氯化钾溶液中,研究了裸GCE和PCMC/GCE的电子转移能力。如图5(b)所示,与GCE电极相比,PCMC/GCE的Rct值非常小,这主要是因为PCMC纳米材料具有较大的比表面积,因而具有较高的电子转移能力。
3.3. pH的影响
图6(a)为PCMC修饰的GCE,在不同pH的PBS溶液(6.3~7.8)中,APAP的循环伏安曲线。可以看到,随着pH值的增加,APAP的氧化和还原电位都负移,这表明APAP的电化学反应涉及质子的转移。如图6(b)所示,峰电位与pH的线性关系经拟合为:
(1)
(2)
其斜率值与Nernst方程得出的理论值非常接近 [17] ,表明APAP的氧化还原是一个伴随着等质子和等电子的过程。此外,图6(c)说明了氧化峰电流与pH值之间的关系。峰电流在6.3~7.2之间增加,在7.2~7.8之间减小。因此,选择pH = 7.2来测量APAP。
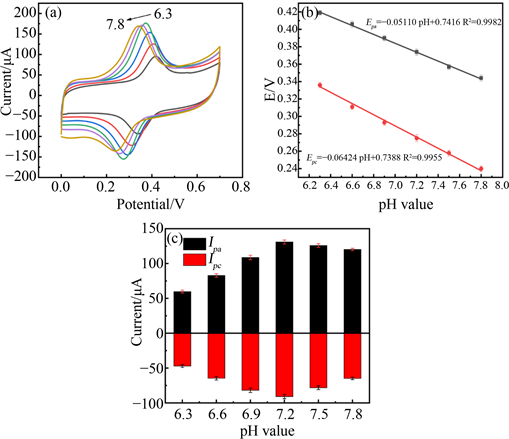
Figure 6. (a) CVs of PCMC/GCE in 0.2 M PBS with different pH containing 50 μM APAP; (b) Effect of pH value on the peak potentials; (c) Effect of pH value on the peak currents. Scan rate: 100 mV s−1
图6. 在不同pH的0.2 M PBS溶液中,(a) 50 μM APAP在PCMC/GCE上的CV曲线;(b) pH值对峰电位的影响;(c) pH值对峰电流的影响;扫描速率:100 mV s−1
3.4. APAP的定量检测
为了研究PCMC/GCE的传感性能,我们采用DPV进行定量分析。图7(a)为在最优化的实验参数下,不同浓度APAP在PCMC/GCE上的氧化峰信号。如图7(b)所示,线性回归方程为:
(3)
(4)

Figure 7. (a) DPVs of APAP with different concentrations from 0.01 μM to 50 μM; (b) The linear relationship between peak current and concentration of APAP
图7. (a) 不同浓度APAP在PCMC/GCE上的DPV曲线;(b) 氧化峰电流与浓度的关系
峰电流与0.01 µM~50 µM范围内的APAP浓度呈现分段线性关系。据LoD = 3 S/m计算该方法的检测限为6.18 nM。材料的高灵敏度可能与材料界面的结构以及高电导率有关,修饰电极材料表面积的增加也会导致电催化活性的增加 [18] 。综合分析特性表明,PCMC/GCE可作为对APAP定量分析的电化学传感器。
3.5. 稳定性和选择性
为了验证PCMC/GCE的选择性和稳定性,在含50 µM的0.2 M PBS (pH = 7.2)溶液中进行CV测定。通过比较50 μM APAP和加入干扰离子的CV氧化峰信号,说明双酚A、对硝基酚、香草醛、草甘膦、敌百虫、对苯二酚等都对检测APAP没有影响(图8(a))。
通过使用同一电极对50 μM APAP进行60次重复测量,研究了其的稳定性(图8(b))。结果发现,其初始电流响应并未发生太大改变。同样,通过连续测量50 μM APAP的电流响应,峰电流几乎没有下降。稳定性令人满意。
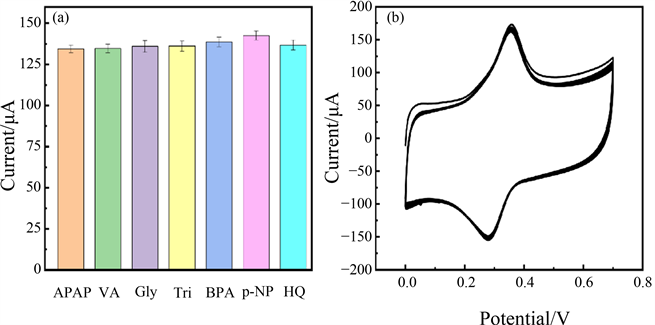
Figure 8. (a) Effect of different interferents; (APAP, Acetaminophen; VA, Vanillin; Gly, Glyphosate; Tri, Trichlorfon; BPA, Bisphenol A; p-NP, p-nitrophenol; HQ, Hydroquinone); (b) The cyclic voltammetry curves for 60 cycles of PCMC/GCE in 0.2 M PBS containing 50 μM APAP
图8. (a) 50 μM APAP中加入不同杂质的电流柱状图(APAP,对乙酰氨基酚;VA,香兰醛;Gly,百草枯;Tri,敌百虫;BPA,双酚A;p-NP,对硝基酚;HQ,对苯二酚);(b) PCMC/GCE在含有50 μM APAP的0.2 M PBS溶液中扫描60次的CV曲线
4. 结论
本工作以胡萝卜为碳源,氢氧化钾为活化剂,制备生物质碳材料(PCMC)。对材料的形貌及其结构进行了表征。以PCMC修饰玻碳电极,用于对乙酰氨基酚的测定。结果表明:在0.01 µM~50 µM范围内,对乙酰氨基酚的浓度与电流呈现分段线性关系,检测限为6.18 nM。PCMC/GCE的抗干扰能力强并具有较好的选择性,制作成本低,因此可作为未来对乙酰氨基酚传感的一种不错的替代方案。
基金项目
南通大学大学生创新训练项目资助(202310304174H)。
NOTES
*通讯作者。