1. 引言
乳癌在东方女性,发生的年龄层较西方女性大约年轻10~15年。在台湾,平均女性乳癌年龄是52.2岁;而自35岁开始发生率就呈现增加的趋势。根据台湾卫生署较新资料显示,乳癌是台湾女性癌症发生率第一位,约为每十万名妇女188~194人。在卫生福利部死因统计数据中显示女性乳癌标准化发生率为69.1 (每十万人口)、标准化死亡率是12.0 (每十万人口)、死亡率是第四位 [2] 。
有鉴于此,施行了将近15年的每两年一次免费的乳腺X线摄影,也确实有效的提早发现零期及早期的乳癌。此项筛检计划涵盖45~69岁间的妇女,符合的妇女可以在就近的医疗院所或是政府提供的乳房摄影巡回车上,再由放射影像专科医师判读后以信函通知妇女本人是否需要进一步回医院诊治。针对这些定义为早期乳癌的病患,其肿瘤大小皆小于三公分;腋下淋巴结也较未有肿瘤转移的现象。若将其乳房全部切除,对于患者身心灵皆有可能产生不适及影响其生活质量。
2. 保留式乳房切除与传统术后放射治疗
因此保留式乳房切除(Breast Conserving Surgery)对于早期的乳癌已被视为一合理的手术方式。但必须配合全乳房的放射线治疗才可以达到相等安全的疾病控制及减少日后乳癌复发之可能 [3] [4] 。
传统的术后放射治疗是采取全乳房照射,以每次200 Gy分次把6000~6500 Gy的剂量完成;需要30至35天的连续治疗方式。对于职业型妇女恐会造成治疗时间过于冗长的负荷,而因此干脆选择乳房全切除(total mastectomy)的过度治疗方式。传统术后放射线治疗的副作用(如皮肤纤维化、皮肤增厚、疤痕挛缩、皮下血管增生等),自照射完三个月到终身都有可能出现。这也令不少妇女因此却步,而宁可做出非属本意的接受全部乳房切除方式。
而目前引进的术中放射治疗,则避免了治疗时间冗长及造成患侧皮肤伤害的缺点。将肿瘤及周围一公分的乳腺切除后,经病理冷冻切片确定切除边缘无残留癌组织,就可以利用刚切除完后的空腔,进行一次性的放射治疗 [5] ,剂量为20 Gy,费时大约八至九分钟。手术腔的放射治疗完成后,乳房的伤口即可进行缝合及微整形(oncoplasty)。病人于术后第二天即可拔除放置于腋下淋巴摘除的引流管及出院(见表1)。
3. 材料与方法
3.1. 患者一般特征
本院于2015年1月至2018年1月,总共施行了六十例早期乳癌的保留式乳房切除及术中放射治疗。病人的平均年龄为56岁。根据AJCC (American Joint Committee on Cancer) 乳癌分级制度:其中零期18例、第一期(IA) 26例、第二期(IIA) 15例及(IIB) 1例。所有非零期的乳癌病人皆同时接受腋下哨兵淋巴摘除术。
术后淋巴结阴性的有33人(55%);有9人淋巴结呈现N1 (15%)的转移(转移数少于3颗淋巴结)。针对有淋巴结转移的病人,将给予术后化学治疗及乳房体外放射治疗五次,以达到更安全的疾病控制(见表2)。
3.2. 术中放射治疗之适应症
根据美国FDA的制定建议,年龄四十岁以上;肿瘤小于三公分,术前腋下没有发现可触摸到的肿大淋巴结之早期乳癌的病患,可为作为施行IORT之人选。
3.3. 手术方法
手术施行方式如下(以下照片已取得病人本人同意并进行拍摄):把恶性肿瘤及其周围组织切除后(见图1),即刻送到病理科作冰冻切片检查,以确定肿瘤的切除边缘为无癌组织残留。在此同时,可先进行腋下哨兵淋巴的摘除步骤。等待病理科回报结果后,就可以把X光放射源置入手术腔中。X光射源为一特别之管状物,末端有一30 cm3的水球。X光射线放射出来时是以此30 cm3球体的周围一公分为辐射涵盖区域。我们在照射中必须同时保护患者乳房下方的肋骨及内脏器官,因此会以小型铅片置于肿瘤下方或胸大肌后方作为射线之屏障(见图2)。当水球、射源棒都和主机器接合后(见图3),由放射肿瘤科专科医师执行按下开关键,手术房人员退到铅板保护区,历时8~9分钟后过程结束。将水球及射源移除后,手术医师继续把乳房伤口作缝合(见图4)。
4. 讨论
在国外针对保留式乳房切除后进行IORT有两大型的临床研究:ELIOT及TARGIT-A临床实验。在

Table 1. Comparison of traditional radiotherapy with intraoperative radiotherapy
表1. 传统放射治疗与术中放射治疗的比较
参考ASTRO (American Society for American Oncology)及NCCN制定建议。

Figure 1. Surgical cavity after safety margin of tumor removal
图1. 保留乳房手术,肿瘤切除后之手术腔
其分析中,术中放射线治疗其效果不亚于术后的全乳房放射治疗 [6] [7] ,尤其对于患者的病况属于较低局部复发风险(肿瘤荷尔蒙接受体阳性、HER-2阴性者)。而本院于短期的追踪期间,并无案例发生局部复发或是远程转移。
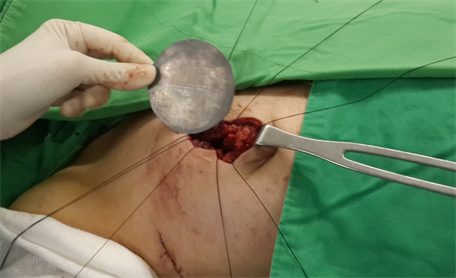
Figure 2. Placement of lead sheet into surgical cavity to protect internal organ
图2. 铅片置于手术腔或胸大肌下,保护肋骨及胸腔脏腑受到辐射线的照射

Figure 3. Connection of X-ray generator
图3. 放射线源与主机结合
IORT逐渐成为医师与病人的新选择,有几个原因:站在医师的角度,在肿瘤取出的手术空腔上,若是有显微下的癌细胞残留,在这些癌细胞尚未发生复制时,就予于放射线照射;相对于把空腔缝合后,等待伤口血肿吸收及表皮愈合三至四周再照射,对癌细胞的杀灭是更有效的。此外有研究显示,每延迟一个月的放射治疗,可能会增加1%的局部复发率 [8] 。另外一个优点是,手术中目测肿瘤的位置较为准确;相较于术中照射,病人原发肿瘤的位置未必是与手术疤痕完全相对应。此种不准确性被推测是由于病人术后照射的姿势与手术是平躺位置不同而产生的误差,误差率可达60~80% [9] [10] 。
5. 结论
IORT这种较新的单次手术中放射线治疗方式可以作为医生治疗早期且局部复发性较低风险的女性乳癌患者的多一种选择 [11] 。毕竟乳癌手术发展至今已经更加强调提供较符合病人期待的追求保留病患身体外观及功能,进而减少对精神心里层面产生负面影响的精准治疗方式。对于复发风险低的乳癌病患不失为一个有利的选择。
NOTES
*通讯作者。