1. 引言
一维纳米材料由于具有较大的长径比以及各向异性的特点,在光电子装置、传感器、能量存储与转换等领域有着广阔的应用前景。其中磁性金属纳米线材料因具有高比表面积及特殊的磁学性能,在垂直磁记录材料中将发挥巨大的作用,不但能提高磁存储的密度,同时也能够避免自退磁现象 [1] [2]。 钴作为重要的软磁材料,其纳米线具有与形貌相关的磁各向异性,成为近年来磁记录材料的研究热点。目前钴纳米线采用模板电沉积方法制备,多采用阳极氧化铝为模板,首先要设计制备氧化铝模板的孔道结构,在电沉积制备结束后,还要通过碱性溶液去除氧化铝模板,使制备过程繁琐复杂,耗时过长 [3] [4]。 因此,探索无模板的钴纳米线制备工艺可以节省时间,简化制备工艺,具有十分重要的工业意义。
离子液体指在室温或接近室温下呈现液态的、完全由阴阳离子所组成的盐,一般由有机阳离子和无机或有机阴离子构成,是一种环境友好的溶剂 [5]。 因其具有较好的化学稳定性与热稳定性,电化学窗口宽,并且可再生循环使用,对环境无污染的优点,近年来,各种类型的离子液体常被用于替代水溶液作为电沉积的电解质 [6] [7] ,各种金属或合金纳米线,如Al [8] ,Cu [9] ,SnCo [10] ,FeCoZn [11] 等可以通过在离子液体中采用无模板的电沉积方法制备。但是离子液体目前存在的较大问题就是对空气中的水分很敏感,不能在空气中使用,这也是离子液体电沉积没有广泛工业化应用的主要原因之一。基于前人的研究,本工作配制了CoCl2-EMIC离子液体,在不使用模板的情况下直接电沉积出钴纳米线,同时研究了CoCl2-EMIC离子液体在空气中对水的稳定性,探索在空气下电沉积纳米线的可行性。
2. 实验部分
2.1. 实验材料及试剂
纯度为99.7%以上的无水氯化钴(Alfa Aesar);氯化1-甲基-3-乙基咪唑(EMIC),纯度大于97% (ACROS);高纯钴,纯度大于99.5% (Aladdin);石墨棒由中钢集团上海新型石墨材料有限公司提供;高纯钨由宝鸡荣昌金属材料有限公司提供;硝酸、丙酮、乙腈等试剂均为分析纯。
2.2. 实验仪器
手套箱:型号SUPER(1220/450),MIKROUNA公司;恒温磁力搅拌器:型号ZNCL-T,上海巴玖实验有限公司;电子天平:CPA225D,SARTORIUS;电化学工作站:PAR2273,美国普林斯顿;烘箱:DHG–9070型干燥箱,上海一恒科技有限公司;扫描电镜/能谱仪:型号SEM(JSM-6360LV) EDS(Falcon),日本电子JEOL公司;X射线衍射仪:型号Rigaku D/mas2550X,日本理学公司(Rigaku);振动样品磁强计:型号Lakeshore7407,China Trend Limited。电解池、参比电极、工作电极和对电极为实验室自制。
2.3. CoCl2-EMIC离子液体的配制
由于无水氯化钴和EMIC都容易吸水,所以要在充满高纯氩气气氛的手套箱内保存,离子液体的配制也在手套箱内进行。按CoCl2与EMCI摩尔比为4:6进行配制,将称量好的EMIC放入电解池中,在恒温磁力搅拌器上搅拌,以0.5℃/min的速度加热到120℃,再向其中缓慢加入无水CoCl2,在120℃下保温2小时,最终形成蓝色的离子液体电解液。
2.4. 电沉积实验
电沉积采用传统三电极体系,加热120℃的条件下进行,以钨片作为基体,并引出直径为0.1 cm的钨丝作为工作电极(阴极),高纯钴片为辅助电极(阳极),自制的钴丝浸入摩尔比4:6的CoCl2-EMIC离子液体,并封存在底部有多孔玻璃砂芯的圆管中作为参比电极。参比电极长期保存在手套箱内,可多次使用。电沉积所用的钨丝和钨片先用颗粒度逐渐减小的砂纸打磨,去离子水清洗后放入2 M HNO3溶液中浸泡10~15分钟去除多余的氧化物,再用丙酮浸泡脱脂,烘干后备用。沉积结束后,钨片用先用乙腈清洗,再用丙酮清洗后干燥。
2.5. 表征方法
本文采用扫描电子显微镜对沉积物表面形貌进行分析,采用与扫描电镜联用的能谱仪对沉积物进行成分分析,采用透射电子显微镜观察沉积物的微观结构,利用振动样品磁强计测量磁滞回线。
3. 结果与讨论
3.1. 电化学分析
采用方波伏安法、计时电位法研究了Co在CoCl2-EMIC离子液体中的电化学行为,以确定电沉积具体实验条件。图1为Co2+离子在摩尔比4:6的CoCl2-EMIC电解液中(120℃)方波伏安曲线的拟合图,可以明显的看到,在−0.28 V处有一个很强的还原峰,对应着2价Co2+被还原的过程。采用计时电位法的测试曲线如图2所示,当采用较小的电流密度时,如−0.106 mA/cm2,电位曲线只出现一个平台,这是因为此过程中工作电极附近的Co2+被还原,电解液中的离子能及时扩散到电极附近参与还原反应,此时只有Co2+离子被还原。当电流密度逐渐增加至−0.954 mA/cm2时,电解液中的Co2+先迅速参与还原反应,而周围离子来不及扩散到电极附近,为了维持电流密度,工作电极附近的EMI+离子参与还原。所以在计时电流曲线上出现了两个平台,分别为−0.3 V对应于Co2+的还原和−1.3 V对应EMI+离子的还原。由图还可以看出,随着电流密度的增大,从第一个平台过渡到第二个平台的时间也在逐渐减小。

Figure 1. Square-wave voltammograms recorded on W electrode in CoCl2-EMIC ILs (mole ratio 4:6) at 120˚C
图1. 摩尔比为4:6的CoCl2-EMIC离子液体在钨电极上的方波伏安图(120℃)

Figure 2. Chronopotentiograms recorded at different current densities recorded on W electrode in CoCl2-EMIC ILs (mole ratio 4:6 at 120˚C)
图2. 摩尔比为4:6的CoCl2-EMIC离子液体在钨电极上不同电流密度下的计时电位曲线(120℃)
为了进一步研究摩尔比为4:6的离子液体CoCl2-EMIC中钴在钨电极上的成核过程,研究了三电极体系中不同过电位下的计时电流曲线。电压瞬态时的电流曲线表现出明显的形核过程:当电容电流开始衰减,测试电流逐渐达到最大值Im,对应的时间为tm;然后电流随着时间的延长开始下降,最终达到一个稳定值。当过电位增加时,最大电流也在增加,且电流迅速增加的时间缩短,说明诱导时间变短。Hills等 [12] 提出了两种极限情况下的成核模型,瞬时模型和连续模型,瞬时模型指在施加电压的瞬间,所有的成核点都被激活;而连续模型指在计时电流实验过程中,成核点逐渐被激活。这两种成核模型满足以下程
(瞬时模型) (1)
(连续模型) (2)
式中,I:电流密度,Im:最大电流密度,t:时间,tm:电流密度达到最大值Im时对应的时间。
为了辨别这两种成核过程,将即时电流曲线做拟合处理,令时间
,最大电流对应的时间
,令电流
,此时最大电流
,其中
为电流I随
呈线性的起始时间,
为其对应的电流。由
与
对应的无因次点以及利用等式1和2得到理论曲线组合成图3。从图中可以看出其无因次曲线更靠近瞬时成核的无因次曲线,表明金属钴在钨电极上电沉积初始过程遵循扩散控制瞬时成核和三维生长方式 [13]。

Figure 3. Non-dimensional
curves in CoCl2-EMIC ILs with mole ratio of 4:6 at 120˚C
图3. 摩尔比为4:6的CoCl2-EMIC离子液体的无因次
曲线(120℃)
3.2. 钴的电沉积和形貌分析
通过电化学分析结果可知,调节一定的电沉积条件,可以改变电解液中发生还原反应速率,并且影响钴形核成长的特性,从而引导特殊纳米结构的生成。经过优化离子液体组成、电沉积温度和沉积电位等条件,最终在120℃,−0.65 V的电位下沉积1200 s,获得形貌均匀的钴纳米线。图4(a)给出了钴纳米线的透射电子显微镜照片,可以看到钴纳米线的直径约为450 nm,长度约为5 µm,长径比约为9.4。图4(b)是上述钴纳米线的透射电镜能谱分析,结果表明纳米线中钴的纯度很高,少量的Cl元素来源于离子液体,W元素为基体钨片,而O元素的存在是由于纳米线表面钴在空气中氧化,形成CoO或表面吸附氧。图4(b)中的插图为钴纳米线的透射电镜电子衍射图谱,表明该纳米线为非晶结构。
3.3. 空气气氛中电沉积钴纳米线
按照离子液体对水的敏感性,可以分为亲水性和疏水性两种,本文使用的EMIC类离子液体已被证明是极易与水发生反应的。因而EMIC暴露在空气中很快会吸水变质,无法在直接在空气环境中使用,这很大程度上限制了离子液体的工业化推广。在实验过程中发现,摩尔比为4:6的CoCl2-EMIC离子液体制备完成并冷却至室温时呈固态,而且在空气中性质稳定,因此尝试了在空气条件下电沉积钴纳米线。将在手套箱中加热至120℃制备的离子液体分为两份,自然冷却成为固体后从手套箱中取出,分别在空气中放置48小时和96小时。再用这两份离子液体在空气中120℃温度下−0.65 V的电位沉积1200 s。图5给出了空气中电沉积得到钴纳米线的扫描透射电子显微镜照片,可以看到纳米线直径约为240 nm,与手套箱中沉积所得纳米线形貌相似。这一结果说明CoCl2-EMIC离子液体相比于EMIC更加稳定,适合于在空气中电沉积,这将大大促进其在工业领域中的应用。
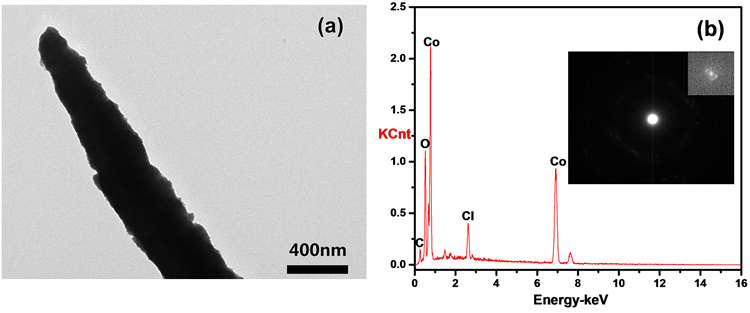
Figure 4. (a) Transmission electron microscopy images of Co nanowires, (b) Energy dispersive X-ray spectrometer and electron diffraction (inset) of Co nanowires (top right corner)
图4. (a) 钴纳米线的透射电子显微镜照片,(b) 钴纳米线的能谱分析,右上角插入图片为钴纳米线电子衍射图谱

Figure 5. SEM images of deposits obtained from CoCl2-EMIC ionic liquids saved in air for different time (a) 48 h; (b) 96 h
图5. 空气中保存不同时间后的CoCl2-EMIC离子液体电沉积得到钴纳米线SEM照片。(a) 空气中保存48小时;(b) 空气中保存96小时
3.4. 钴纳米线的磁性
将电沉积得到的钴纳米线经过清洗,采用振动样品磁强计对其平行与垂直方向进行磁性能测试,结果如图6磁滞回线所示。可以看到,钴纳米线平行于线米线方向剩磁比更大,易磁化轴的方向平行与纳米线的长轴方向,饱和磁化强度为0.026 emu。结果表明此方法制备的钴纳米线有一定的磁各向异性,但饱和磁化强度不高,剩磁比有一定差别,磁各向异性不明显,其原因可能是纳米线长径比不高,并且为非晶结构。

Figure 6. Hysteresis curve of Co nanowires CoCl2-EMIC, 900 s, 120˚C, −0.65 V 4:6 mol%
图6. Co纳米线磁滞曲线CoCl2-EMIC,900 s,120˚C,−0.65V 4:6 mol%
4. 结论
本文以摩尔比为4:6的CoCl2-EMIC离子液体电沉积制备得到钴纳米线,采用电化学分析方法研究了不同条件下沉积的可行性,并通过计时电流法探讨钴纳米线的成核机制。最终在−0.65 V,120℃的条件下沉积1200s,可以获得一定长径比的钴纳米线。并且,本文探索了在空气条件下CoCl2-EMIC离子液体的稳定性,证实空气条件下,离子液体中电沉积钴纳米线的可行性,电沉积得到的纳米线具有一定的磁各向异性。
NOTES
*通讯作者。