1. 引言
线纹海马(Hippocampus erectus)属刺鱼目(Gasterosteiformes)海龙亚目(Syngnathoidei)海龙科(Syngnathidae)海马属(Hippocampus),又名灰海马、直立海马,体侧具不规则或呈纹状的斑点及线纹 [1],是原产于美洲地区的一个海马品种。线纹海马最大全体长可达27 cm,寿命在3~4年左右,成体线纹海马适应温度在16℃~30℃,最适温度26℃,幼体海马的适应温度则在26℃左右。我国学者于2009年从美国引入此种,由于其生长速度快,抗病能力强以及成活率高等优势,相比国内传统养殖的大海马和三斑海马其更适合作为人工养殖的品种。在人工喂养环境下长到5公分只需3个月的时间,成长到8公分也仅需6个月的时间。当每立方水体100条以上的高密度养殖环境下,线斑海马的成活率仍能达到90%以上,而且线纹海马即使染病,多会在单体间发生,很少蔓延到整个海马群体,这在一定程度上可提高成活率 [2]。除此之外,只要5~6个月的时间其即可达到性成熟并且只要控制好温度、盐度等要素,线纹海马全年都可繁殖,在6~8个月的时间内就可达成体,所以线纹海马是可以在短时间内就将种群规模扩大并且全年都可稳定供应的商品海马。另外,在光线减弱时,线纹海马基本就停止进食进入休息状态不再活跃,线纹海马幼体出生期一般在阳光较为微弱的清晨,单次繁殖幼体海马在几十尾到几百尾之间,晚上也并不需要人员看护守夜,极大程度上减少了人工,这也是线纹海马之所以能成为海马养殖种首选的一大重要原因。线纹海马现如今主要销售渠道是药材厂,根据海马养殖场工作人员介绍,线纹海马干体现在在药材市场供不应求,往往几家海马养殖场所产出的成体海马干体都不够一家药材厂要收购的目标量。现如今很多养殖户看到了海马养殖的商机,但是繁殖后小海马从幼体到性成熟存活率在50%~60%之间,真正繁殖的一些技术也只掌握在大型养殖场手中,小型养殖户一般做不到繁殖这一项,只能通过购买5公分左右苗种来饲养,现在的苗种市场也是很大一个市场。线纹海马在性成熟之后,某些个体体色和花纹会随之而变化。一般的线纹海马体色发黑,但有的个体达到性成熟后体色会变为黄色或灰白色,体侧白色斑纹也会变得更加明显,这也使得线纹海马具有一定的观赏性(图1),加上它的适应能力强,也被很多水族馆和海水观赏生物的玩家作为展示观赏种海马。线纹海马在被作为观赏水族生物从养殖场出售时价格会偏高一点,但是观赏水族市场较小,需求量少,主要有几个原因:一是因为大部分海马属于保护物种,并且难饲养;二是现如今水族市场需求量少,海马养殖户宁愿卖给需求量大的药材厂;三是国内海水水族方面才兴起不久,海水水族市场有很大一部分的空缺,海水水族方面花费资金也多,很多人就会望而却步。所以未来在水族方面,随着人们生活水平的提高,海水水族玩家的增多,线纹海马甚至包括其它种的具有观赏性的海马会有很大的发展前景。
 (a)
(a)  (b)
(b)  (c)(a):体色黄色雄性线纹海马;(b):体色黄色雌性线纹海马;(c):正常体色雄性线纹海马
(c)(a):体色黄色雄性线纹海马;(b):体色黄色雌性线纹海马;(c):正常体色雄性线纹海马
Figure 1. Hippocampus erectus
图1. 线纹海马
海马是地球上唯一一种靠雄性生育后代的物种,雄性海马的尾部腹侧具有育儿囊,所以最简单区分海马雌雄的方法就是看尾部腹侧是否具有育儿囊,但此方法只适合性成熟后的海马,性成熟之前的海马的育儿囊只能通过解剖观察性腺来判断。在海马人工繁殖育种整个过程中,要实现幼体海马的雌雄个体分类养殖、保证性成熟后海马催产的合理性别分配、提高人工繁殖数量及选育成效等都需要对性别的准确鉴别 [3] [4]。近年来伴随着分子育种技术的升高,雌雄个体的鉴别也可通过分子遗传标记来准确区分 [5] [6] [7],此方法虽然准确率高,但所用资金较多,而且不方便,不易用于日常管理养殖,因此寻求更简便易行、实用有效的方法,将对线纹海马养殖业有着更重要的意义。为了减少对于资金、仪器和时间的需求,通过对大量的实验样本进行测量可量性状,分析标准化比例性状指标,并筛选出一定的特殊指标,利用这些指标建立一个性别鉴定方程,在日后鉴定工作中只需要测量相应的数据并带入性别判定方程即可。对于日本鳗鲡(Anguilla japonica),曾有人用此方法做过统计测量分析实验,得出的结果用于日本鳗鲡的雌雄鉴别发现其准确率可高达85%以上 [8]。本研究测量了线纹海马40尾雄鱼以及40尾雌鱼的5个可量性状,计算出5个标准化性状,通过对所得实验数据的分析和比较,找出雌雄个体形态方面的差异,从外形特征上为线纹海马幼体的性别鉴别提供一套可简便操作的判别方法,为今后线纹海马幼体的选育、分养过程中雌雄形态特征判别提供方法和后续单性育苗研究提供理论上的依据。
2. 材料与方法
2.1. 实验材料
试验用线纹海马取自文登南海海马养殖场(威海银泽生物科技股份有限公司),未进行实验前,试验选取海马均已达到性成熟,并作为种海马进行配对饲养于1 m × 1 m × 1 m的网箱内,每个网箱内饲养10对左右,控制水温在26℃~28℃,盐度28~30,水经过过滤棉、陶瓷环和蛋白分离器过滤以及紫外消毒灯杀毒。每天保证充足的光照、氧气和食物,每天换水5%~10%。每个网箱内只要有小海马出生,就需要人工捞出并计数。之所以使用网箱饲养主要有以下四个原因:第一,小网箱水体小,海马摄食方便,节约饲料;第二,小网箱可以保证海马种质的优良性,比如花纹,体色等观赏性性状;第三,海马属于比较懒的鱼类,只要找到附着物缠绕上就基本不会再游动,需要的活动范围和空间较小,所以只需要小空间就可以,这样就可以做到节约水体和空间;第四,小网箱养殖种马,当海马繁殖之后也便于收集和计数。小体积网箱养殖可以使养殖方式变为高密度集约化,网箱内饲养鱼种要求质量要高,而且管理人员的管理水平要高,要不时监测网箱内鱼种的状态,属于投入高,但产出也高的技术,是当前发展海马养殖业的一大非常有潜力和市场的养殖模式,而本试验的结果也可为这一新的养殖模式提供部分的基础数据参考。本实验从多个网箱内随机共捞取80尾性成熟后的线纹海马,其中雄性海马40尾,雌性海马40尾。实验所测线纹海马体长为8.20~15.45 cm,生长期基本相同,雌雄判别依靠育儿囊的有无来确定。
2.2. 数据测量
用刻度尺测量海马的可量性状,包括躯干长(trunk length, Tr L)、尾长(tail length, Ta L)、体宽(body width, BW)、头长(head length, HL)、吻长(snout length, SnL)五项指标(图2),精确到0.01 cm。由于海马是活体,而且身体通常是蜷曲着的,躯干长和尾长的测量需要将海马身体完全伸直,只用直尺肯定不方便测量,所以需要用细线来辅助测量,测量时用细线紧贴着海马的躯干或尾部并进行标记相应位点,最后再用直尺去测量细线相应的长度 [9] 即可得到海马的躯干长或尾长。而对于体宽则可用两脚规去辅助测量以达到减小误差,使实验数据和最后结果更加准确的目的。
2.3. 数据处理
实验采集线纹海马共计80尾,其中雄性海马为40尾,雌性海马为40尾。为消除因采集线纹海马的大小差异而产生的对实际测量参数数据的影响,将体长除以躯干部形态性状测量值、头长除以头部形态性状测量值,共计转化为5项标准化性状,包括体长/头长、体长/躯干长、体长/尾长、体长/体宽。通过采用Excel 365和SPSS25.0软件将这5项标准化性状取均值、主成分分析、R-聚类分析和逐步判别分析对线纹海马雌雄个体进行外观形态分析,筛选出雌雄海马之间具有显著差异的性状并依次建立线纹海马雌雄个体判别方程式。
3. 结果
3.1. 线纹海马的雌雄个体形态性状分析
试验共测定了80尾线纹海马的躯干长、尾长、头长、吻长、体宽这5项可量性状,其中包括雄性海马40尾,雌性海马40尾,所测得的线纹海马体长在9.20~15.45 cm之间。将测量所得的数据转化为5项标准化性状数据,计算这5项数据的均值及变异系数,结果见表1~表3。由表可得雌雄线纹海马之间头长:吻长之间的变异系数最大,为15.44%,其次是体长:体宽,其变异系数为11.46%,再其次是体长:尾长,变异系数为11.02%,体长:头长的变异系数较小,为9.78%,最小的为体长:躯干长,变异系数为6.59%。
 注:图中所示躯干长和尾长实际长度为伸直后的长度,实际测量值为拉伸后的测量长度(引自刘帅帅,2016)。体宽:背鳍处上端第一节体环从背部到腹部的长度。尾长:体侧最后一节体环的中央点到尾末端的距离。躯干长:从最后一个体环的中央点到匙骨环中央点的距离。头长:匙骨环中央点到吻端的距离。吻长:紧靠眼睛前方有一凸起,从此处到吻端的距离即为吻长。匙骨环:位于鳃盖正后方与胸鳍之间的骨环。
注:图中所示躯干长和尾长实际长度为伸直后的长度,实际测量值为拉伸后的测量长度(引自刘帅帅,2016)。体宽:背鳍处上端第一节体环从背部到腹部的长度。尾长:体侧最后一节体环的中央点到尾末端的距离。躯干长:从最后一个体环的中央点到匙骨环中央点的距离。头长:匙骨环中央点到吻端的距离。吻长:紧靠眼睛前方有一凸起,从此处到吻端的距离即为吻长。匙骨环:位于鳃盖正后方与胸鳍之间的骨环。
Figure 2. Characteristic sketch of hippocampus erectus
图2. 海马体型特征示意图

Table 1. Standardized traits of male Hippocampus erectus (Mean ± SD)
表1. 雄性线纹海马标准化性状(均值 ± 标准差)

Table 2. Standardized traits of female Hippocampus erectus (Mean ± SD)
表2. 雌性线纹海马标准化性状(均值 ± 标准差)

Table 3. Standardized traits of male and female Hippocampus erectus (Mean ± SD)
表3. 雌雄线纹海马标准化性状(均值 ± 标准差)
3.2. 主成分分析
对线纹海马的5项标准化性状进行主成分分析,筛选出前三个贡献率以及各指标在这三个主成分上的负荷量,分析结果见表4。由于前三个主成分累积贡献率达87.127%,所以可舍掉其余主成分。
从表4可以看出,主成分1、2和3的贡献率分别为42.355%、23.646%、21.127%,其中主成分Ⅰ的贡献率最大,主成分Ⅰ负荷量较大的主要是体长:尾长,反映的主要是尾部特征,主成分Ⅱ负荷量较大的主要是体长:头长、体长:体宽2个性状,反映的主要是体型特征,主成分Ⅲ负荷量较大的主要是头长:吻长,反映的是头部特征。

Table 4. Contribution rate of the first three principal components and load quantity of indicators
表4. 前三个主成分的贡献率和各指标的负荷量
3.3. R-聚类分析
由图3分析可知,这5项标准化形态指标可分为两大类,第I类为体长:尾长、体长:躯干长、头长:吻长,反映的是体型及头部的特征参数,第II类为体长:体宽、体长:头长,反映的是体型的特征参数。
R-聚类分析所得出的第I类标准化性状与主成分分析得出的第I、III主成分的组分相对应,反映的是线纹海马体型及头部的特征,第II类标准化性状与第II主成分的组分相对应,反映的是线纹海马的体型特征。两者对比所得出的结果大体一致。

Figure 3. R-Cluster analysis map of standardized morphological indicators of Hippocampus erectus
图3. 线纹海马标准化形态指标R-聚类分析图
3.4. 雌雄线纹海马判别分析
对测量的80尾线纹海马个体的5项标准化性状进行逐步判别分析,根据各个变量对模型的贡献大小,逐步去剔除不相关的变量,最终筛选出3个变量体长:体宽(X1)、体长:尾长(X2)、体长:头长(X3),这三个指标分别反映了雌雄线纹海马在尾部(X2)和身体形态(X1、X3)方面的差异,所建立的判别模型方程为
雄:F1 = 12.508X1 + 227.692X2 + 24.502X3 − 270.108
雌:F2 = 15.194X1 + 247.685X2 + 20.868X3 − 300.656
通过对判别函数的显著性检验显示,P < 0.01,这表明判别函数达到了极显著水平。通过计算,得到每尾线纹海马个体的判别分数值,得到频布图。由图4、图5可看出,所建立的该判别模型可用于区分线纹海马的性别。
利用所建立的判别模型方程,对测量的80尾线纹海马个体进行性别判别。将每尾个体的三个性状参数值带入判别模式方程中,分别计算F1、F2。若F1 > F2,则判定为雄性线纹海马,反之则判定为雌性线纹海马。判定结果见表5,结果显示,雄性线纹海马判别准确率为87.5%,雌性线纹海马判别准确率为85.0%,综合判别准确率为86.25%,在80尾线纹海马中仅有11尾被误判为其它性别。

Figure 4. Frequency distributions of discriminant scores obtained from male Hippocampus erectus
图4. 线纹海马雄性个体判别分数的频步图
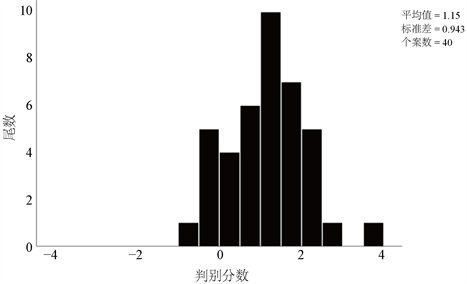
Figure 5. Frequency distributions of discriminant scores obtained from female Hippocampus erectus
图5. 线纹海马雌性个体判别分数的频步图

Table 5. The results of sexual discriminant of Hippocampus erectus
表5. 线纹海马雌雄判别验证结果
对筛选出的用于建立性别判定函数的三个性状进行t检验(表6),结果显示体长:体宽、体长:尾长、体长:头长的差异极显著(P < 0.01)。以上数据表明,雄性的体宽、尾长相较于雌性更宽、更长,而雄性的头长相较于雌性则更短。
4. 讨论
4.1. 多元统计分析在雌雄个体差异分析上的应用
随着科学技术的进步、计算机技术的不断成熟以及各类统计软件的开发完善,多元统计分析在水产统计分析领域应用越来越广泛。主成分分析是在较少的损失或是不损失原有信息基础上,将测得的多个实际变量简化成几个较少的变量,能更好的去反映事物本质的一种分析方法。聚类分析和判别分析是两类研究事物分类的基本方法,但是聚类分析是一种由事物本身的特性再研究个体分类的方法,而判别分析是要根据先求的判别函数再去对所属类别不明的事物进行分类的一类分析方法 [10]。许多鱼类在雌雄个体间存在着或多或少的差异,这些差异包括有生长率、体型、丰满度、体色、性腺成熟时间等生物学性状。近年来,越来越多的学者将多元统计分析应用于水生动物的雌雄个体外观形态差异上的分析。安丽等 [11] 对67尾翘嘴红鮊(Erythroculter ilishaeformis)的10项标准化比例性状进行主成分分析、R-聚类分析,并且建立了雌雄判别公式,对翘嘴红鮊的雌雄判别提供了一定的依据。岳亮等 [12] 采用主成分分析、逐步判别分析和t检验的方法对红鳍东方鲀(Takifugu rubripes) 雌雄个体的形态差异进行了分析研究,研究结果表明红旗东方鲀雌雄之间形态方面存在着较明显的差异,雄性的体型和体周长要比雌性的更宽,更长。

Table 6. T-test for traits of Hippocampus erectus in equation
表6. 线纹海马性状的t检验及雌雄形态差异
4.2. 雌雄个体差异分析
鱼类的形态学特征会受到遗传因子和环境因子的共同作用影响 [13],但在本实验中,所有样本均在同一环境中长大,环境因素对其形态学特征影响较小,由于其亲本不确定,所以无法排除遗传因子对其形态学特征的影响,不过此影响对形态学特征比例影响较小,可忽略此因素影响。
对于鱼类的雌雄鉴别是鱼类生物学研究的一大重要内容,也是诸多保护性珍稀鱼类的人工繁养殖、增殖的关键技术之一。通过对某些鱼类的外部特征测量及多元统计分析,可找到一些典型的外形特征以来鉴别鱼类雌雄个体的方法,这类技术已经在一些由于性腺发育而造成身体外部形态特征有不同程度改变的两性异形硬骨鱼类中得到应用 [14]。
本研究测量了80尾线纹海马的5项可量性状,并计算得出了5项标准化性状。通过对这5项标准化性状进行多元统计分析,得到了三个主成分,三个主成分贡献率达到了87.127%,三个主成分分别代表了线纹海马尾部特征、体型特征、头部特征,通过这些指标的测定及分析基本可以反映出线纹海马的外部形态。聚类分析中,第I类标准化性状与主成分分析得出的第I、III主成分的组分相对应,反映的是线纹海马体型及头部的特征,第II类标准化性状与第II主成分的组分相对应,反映的是线纹海马的体型特征,两者对比所得出的结果大体一致。运用逐步判别法,最终筛选出三个标准化性状分别是体长:尾长、体长:体宽、体长:头长,以这三个标准化性状为变量建立线纹海马雌雄判别方程式,综合判别准确率达86.25%,这说明判别方程具有一定的鉴别效果,利用线纹海马的一部分外形形态数据建立雌雄判别方程对线纹海马的雌雄快速判别具有一定可行性。本研究测量样本均为人工养殖的线纹海马,其与野生群体的生长环境以及摄食模式等有着较大的差别,因此野生群体和人工养殖群体可能存在一定的差别,需要进一步研究比较。
5. 结论
线纹海马在幼体阶段育儿囊未发育成熟,因此很难辨别雌雄,只能通过解剖观察性腺得知性别,而此方法在实际应用中根本不实际,通过本次实验,我们得出,只需测量线纹海马的某些外观指标,套入雌雄判别公式,即可得知海马的雌雄性别,较为方便简单,但是仍会存在误判的结果。但是此方法对于线纹海马幼体时期雌雄分养殖、养殖场出苗时雌雄分类等有一定的借鉴作用。
基金项目
青岛水族技术协同创新中心合作项目(6602418043);青岛市市南区应用基础研究计划项目(2018-4-011-ZH)。
NOTES
*通讯作者。