1. 临床资料
朱某,女,23岁,因“停经34周 + 2,心慌一天”于2021-07-22入院收住产科。现病史:2021-06-18于当地医院产检时行心电图检查发现房性心动过速,心率最高达160~170次/分,06-19行超声心动图,自诉结果无明显异常(未见报告),孕妇无明显自觉症状,遂未予进一步检查。半月前孕妇无明显诱因出现阵发性干咳,持续至今;偶有胸闷气喘,休息后好转,病程中无咳痰,无畏寒发热,无头晕头痛,无视物模糊,无端坐呼吸。一周前自觉下肢偶有轻度水肿,休息后好转。一天前自觉心慌心悸,伴气急,无胸痛胸闷,无明显呼吸困难,遂至我院就诊,行心电图:1) 阵发性室上性心动过速;2) 左前分支阻滞;3) 完全性右束支阻滞(室内差异性传导、差传蝉联不除外,请结合临床) (图1)。急诊心电监护示心率160~170次/分,床边心脏彩超示:左室射血分数36%,二尖瓣、三尖瓣轻–中度反流,轻度肺动脉高压。心内科予食道调搏后心率仍高达160~170次/分。急诊拟“妊娠合并心功能不全;心律失常”收住入院。病程中无头痛、头昏、眼花,无咳痰,无畏寒发热,无头晕头痛,无视物模糊,无端坐呼吸,无明显腹痛,无阴道流血流水,自觉胎动正常,入院治疗。既往史:平素体健。生育史:0-0-0-0。家族史:无特殊病史可询。体格检查:T 36.5℃,P 178次/分,R 35次/分,BP 135/93 mmHg。神志清楚,精神正常,发育正常,营养中等,查体合作。全身皮肤粘膜无黄染,无淤斑,浅表淋巴结未扪及肿大。头颅无畸形,结膜无充血,巩膜无黄染,双瞳孔等大等圆,对光反射灵敏;咽不红,双侧扁桃体无肿大。颈软,气管居中,甲状腺无肿大,锁骨上未扪及淋巴结肿大。胸廓对称。双肺呼吸音清,未闻及干湿性啰音,心界不扩大,心律齐,无病理性杂音。腹隆如孕月大小,可扪及胎体胎肢,闻及胎心,脊柱生理弯曲存在,四肢关节活动好,未见畸形,肛门外生殖器未见异常。生理反射存在,病理反射未引出。产科检查:宫高33 cm,腹围118 cm,胎方位LOA位,胎心145次/分,先露头,未衔接。阴道指检:宫颈质地中等,颈管未消,宫口未开,胎膜未破,先露-2,骨盆外测量25-28-20-9 cm。辅助检查:产科B超(2021-07-22 )单胎,头位,存活;双顶径(BPD):92 mm,耻上探及;股骨(FL):70 mm;胎盘(PL):宫左侧壁,III˚-;羊水:45 mm;脊柱:连续,胎心律规则。脐带血流S/D:2.5。因体位关系,颜面部显示不清。心电图(2021-07-22) (图1):1) 阵发性室上性心动过速;2) 左前分支阻滞;3) 完全性右束支阻滞(室内差异性传导、差传蝉联不除外,请结合临床)。床边超声心动图示(2021-07-22):左室射血分数36%,二尖瓣、三尖瓣轻–中度反流,轻度肺动脉高压。
入院初步诊断为:1) 单胎G1P0孕34周 + 2待产LOA;2) 妊娠合并心功能不全(围生期心肌病?);3) 心律失常。
2. 治疗经过
入院后给予患者吸氧、心电监护等治疗,与患者及家属沟通病情后于07-22行紧急剖宫产术(子宫下段横切口),术后转至重症医学科诊治,予以重症监护,高流量吸氧,同时完善相关检查,N末端B型钠尿肽原(N-terminal B-type brain natriuretic peptide, NT-proBNP) 2940.00 pg/ml;血气分析:PO2 128.4,PCO2 27.9 mmHg,Glu 6.2 mmol/L,Lac 2.2 mmol/L;肝肾功能:天门冬氨酸氨基转移酶54.00U/L,尿酸(GHX) 753.70 umol/L;血常规:白细胞17.96*10^9/L,中性粒细胞百分比95.4%,中性粒细胞17.13*10^9/L;心肌损伤标记物:肌钙蛋白I测定0.086 ng/ml,肌酸激酶同工酶3.26 ng/ml,肌红蛋白185.70 ng/ml;心电图:1) 窦性心动过速,2) ST-T改变。密切监测患者的心功能,定时复查心肌损伤标志物,床边心电图。予以头孢呋辛钠抗炎及促进子宫复旧,适当补液,严格限制液体速度,病情稳定后转回产科进一步治疗。
患者于07-24出现胸闷、气喘,血氧饱和度下降,行床边超声心动图提示:左室射血分数59%,肺动脉压31 mmHg。考虑急性左心衰,予20 mg速尿静推,0.4 mg西地兰缓慢静推,并同时予行床边心电图、完善血常规、凝血常规、D-二聚体、NT-proBNP、肝肾功能电解质等相关检查,抢救结束后患者症状稍缓解,予地高辛、倍他乐克、呋塞米、螺内酯抗心衰治疗,严格限制其入量及速度。复查NT-proBNP 5200.00 pg/ml。电解质:氯108.20 mmol/L;钾4.23 mmol/L。床边心电图:1) 窦性心律,2) 电轴右偏,3) ST-T改变,提示心肌缺血。患者症状逐渐好转,继续予心电监测。
7-25患者心率达160~170次/分,立即予口服倍他乐克降心率,复查床边心电图(图2),提示:1) 窦性心律(60~70次/分),2) 电轴右偏,3) ST-T改变,提示心肌缺血。行床边超声心动图提示:心功能减退,主动脉瓣、二尖瓣、三尖瓣轻度返流,射血分数46%。复查电解质:钾2.0 mmol/L,提示低钾血症,停用地高辛,继续予以口服倍他乐克降心率、补充电解质、纠酸等治疗维持内环境平衡。07-25 22:03患者诉心悸,无其他明显不适,心电监测提示:心率160次/分,呼吸32次/分,血压122/74 mmhg,血氧饱和度98%,予以口服倍他乐克12.5 mg,暂不用地高辛。患者口服倍他乐克后心率逐渐下降。22:55患者无心悸,呼吸平稳,稍有心前区不适,立即行心电图(图3)提示1) 窦性心动偏缓,2) T波改变,3) 不完
 阵发性室上性心动过速;左前分支阻滞;完全性右束支阻滞;(室内差异性传导、差传蝉联不除外)
阵发性室上性心动过速;左前分支阻滞;完全性右束支阻滞;(室内差异性传导、差传蝉联不除外)
Figure 1. ECG at admission
图1. 入院时心电图
 窦性心律;电轴右偏;ST-T改变,提示心肌缺血
窦性心律;电轴右偏;ST-T改变,提示心肌缺血
Figure 2. ECG on the morning of the onset of Adams-stokes syndrome
图2. 阿斯综合征发作当天上午心电图
 窦性心动偏缓;T波改变;不完全性房内传导阻滞
窦性心动偏缓;T波改变;不完全性房内传导阻滞
Figure 3. ECG on the night of onset of Adams-stokes syndrome
图3. 阿斯综合征发作当晚心电图
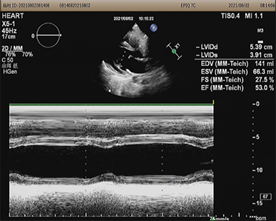 (a) 左室射血分数53%
(a) 左室射血分数53% 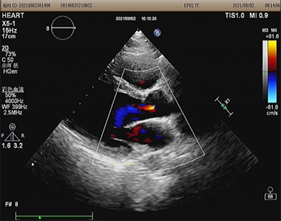 (b) 主动脉瓣、二尖瓣、三尖瓣轻度反流
(b) 主动脉瓣、二尖瓣、三尖瓣轻度反流
Figure 4. 08-02 review of echocardiography
图4. 08-02复查超声心动图
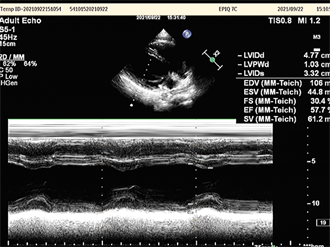 左室射血分数57.7%
左室射血分数57.7%
Figure 5. 09-22 review of echocardiography
图5. 09-22复查超声心动图
全性房内传导阻滞。暂无特殊处理,建议患者注意休息,继续严密观察。23:28患者突发面色青紫,牙关紧闭,口吐白沫,四肢抽搐,神志不清,端坐呼吸,测心率155次/分,呼吸35次/分,血压122/71 mmHg,血氧饱和度80%。手搭颈动脉未扪及脉搏,考虑阿斯综合征(Adams-stokes syndrome),立即予以电除颤(200焦,非同步)共三次、气管插管、心肺复苏等抢救后患者恢复窦性心律。再次转入重症医学科诊治,予以抗感染、利尿、控制血压、抗凝、抗心衰、甘露醇脱水降颅压、尼莫同缓解脑血管痉挛,亚低温脑保护,纠正内环境紊乱等对症治疗,动态脑电图监测,预防癫痫,控制体温等治疗,患者神志转清,心率、血压平稳后转心内科继续诊治。08-02复查超声心动图(图4):主动脉瓣、二尖瓣、三尖瓣轻度反流。左室射血分数53%,患者心脏功能较入院前好转,08-04出院。出院后一月门诊复查超声心动图(图5):左室射血分数57.7%。随访3个月患者无不适,病情平稳,工作、生活均正常。
最后诊断:1) 围生期心肌病,妊娠合并心功能不全,心功能IV级(NYHA分级);2) 室性心动过速,房性心动过速;3) 心源性休克;4) 呼吸心跳骤停(心肺复苏术后);5) 低钾血症;6) 单胎活产孕34周 + 2已产LOA。
3. 讨论
妊娠合并心脏疾病是导致孕产妇死亡的前三位死因之一 [1],既往一项大型研究结果显示,妊娠相关心肌病的发病率为50/100,000,其中围产期心肌病(peripartum cardiomyopathy, PPCM)占50% [2],虽然PPCM的发病率低但是致死率高,严重危害孕产妇健康,甚至危及母婴生命。因此及早发现、诊断PPCM,并进行积极治疗,对改善患者预后有非常重要的意义。
传统上围生期心肌病(PPCM)被定义为妊娠最后1个月、分娩期间或产后前6个月发生的心衰,可在数小时内迅速出现或在几周或几个月后缓慢进展 [3]。但临床上部分妊娠相关心肌病病例也完全符合PPCM的特点,只是发病时间更早或更迟一些,所以2019年欧洲心脏病学会(ESC)更新后的专家共识把PPCM的时间放宽,PPCM最新定义为发生在妊娠末期或分娩后数月的一种表现为心衰的特发性心肌病,其突出特点是左心室收缩功能下降,左心室射血分数(LVEF) < 45%。左心室多有扩大,但部分患者也可以不扩大。部分LVEF超过45%的患者,如有明确的心功能受损和典型PPCM表现,有时也需诊断为PPCM。诊断PPCM必须排除其他原因导致的心衰 [4]。大多PPCM患者发病时表现为呼吸困难、心悸、咳嗽、咯血、水肿、端坐呼吸及夜间阵发性呼吸困难等心衰症状,少数患者发病即为血栓栓塞性并发症、恶性心律失常甚至心源性猝死。因其临床表现和起病方式复杂且多样性的特点,常易漏诊或误诊。
目前主要危险因素有多胎多产、家族史、种族(非洲裔妇女高发)、吸烟、糖尿病、高血压、子痫前期、营养不良、母亲年龄、长时间使用β受体兴奋剂类的保胎药等。
在辅助检查方面,超声心动图检查是诊断PPCM的关键,超声心动图测量的LVEF下降和肺动脉高压均是PPCM患者重要的预后指标 [5]。所有怀疑PPCM的患者均应行心电图检查,心电图虽然对PPCM的诊断没有特异性,但有助于鉴别肺栓塞、心肌炎、急性心肌梗死等其他疾病。PPCM患者尤其是急性发病患者B型利钠肽(B-type natriuretic peptide, BNP)和(或)NT-proBNP明显升高 [6],BNP/NT-proBNP的升高程度及其对治疗的反应与临床预后密切正相关 [7]。
再回顾病程,患者入院时心律不齐,伴有心慌心悸等不适,入院前已经表现出心功能衰竭的症状,急诊行剖宫产术后一定程度上减轻了心脏负荷,但分娩后妊娠子宫下腔静脉压迫解除,子宫收缩引起自体输血,产妇体液动员和吸收都增加了静脉回流使得产妇回心血量增多,增加了产后液体超负荷和肺水肿的风险,产后72小时内易出现心衰症状。本例病例中入院时超声心动图就已经提示左心室射血分数只有36%,后反复几次查超声心动图显示左心室射血分数 < 45%、NT-proBNP明显升高,根据ESC诊断标准[3]围生期心肌病诊断依据充分。术后严格限制其液体入量及速度,但患者分娩后第二天出现急性左心衰症状,予加用地高辛、倍他乐克、呋塞米、螺内酯等抗心衰治疗后好转,后复查电解质提示低钾血症,予以适当补钾,但患者07-25夜间出现了恶性心律失常导致阿斯综合征发作进行抢救。通过对患者病程的分析,笔者认为该患者阿斯综合征发作的主要诱因是应用利尿剂导致了低钾血症,低钾血症会使心肌细胞兴奋性和自律性增强而出现室早、室速、室颤等心律不齐。同时病程中为降低心率、抗心衰还使用了倍他乐克对症治疗,曾有文献报道过倍他乐克导致阿斯综合征发作的病例 [8]。倍他乐克是一种选择性β1肾上腺素能受体阻滞剂,可发挥负性变时、负性变力及负性传导的作用,有效地对肾素/血管紧张素/醛固酮(RAAS)系统及交感/肾上腺髓质系统的活性进行拮抗而使心率减慢,实现稳定心室率、抗心律失常的目的,但也因为使心脏传导系统不应期显著延长,房室结区受到阻滞导致传导障碍,出现窦性心动过缓、房室传导阻滞等副作用。在低钾血症和倍他乐克的副作用的共同作用下导致了该患者阿斯综合征的发生。
2016年妊娠合并心脏病的诊治专家共识中指出,对于妊娠合并心脏病患者发生恶性心律失常的处理原则首先要针对发生诱因、类型、血流动力学变化对母儿的影响、孕周综合决定尽早终止心律失常的方式,防止其他并发症,病情缓解或稳定后再决定其长期治疗的策略 [9]。
在PPCM的诊治上首先要提高识别能力,因缺乏特异性的治疗手段,目前对PPCM的治疗主要还是从缓解心衰症状及抑制心肌重构等方面入手。但因目前无大量临床研究,围生期使用抗心衰药物必须权衡治疗获益与潜在的毒副作用。笔者从本病例的教训中认识到危重的PPCM患者在使用呋塞米等利尿剂及倍他乐克等抗心律失常药时,更应密切监护心电图及电解质水平,一旦出现窦性心动过缓、房室传导阻滞应及时停药,避免发生恶性心律失常而危及孕产妇甚至母儿生命安全。目前认为PPCM痊愈为LVEF恢复到≥50%即为心功能恢复正常,心功能恢复正常多在发病后一个月内开始,一般在6个月内完全恢复正常,但超过6个月者仍有可能恢复,最长者可达2年 [10]。由于该患者合并阿斯综合征发作,呼吸心跳骤停,及时抢救并针对性进行了一系列治疗措施预防缺氧缺血性脑病的发生和抑制心肌重构、抗心衰,从目前看来该患者预后良好,但根据既往研究发现产妇心血管事件发生和死亡风险在产后至少持续数周,且临床上对于PPCM合并阿斯综合征发作的病例报道较少,对于这一类患者的长期预后是否良好还需要进行长时间定期随访。综上所述,尽早发现、诊断PPCM并及时治疗对PPCM患者的预后有着十分重要的意义,及早判断和识别可能导致恶性心律失常及心源性猝死的诱因,积极采取干预措施,避免发生围生期孕产妇心血管不良事件发生。