摘要: 目的:系统性归纳不同干预措施治疗女性型脱发的有效性和安全性,确定两者兼顾的治疗方案及机制。方法:计算机检索PubMed、The Cochrane Library、Web of Science、EMbase、CNKI、WanFang Data、CBM、VIP数据库,搜集不同干预措施治疗女性型脱发的随机对照试验,语种限定为中文和英文,检索时限均为2000年1月1日至2022年07月20日,包括单一和联合治疗,除外中药治疗和动植物组织提取物等相关治疗。由2位评价员独立筛选文献、提取资料并评价纳入研究的偏倚风险后,采用StataMP 17中的network及mvmeta软件包进行数据处理。结局指标为头发数量相对于基线的平均变化,因其为连续型变量,故采用均数差及95%可信区间(confidence interval, CI)作为统计分析的效应量,当P < 0.05时认为差异有统计学意义。结果:经严格文献筛选后共纳入14个研究,涉及外用不同浓度的米诺地尔、口服米诺地尔、低能量激光、口服避孕药及多组联合疗法共计11种干预措施。Meta分析结果显示,低能量激光治疗增加头发计数的效果优于其余10种干预措施(P = 0.05);在不良反应方面,外用1%米诺地尔的耐受性最好,其余干预措施因不良反应退出实验的可能性没有差别(P = 0.05)。结论:低能量激光是改善女性型脱发患者毛发数量最好的干预措施,且耐受性较好,不良反应少。综合而言,低能量激光可能是治疗女性型较为脱发最理想的干预措施。受纳入研究数量和质量限制,上述结论尚需开展更多高质量研究予以验证。
Abstract:
AIM: To systematically summarize the effectiveness and safety of different interventions in the treatment of female pattern alopecia, and determine the optimal treatment plan and mechanism. METHODS: A computer search of PubMed, The Cochrane Library, Web of Science, EMbase, CNKI, WanFang Data, CBM, and VIP databases was conducted to collect randomized controlled trials of different interventions for the treatment of female pattern alopecia in Chinese and English. The search period was from January 1, 2000 to July 20, 2022, and included both single and combination treatments, except for herbal treatments and plant and animal tissue extracts. Data were processed using the network and mvmeta packages in StataMP 17 after independent screening of the litera-ture by 2 evaluators, extraction of information, and evaluation of the risk of bias of the included studies. The ending indicator was the mean change in hair count relative to baseline, which is a con-tinuous variable, so the mean difference and 95% confidence interval (CI) were used as effect sizes for statistical analysis, and differences were considered statistically significant when P < 0.05. RESULTS: A total of 14 studies involving different concentrations of topical minoxidil, oral minoxidil, Low-Level Laser Therapy, oral contraceptives and combinations of therapies between them were in-cluded after rigorous literature screening. meta-analysis showed that Low-Level Laser Therapy in-creased hair count better than the remaining 10 interventions (P = 0.05); in terms of adverse ef-fects, topical minoxidil 1% Minoxidil was the best tolerated, and the remaining interventions did not differ in the likelihood of withdrawal from the trial due to adverse effects (P = 0.05). CONCLUSION: The available evidence suggests that Low-Level Laser Therapy is the best intervention for increasing hair count in female pattern baldness and is well tolerated. Taken together, Low-Level Laser Therapy may be the ideal intervention for the treatment of more female-pattern alopecia. Due to the number and quality of included studies, the above findings need to be validated by additional high-quality studies.
1. 引言
毛发是往往是一个人个性的非语言表达,缓慢、持续、进展地脱发会给人们带来强烈的负面情绪,甚至影响到生活质量,这对于女性来说更是如此,故女性的脱发情况越来越受到关注。导致女性脱发的原因很多,如女性型脱发(female pattern hair loss, FPHL)、斑秃、瘢痕性脱发、休止期脱发、妊娠导致脱发以及药物导致脱发等,其中FPHL是女性脱发的主要原因。曾经认为女性型脱发是雄激素性脱发(androgenetic alopecia, AGA)中女性患者的表现形式,称之为女性雄激素性脱发,但尽管男女两型脱发的毛囊改变相似,均表现为毛囊微小化,但其临床表现和对抗雄激素治疗的反应存在显著差异,同时雄激素在女性型脱发中的致病作用尚未完全阐明,故FPHL的命名比女性雄激素性脱发更合适 [1]。FPHL目前的主要治疗措施包括口服抗雄激素药物、外用米诺地尔、低能量激光等,但各种治疗的效果存在差异,其中外用米诺地尔目前被认为是有效的,也是临床医生为脱发患者首选的治疗方案,低能量激光的选择因治疗费用较贵,并不为首先,但很多研究证明其对脱发有较好的治疗效果 [2] [3] [4] [5]。抗雄激素性药物主要有非那雄胺、醋酸环丙孕酮,此外螺内酯也具有抗雄激素作用,但效果不确切。因存在多种治疗方式,且效果各异,有时甚至无效,因此选择合适的治疗方案至关重要。但各种治疗的效果存在差异,甚至可能无效,因此选择合适的治疗方案至关重要。网状Meta分析基于临床研究的直接和间接证据,对涉及的干预措施疗效进行综合评价,可为临床治疗决策提供最优的证据 [6]。因此,本研究采用网状Meta分析的方法对不同干预措施改善女性型脱发的发量的有效性和安全性进行系统评价,旨在为临床实践提供参考。
2. 资料与方法
2.1. 文献纳入标准
1) 研究类型:比较不同干预措施治疗FPHL的随机对照试验(Randomized controlled trials, RCT),语种限定为中文和英文。
2) 研究对象:纳入的研究对象为FPHL的患者,无论病变的大小、侵袭性和既往治疗史如何,其年龄、性别、病程以及病例来源均不限定。
3) 干预措施:针对女性脱发的各种治疗方式,联合治疗及单一治疗均包括在内,中药治疗、动植物提取物等干预措施暂不包括在内。
4) 结局指标:主要结局指标是头发数量相对于基线的平均变化(以每平方厘米的头发为单位),对变异性的测量是标准偏差(±SD),次要指标是因为不良反应而脱落的病例数。
2.2. 文献排除标准
1) 重复发表的文献;
2) 摘要信息不全、未提供原始数据的文献。
2.3. 文献检索
计算机检索英文数据库(PubMed, The Cochrane Library, Embase, Web of science)和中文数据库[万方数据(WanFang Data),中国知网(CNKI),中国生物医学文献数据库(CBM),维普(VIP)]。检索时间为2000年1月1日至2022年07月20日。关键词包括:female pattern hair loss、female pattern alopecia、Female Pattern Baldness、Baldness、Female Pattern、therapy、randomized controlled trial(s)、controlled clinical trial(s)、女性型脱发、女性脱发、雄激素性脱发、随机对照试验、对照临床实验、临床研究、随机分配、临床试验等。以PubMed为例,其具体检索策略见图1。
2.4. 文献筛选及质量评价
检索上述数据库后,用Endnote20软件对所得文献进行剔重,由两名研究员独立阅读题目和摘要,对所有文献进行归纳整理并标注纳入及排除原因。初筛完成后,将所得文献进行全文阅读并标注纳入及排除原因,保留通过复筛的文献即为纳入文献。
采用Cochrane协作网偏倚风险工具(Cochrane Collaboration’s tool for assessing the risk of bias in randomized trials, RoB)对RCT研究进行评估。Cochrane偏倚风险工具评价维度包括随机序列生成、分配序列隐藏、参与者和工作人员的盲法、结果的盲法、不完整结果数据及其他偏倚来源。该步骤由两人独立完成,结果不一致时进行协商,无法统一时由第三人进行判断。
2.5. 文献资料提取
由两名研究员仔细阅读全文,对文献中研究对象信息进行提取,提取信息包括研究员,发表年份,每组样本量,年龄范围,疗程,观察指标。并将结果进行交叉核对,意见不统一时二人协商确保信息正确,或由第三人提出解决方案。
2.6. 统计方法
本研究采用基于贝叶斯框架实现网状meta分析。本研究主要提取治疗前后头发计数变化量的均值 ±标准差(X ± SD),当未报告SD时,通过95%置信区间(confidence interval, CI)或范围区间或标准误(standard error, SE)来间接获取。使用StataMP 17中的network及mvmeta软件包以及进行数据处理。结局指标为连续型变量,故采用均数差及95%可信区间(confidence interval, CI)作为统计分析的效应量,当P < 0.05时认为差异有统计学意义。存在闭合环时分别拟合不一致性模型和一致性模型,并采用节点劈裂法(node-splitting method)进行局部不一致性检验。设定P > 0.05为不存在不一致性,采用一致性模型进行分析;P < 0.05为存在不一致性,采用不一致性模型分析,并分析不一致性来源。使用StataMP 17绘制网状关系图、森林图、累积概率图、累积排序概率图下面积图(surface under the cumulative ranking, SUCRA)、联赛图及漏斗图等(SUCRA值的范围为从0到1)。
3. 结果
3.1. 文献检索结果
各数据库去重初筛获得相关文献497篇,经严格遵循纳入排除标准筛查后,最终纳入14个RCT [7] - [20],FPHL患者共计2045例,涉及11种治疗方式。流程见图2。
3.2. 纳入文献基本特征
各研究均报告各干预组间性别、年龄等基线齐,具有可比性。其中三臂试验1个 [9],其余均为两臂试验。各组样本量介于18~123例之间,共涉及不同浓度的米诺地尔外用、米诺地尔口服、低能量激光、口服避孕药及其之间组合疗法共计11种。疗程均在为17~48周之间。纳入文献的基本信息见表1。
3.3. 纳入研究的方法质量学评价
根据Cochrane偏倚风险评价,所有RCTs均提及随机化,其中有1个RCTs [9] 描述通过的“计算机随机”或“随机数字表法”产生随机序列。2个RCTs [10] 描述了分配隐藏方法,4个RCTs [9] [10] [12] [16] 记录并实施了盲法,2个RCTs [8] [9] 记录了脱落及处理。偏倚风险图见图3。

Figure 2. Literature screening process and results
图2. 文献筛选流程及结果

Table 1. Basic information of the included studies
表1. 纳入研究的基本信息
*三臂实验;A/B代表组别;OM代表口服米诺地尔;OF代表口服非那雄胺;OCA代表口服醋酸环丙孕酮;TM代表局部外用米诺地尔;T17αE0.025%代表外用0.025%的雌二醇;TT代表埋线疗法;LLLT代表低能量激光治疗;① 头发计数变化;② 不良反应。
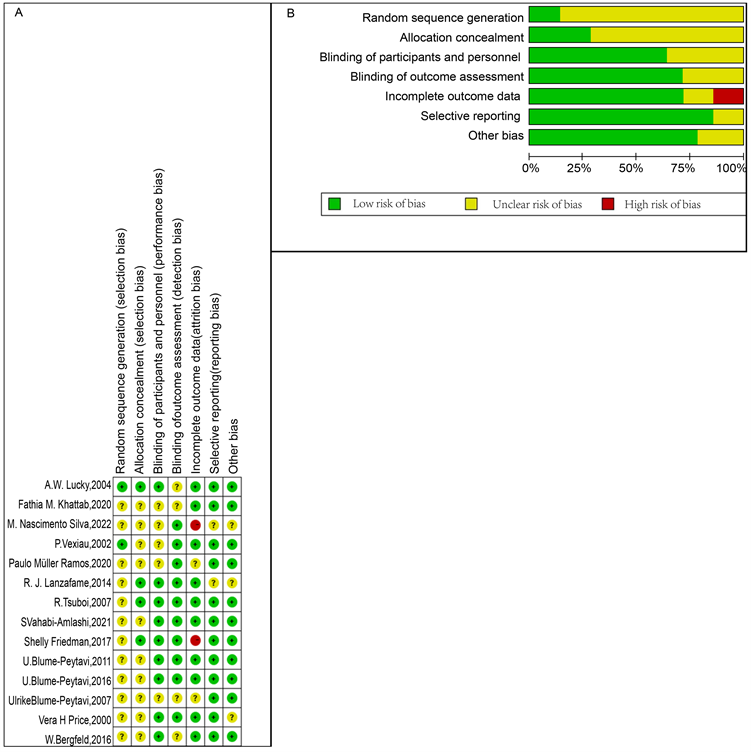
Figure 3. Risk assessment of included studies. Red indicates high risk, yellow indicates uncertain risk, and green indicates low risk
图3. 纳入研究的风险评估。红色表示高风险,黄色表示不确定风险,绿色表示低风险
3.4. 网状Meta分析结果
3.4.1. 头发计数变化
共纳入12个RCT,1个三臂试验,11个二臂试验,涉及11种干预措施,分别为外用1%/2%/5%的米诺地尔、口服0.25 mg/1 mg米诺地尔、外用雌二醇、低能量激光、口服醋酸环丙孕酮、埋线疗法 + 外用2%米诺地尔、口服1 mg非那雄胺、安慰剂。其网状证据关系图见图4(A)。节点劈裂法结果显示,直接比较与间接比较结果的差异无统计学意义(P > 0.05)。网状Meta分析结果提示低能量激光的疗效明显优于其他干预措施(表2),头发计数变化量累积排序曲线下面积(SUCRA)依次为低能量激光 > 埋线疗法 +外用2%米诺地尔 > 口服1 mg米诺地尔 > 外用5%米诺地尔 > 外用1%米诺地尔 > 外用2%米诺地尔 > 外用5%米诺地尔 > 口服0.25 mg米诺地尔 > 安慰剂 > 口服1 mg非那雄胺 > 口服醋酸环丙孕酮 > 外用0.025%雌二醇(图5(A)),提示低能量激光在改善头发计数方面疗效最为突出。

Figure 4. Web-based evidence relationship diagram. A: Changes in the amount of hair; B: Adverse reactions
图4. 网状证据关系图。A:头发数量变化;B:不良反应

Table 2. Results of net analysis of hair count changes (WMD, 95%CI)
表2. 头发计数变化的网状分析结果(WMD, 95%CI)

Table 3. Results of reticulation analysis of adverse reactions (RR, 95%CI)
表3. 不良反应的网状分析结果(RR, 95%CI)

Figure 5. Area under the cumulative ranking probability map. A: Hair count; B: Adverse reactions. Note: The larger the area below the line, the higher the ranking
图5. 累积排序概率图下面积图。A:头发计数;B:不良反应。注:线下面积越大表示排名越靠前
3.4.2. 不良反应
多数干预措施均发生了不良反应,其中有8个RCT [7] [8] [9] [10] [12] [14] [15] [19] 报告了因发生不良反应而脱落的病例,包括1个三臂试验 [9],7个二臂试验,涉及7种干预措施,分别为外用1%/2%/5%米诺地尔、口服1 mg非那雄胺、口服醋酸环丙孕酮、口服0.25 mg米诺地尔、安慰剂。网络证据关系图见图4(B)。节点劈裂法结果显示,直接比较与间接比较结果之间的差异无统计学意义(P > 0.05)。网状Meta分析结果显示,具体见表3。SUCRA依次为外用1%米诺地尔 > 安慰剂 > 口服醋酸环丙孕酮 > 口服1 mg非那雄胺 > 外用2%米诺地尔 > 外用5%米诺地尔 > 口服0.25 mg米诺地尔(图5(B))。
3.4.3. 发表偏倚检测
由于只有8个RCT报告了因发生不良反应而脱落的病例,因此不必做不良反应相关的发表偏倚。在头发计数方面,可以看到各研究散点分布于倒漏斗图(图6)两侧且较为对称,且大部分散点均位于倒漏斗图上部,提示该结局指标的发表偏倚和受小样本效应影响的可能性较小。
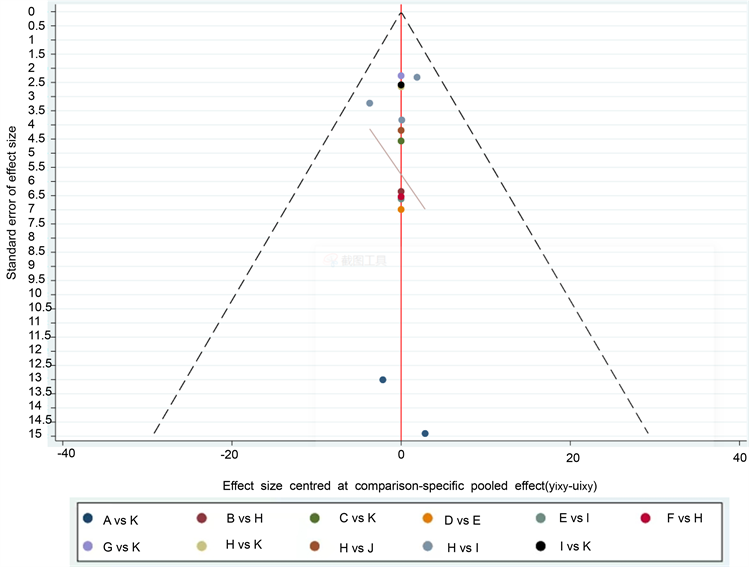
Figure 6. Hair counting funnel plot. Note: A: LLLT; B: OCA; C: OF1mg; D: OM0.25mg; E: OM1mg; F: T17αE0.025%; G: TM1%; H: TM2%; I: TM5%; J: TT + TM2%; K: placebo
图6. 头发计数漏斗图。注:A:LLLT;B:OCA;C:OF1mg;D:OM0.25mg;E:OM1mg;F:T17αE0.025%;G:TM1%;H:TM2%;I: TM5%;J:TT + TM2%;K:placebo
4. 讨论
FPHL的特点是头发密度弥漫性降低,主要影响头顶和前额的头发,与男性脱发不同的是,前额发际线通常被保留,脱发很少发展为完全秃顶,其临床脱发的患病率随着年龄的增长而增加,特别是在50岁之后,平均头发密度也随着年龄的增长而下降,40岁时头发密度的下降很明显,这表明脱发并非由于更年期的影响 [21]。
FPHL的治疗,目前以外用米诺地尔为主,在各国使用的药物浓度从2%~5%不等,大多数时候效果不尽人意,并且评估疗效以12月之后为宜,治疗周期较长。当然对于存在高雄激素水平的脱发患者加用抗雄激素药物,如非那雄胺、螺内酯、醋酸环丙孕酮等对治疗或许有帮助。尽管目前治疗措施效果不甚明显,但积极干预缓解症状和改善预后的临床获益是肯定的。
我们纳入的研究显示,外用不同浓度米诺地尔、口服不同剂量米诺地尔、低能量激光均对改善FPHL发量有效,而目前针对哪一种干预措施更适合FPHL患者尚缺乏循证医学证据,为此我们系统评价目前不同治疗FPHL的药物,旨在为临床医师提供参考,优化临床治疗方案。
本研究纳入14个研究,系统评价了11种治疗FPHL的干预措施,包括1%/2%/5%的米诺地尔、口服0.25 mg/1 mg米诺地尔、外用雌二醇、低能量激光、口服醋酸环丙孕酮、埋线疗法 + 外用2%米诺地尔、口服1 mg非那雄胺、安慰剂。最终网状结果显示,相比与其他干预措施,低能量激光具有最好的治疗效果(P < 0.05)。而口服非那雄胺、醋酸环丙孕酮、外用雌二醇对女性型脱发无用。所有纳入研究设计的干预措施均未见严重不良反应记录,在口服药物上多是头晕、恶心等轻微不良反应 [7],而在外用药物时则会有头皮瘙痒、干燥、脱屑等不良反应 [8] [9],而研究纳入的低能量激光治疗文中未提及不良反应发生 [13] [16]。
本研究的局限性:① 纳入研究中,部分RCT未报道随机化、分配隐藏方法和盲法的实施,可能存在选择和测量偏倚;② 部分纳入的RCT研究样本量较小,可能会影响研究结果的稳定性;③ 纳入研究中的部分干预措施缺乏直接比较;④ 纳入研究的患者脱发程度存在一定的差异,以及各研究间缺乏统一的发量变化测试方案,这可能会导致研究在估计治疗效果方面的异质性。
综上所述,低能量激光可能是治疗女性型较为脱发理想的干预措施。受纳入研究数量和质量限制,上述结论尚需开展更多高质量研究予以验证。
NOTES
*通讯作者。