1. 引言
骨性关节炎(Osteoarthritis, OA)是一种以关节软骨退行性变和继发性骨质增生为特征的慢性关节疾病,可导致关节僵硬、肿胀、疼痛和功能丧失,致畸致残率高,已成为国内外重大的公共健康问题 [1] 。由于人口老龄化和肥胖流行,OA的发病率不断上升,我国骨性关节炎的总患病率约为15%,40岁以上的患病率约为10%~17%,60岁以上达50%,而75岁以上则高达80% [2] 。OA患病率持续增长且危害严重,防控形势严峻;识别其危险因素并加以干预是健康中国战略部署的要求。传统观点认为OA与衰老、创伤等因素有关,但新近的流行病学及生物学证据表明OA不是单纯的退行性疾病,而是由“代谢紊乱”和“炎性衰老”等多因素共同导致。因此OA被认为是一种代谢性疾病,称为“代谢性骨性关节炎”(metabolic OA) [3] 。
残粒脂蛋白胆固醇(Remnant lipoprotein cholesterol, RLP-C)是富含甘油三酯的脂蛋白(TRLs)代谢产生的残留物,即乳糜微粒(CM)和极低密度脂蛋白(VLDL)被脂蛋白脂酶(LPL)分解,失去甘油三酯(TG)并产生富含胆固醇的代谢残留物 [4] 。新近的研究发现,在普通人群中,RLP-C与心血管疾病和胰岛素抵抗密切相关,亦有研究发现,OA与心血管疾病风险增加和胰岛素抵抗正相关 [5] [6] 。那么,RLP-C与OA是否相关?国内外缺乏研究。我们首次通过OA队列研究发现,RLP-C增高是OA进展的独立危险因素,为该病的防治提供了科学依据。
2. 研究对象与方法
2.1. 伦理
该研究得到了山东省立医院伦理委员会的批准,并在收集数据之前获得了所有受试者知情同意,并签署书面知情同意书。
2.2. 研究对象
本研究选取2017~2020年山东第一医科大学附属省立医院骨关节科、疼痛科、康复医学科的原发性膝OA患者作为研究对象。根据《中国骨关节炎诊疗指南(2021年版)》 [7] ,膝OA的诊断标准如下:1) 最近一个月膝关节反复疼痛;2) 站立或负重位时,X线片显示关节间隙狭窄、软骨下骨硬化、囊性变及关节边缘骨赘形成;3) 年龄 ≥ 50岁;4) 晨僵 ≤ 30分钟;5) 活动时有骨摩擦感或骨摩擦音。在上述诊断标准中,满足1和(2、3、4、5中的任意两个)即可被诊断为膝关节OA。最初共纳入了2918名参与者。
在数据收集过程中,有232名参与者因重要数据缺失等原因被排除,具体信息如下:1) 重要数据缺失(184人),如体重指数(BMI)、血压、血糖、各项血脂指标等;2) 影响脂质代谢的情况或疾病(41人),如妊娠、哺乳、恶性肿瘤、肝功能不全(丙氨酸转氨酶和/或天冬氨酸转氨酶 > 100 U/L)、肾功能不全(肌酐 > 105 umol/L);3) 服用影响血脂代谢的药物(7人),如他汀类药物、贝特类药物、糖皮质激素等。最终2686名参与者被纳入分析。
2.3. 研究方法
以kg和m为单位测量体重和身高,体重指数(BMI)用体重(kg)除以身高(m)的平方计算。使用电子血压计测量参与者上午6:00到10:00之间的血压,每次测量间隔3分钟,共计三次,并计算三次测量均值。
上午8:00至10:00采集参与者的空腹静脉血样。2小时内采用葡萄糖氧化酶法测定空腹血糖(FPG)。利用VARIANT II血红蛋白分析仪(Bio-Rad Laboratories)通过高效液相色谱法检测糖化血红蛋白(HbA1c)。分离血清和血浆后及时送往山东第一医科大学附属省立医院检验科,进行脂质谱分析,包括甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)和高密度脂蛋白胆固醇(HDL-C)。以TC减去LDL-C与HDL-C之和估算血清RLP-C含量。
高血压诊断标准为收缩压 ≥ 140 mmHg和/或舒张压 ≥ 90 mmHg [8] 。糖尿病为空腹血糖 ≥ 7.0 mmol/L和/或糖化血红蛋白 ≥ 6.5%和/或服用降糖药物和/或自述患有糖尿病 [9] 。
所有参与者均拍摄患侧膝关节X线平片,由专业医师进行数据采集,并根据Kellgren-Lawrence分级标准 [10] 对膝OA病变情况进行评估和分级。Kellgren-Lawrence分级标准如下:0级,正常膝关节;I级,关节间隙可疑变窄,可能有骨赘;II级,有明显骨赘,关节间隙轻度变窄;III级,中等量骨赘,关节间隙变窄较明确,软骨下骨骨质轻度硬化改变,范围较小;IV级,大量骨赘形成,可波及软骨面,关节间隙明显变窄,硬化改变极为明显,关节肥大及明显畸形。
2.4. 统计分析
采用Windows SPSS 26.0统计软件对资料进行统计分析。利用Kolmogorov-Smirnov检验评估所有变量是否满足正态性,符合正态分布的连续变量用平均值±标准差表示,非正态分布的连续变量则用中位数(四分位数间距)表示,分类变量以计数(百分比)表示。使用非参数检验评估OA分级、性别、糖尿病、高血压以及不同BMI组的RLP-C分布差异。
既往有研究发现,OA的患病率存在男女差异 [11] ,因此在本研究中,对男性和女性分别进行了数据分析。通过有序Logistic回归模型评估各脂质成分与OA进展之间的相关性,并对所有可能影响脂质成分与OA进展之间相关性的潜在混杂因素进行校正,包括年龄、性别、BMI、高血压、糖尿病。
最后按照四分位数将血清RLP-C分为四个亚组,采用线性趋势X2检验分析血清RLP-C与OA进展之间是否存在线性趋势。
在上述统计方法中,所有计算的P值均为双侧,以P<0.05为差异有统计学差异。
3. 结果
3.1. 一般资料
纳入本次研究的所有参与者(N = 2686)的一般资料特征如表1所示。参与者的年龄中位数为64岁,身高中位数为1.59 m,体重中位数为70 kg,BMI中位数为27.92 kg/m2。有接近一半的患者合并高血压,约1/5的患者合并糖尿病。值得注意的是,本研究中男女参与者的比例大约为1:3,女性人数明显多于男性,该结果与既往研究结果相符,OA在女性人群更多见 [12] [13] 。

Table 1. Participant characteristics
表1. 参与者一般资料
BMI:体重指数Body mass index;TG:甘油三酯Triglyceride;TC:总胆固醇Total cholesterol;LDL-C:低密度脂蛋白胆固醇Low density lipoprotein cholesterol;HDL-C:高密度脂蛋白胆固醇High density lipoprotein cholesterol;RLP-C:残粒脂蛋白胆固醇Remnant lipoprotein cholesterol。
在血脂各项指标中,TG、TC、LDL-C、HDL-C的中位数分别为1.37 mmol/L、5.05 mmol/L、3.07 mmol/L、1.24 mmol/L,血清RLP-C中位数为0.64 mmol/L,其水平在不同性别之间存在明显差异,女性明显高于男性(男性:0.59 (0.38, 0.81) mmol/L;女性:0.66 (0.45, 0.92) mmol/L,P < 0.001),而且该指标在糖尿病患者中较高(无糖尿病:0.64 (0.43, 0.87) mmol/L;有糖尿病:0.66 (0.43, 0.98) mmol/L,P = 0.023)。有无高血压及BMI均不影响血清RLP-C水平(如图1)。

Figure 1. Distribution of RLP-C by gender (a), diabetes (b), hypertension (c) and BMI (kg/m2) (d). The presence or absence of hypertension and BMI does not affect the level of serum RLP-C. However, the level of serum RLP-C in diabetes patients was higher than that in nondiabetes patients, female’s levels were substantially higher than male’s
图1. 按性别(a)、糖尿病(b)、高血压(c)和BMI (kg/m2) (d)类别划分的残粒脂蛋白胆固醇分布。有无高血压及BMI并不影响血清残粒脂蛋白胆固醇水平,但女性以及糖尿病患者较男性和非糖尿病患者血清残粒脂蛋白胆固醇水平增加
3.2. 血清RLP-C水平随OA严重程度增加而升高
为评估血清RLP-C水平与OA严重程度的关系,我们按照OA分级分别计算各组患者的RLP-C水平,如图2所示,随着OA分级增加,血清RLP-C水平逐渐升高,与I级OA患者相比,IV级OA患者的血清RLP-C水平增加了61.54% (I级:0.52 (0.30, 0.68);II级:0.61 (0.45, 0.80);III级:0.62 (0.41, 0.86);IV级:0.84 (0.57, 1.14),P < 0.001)。
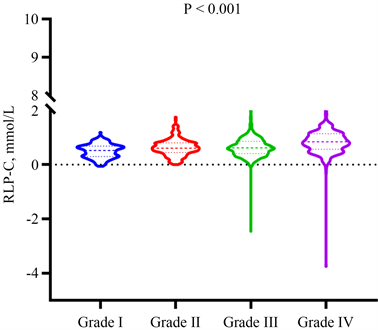
Figure 2. Serum RLP-C levels of patients in different OA grades. The level of serum RLP-C in patients with grade IV was higher than that in patients with the other three grades, and the level of serum RLP-C gradually increased with the grading of OA
图2. OA各分级中患者的血清残粒脂蛋白胆固醇水平。IV级OA患者的血清残粒脂蛋白胆固醇水平均要高于其他三个分级OA患者,并且血清残粒脂蛋白胆固醇水平随OA分级逐渐升高
3.3. 血清RLP-C水平升高是OA进展的重要危险因素
为进一步明确影响OA进展的危险因素,我们采用有序Logistic回归的方法分别分析了各危险因素的比值比(OR)。如表2所示,TG、TC、LDL-C和RLP-C均是OA进展的危险因素,而HDL-C却是阻止OA进展的保护因素。在各项危险因素中,RLP-C与TG增加OA进展的风险最高,但二者对男女人群的影响程度存在差异。在男性人群中,与正常水平者相比,RLP-C水平升高者OA进展风险增加约3.41倍,在女性人群,这个风险增加约1.71倍;而TG水平对女性人群影响更大,风险比为3.31,男性人群为1.56。不过,在总人群中,TG促进OA进展的风险要高于RLP-C (2.55:1.79)。TC与LDL-C亦是OA进展的危险因素,但比值比较前两个指标低,OR值分别为1.29和1.55,而且男女差异不大。值得注意的是,与HDL-C水平正常的人相比,HDL-C水平升高者,OA进展的风险可降低约70% (男性降低62%,女性降低75%),提示HDL-C是阻止OA进展的重要的保护因素。


Table 2. Univariate ordered logistic regression analysis
表2. 单因素有序Logistic回归分析
TG:甘油三酯Triglyceride;TC:总胆固醇Total cholesterol;LDL-C:低密度脂蛋白胆固醇Low density lipoprotein cholesterol;HDL-C:高密度脂蛋白胆固醇High density lipoprotein cholesterol;RLP-C:残粒脂蛋白胆固醇Remnant lipoprotein cholesterol。
随后,我们进一步应用多因素有序Logistic回归方法校正了影响OA的混淆因素,例如:年龄、BMI、高血压与糖尿病等。如表3所示,结果并未发生显著变化,RLP-C、TG、TC与LDL-C依然是OA进展的危险因素,而HDL-C仍是保护性因素。


Table 3. Multivariate ordered logistic regression analysis
表3. 多因素有序Logistic回归分析
TG:甘油三酯Triglyceride;TC:总胆固醇Total cholesterol;LDL-C:低密度脂蛋白胆固醇Low density lipoprotein cholesterol;HDL-C:高密度脂蛋白胆固醇High density lipoprotein cholesterol;RLP-C:残粒脂蛋白胆固醇Remnant lipoprotein cholesterol。
3.4. OA严重程度随着血清RLP-C水平升高呈线性增加
我们进一步将RLP-C按照四分位数分为四个亚组(A组:RLP-C ≤ 0.43 mmol/L,B组:0.43 mmol/L < RLP-C ≤ 0.64 mmol/L,C组:0.64 mmol/L < RLP-C ≤ 0.89 mmol/L,D组:RLP-C > 0.89 mmol/L),分析各组中OA分级所占百分比,如图3所示,I级OA患者占比随着血清RLP-C水平升高逐渐减少,而IV级OA患者占比随着血清RLP-C水平升高逐渐增加;与A组相比,D组中IV级OA患者的占比增加了2倍。进一步统计分析发现,各亚组之间的OA分级占比存在明显差异(表4),除了A组和B组之外,其余各亚组两两比较均具有统计学意义(P < 0.05,表5)。
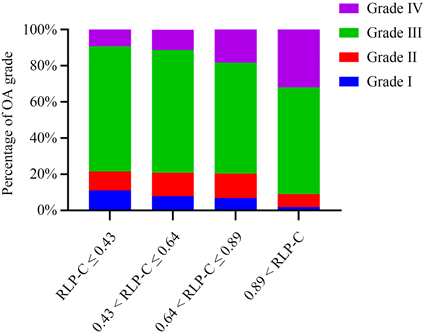
Figure 3. Percentage of OA grades in RLP-C subgroup. The RLP-C was divided into four subgroups according to the quartile, and the percentage of OA grade in each group was compared. The proportion of patients with grade I gradually decreased with the increase of serum RLP-C level, while the percentage of patients with grade IV was opposite
图3. 残粒脂蛋白胆固醇亚组中OA分级所占百分比。将残粒脂蛋白胆固醇按照四分位数划分为四个亚组,比较各组中OA分级所占比,I级OA患者占比随着血清残粒脂蛋白胆固醇水平升高逐渐减少,而IV级OA患者占比与之相反

Table 4. The proportion difference of OA grades in each subgroup of RLP-C
表4. 残粒脂蛋白胆固醇各亚组中OA分级占比差异

Table 5. Paired comparison of the proportion of OA grades in each subgroup of RLP-C
表5. 残粒脂蛋白胆固醇各亚组中OA分级占比的成对比较
A: RLP-C ≤ 0.43 mmol/L; B: 0.43 mmol/L < RLP-C ≤ 0.64 mmol/L; C: 0.64 mmol/L < RLP-C ≤ 0.89 mmol/L; D: RLP-C > 0.89 mmol/L.
在此基础上我们应用线性趋势卡方检验进一步评估了血清RLP-C水平与OA分级是否具有线性相关关系。如表6所示,无论在总人群,还是男性或者女性人群,OA分级与血清RLP-C水平之间呈显著线性正相关(相关系数R:总人群0.209,男性0.201,女性0.217)。上述结果提示,随着血清RLP-C水平升高,OA严重程度呈线性增加。

Table 6. Linear trend of RLP-C and OA grades
表6. 残粒脂蛋白胆固醇与OA分级的线性趋势
4. 讨论
在该研究中,我们建立了一个大型的OA研究队列(N = 2686),评估了血脂各指标与膝OA的关系,首次发现血清RLP-C是膝OA进展的重要独立危险因素。随着血清RLP-C水平升高,OA严重程度呈线性增加,在男性人群中,与正常水平者相比,RLP-C水平升高者OA进展风险增加约3.41倍,在女性人群,这个风险增加约1.71倍,校正混杂因素后,结果仍具有统计学意义。同时还发现,除RLP-C外,TG、TC和LDL-C均是OA进展的危险因素,而HDL-C是阻止OA进展的保护因素。该研究进一步证实了代谢因素——血脂紊乱在OA进展中发挥重要作用,揭示了不同血脂指标的致病作用,明确了血清RLP-C是膝OA进展的重要独立危险因素,为OA的精准干预提供了科学依据,为实现健康中国战略目标奠定基础。
OA作为一种慢性退行性疾病,传统观念认为单纯的机械磨损是造成该疾病发生发展的重要因素 [14] ,然而随着研究的不断进展,该观点已经被逐渐摒弃。研究发现,OA发病的原因并非仅仅局限于机械损伤,而是由多种因素共同参与所致 [15] 。在诸多代谢因素中,以脂代谢紊乱尤为重要 [16] 。Ran L [17] 等人在一项中国农村人口OA与高脂血症关系的研究中发现,高脂血症与OA患病率相关(调整后OR 1.83,95%可信区间1.355~2.477,P < 0.001)。有关血脂成分中的TG、TC、LDL-C与OA的相关性已有研究报道,并且其对OA的发生发展起着不同程度的促进作用 [18] [19] [20] ,然而RLP-C对OA作用的研究却很少。
RLP-C是富含甘油三酯脂蛋白(Triglyceride-rich lipoproteins, TRLs)代谢的残余物,由非禁食状态下的乳糜微粒(Chylomicron, CM)残余物和禁食状态下的极低密度脂蛋白(Very low density lipoprotein, VLDL)和中等密度脂蛋白(Intermediate density lipoprotein, IDL)组成 [21] 。先前的证据表明,RLP-C与主要不良心血管事件(MACE)的风险增加有关,这不仅可归因于动脉粥样硬化斑块的形成,还可归因于局部炎症 [22] ,而OA的发生发展也被认为是一种慢性炎症 [23] ,这可能在两者之间存在某种相互联系。由于RLP-C的研究主要集中在RLP-C与MACE之间的关系上,因此尚未对血清RLP-C水平与OA进展的关系进行研究。在一项病例报告中发现 [24] ,高脂血症患者在六年内每天摄入30,000 IU视黄醇后,股骨头横截面的组织学显示破坏性骨关节炎,由于没有发现其他原因,所以推测视黄醇可能会导致退行性关节疾病快速进展。尽管停止了视黄醇的摄入,但由于高脂血症,临床症状仍然存在。而CM的增多和VLDL的较高比例可能代表了第二个视黄醇池,因此CM与VLDL作为RLP-C的成分可能与OA存在某种联系。
虽然我们的研究结果显示血清RLP-C与OA进展之间的相关性,但是在研究对象选择方面,由于缺少膝关节X线检查,无法纳入非OA健康对照者作为对照组,因此没有评估血清RLP-C与OA发生之间的相关性。
总之,我们的结果表明,血清RLP-C与OA进展密切相关,是重要的独立危险因素。本研究可为OA的病因治疗和一级预防提供可靠依据。在OA的发生和发展过程中,RLP-C可能异常积聚在软骨细胞或关节滑液中,造成局部慢性炎症,然而其造成炎症的具体机制尚未有明确研究和报道,可以作为今后的研究方向进行深入探讨。但鉴于RLP-C与OA之间存在联系,因此维持血清RLP-C水平在适当范围内,甚至生活方式干预,可能是抵抗OA发展的可行方法。
基金项目
国家自然科学基金(81500608),山东省自然科学基金(ZR2021HM150)。
NOTES
*通讯作者。