1. 引言
类风湿性关节炎(Rheumatoid Arthritis, RA)是一种由身体免疫系统攻击自身关节导致的疾病,其主要特征为关节炎症状的侵袭性 [1] 。滑膜炎是其主要的病理变化,它可以扩散到关节软骨、韧带、肌腱和软骨下骨,导致关节软骨、骨和关节囊的破坏,最终会导致关节畸形和功能丧失 [2] [3] 。据调查,RA在全球的发病率为0.5%~1%,在我国的发病率为0.32%~0.36%,严重危害人类的健康 [4] 。现代医学主要通过药物治疗缓解和控制,RA病程缠绵难愈一般需长期用药,目前临床上治疗RA的药物有:传统抗风湿药、生物制剂及各种生物仿制药。大多数口服药物均会出现不同程度的毒副作用,如目前首选治疗RA的甲氨蝶呤,其能有效缓解RA症状,修复骨破坏,对于活动期RA、良性自限性RA和进展侵蚀性RA均能有效改善。但长期应用会引发胃肠道反应,及其他皮肤疾病,如皮肤发红、瘙痒或皮疹,甚至会引起伪膜性或出血性肠炎等症状 [5] [6] 。外用制剂具有众多优势,能够避免口服药物受到胃肠道分泌物和胃酸等不利因素的干扰;降低血药浓度的峰谷变化以减轻药物的不良反应;减少了给药的次数,并且病人能够独立服药,服药依从性好;用药期间若出现不良反应能随时中断使用 [7] 。常用的外用制剂类型主要有乳膏剂、软膏剂、贴膏剂和凝胶剂。但传统中药外用剂型存在着工艺单一、药物吸收差、不易通过皮肤角质层等问题,例如传统膏药生产时药物会与高温油发生化学反应导致药效减低等问题,尤其是某些芳香通窍的药物在温度较高时更容易挥发、破坏有效成分从而导致药效下降 [8] [9] 。
纳米乳(Nanoemulsion, NE)是粒径为10~100 nm乳滴散布于另一液体中而形成胶体分散体系,乳滴多为球形,透明或半透明。其促渗作用可改善角质层脂质双层流动性、影响皮肤毛囊透皮吸收、提高药物溶解性等,同时缓释效果好。因此,将药物制备成纳米乳能够很好的解决上述问题 [10] 。
艾纳香又称大风叶、大毛药、冰片艾等,是菊科(Asteraceae)艾纳香属植物艾纳香[Blumea balsamifera (L.) DC.]的新鲜或干燥地上部分,是苗族、布依族、黎族、傣族等少数民族的重要药材,具有消除风湿、驱除害虫的功效,可用来治疗类风湿性关节炎、疮疖痈肿、皮肤瘙痒和跌打损伤 [11] 。艾纳香含有大量挥发油、黄酮类成分,而主要发挥抗炎、镇痛作用的是挥发油中的左旋龙脑、(-)-芳樟醇、反式石竹烯等 [12] 。研究发现,挥发油及其成分在透皮吸收过程中能够打破脂质细胞的结构,使其由有序变为无序,增加细胞流动性,从而弱化皮肤对药物的屏障作用,能促进药物吸收 [13] 。
综上所述,基于纳米乳能解决传统外用制剂存在的问题,艾纳香挥发油促进药物吸收,本实验将两者结合,以艾纳香挥发油作为油相,艾纳香水提物作为水相,采用水转相法将其制备成纳米乳,并对其进行质量评价。以期丰富艾纳香中药制剂的种类,为其进一步开发提供思路及实验依据。
2. 仪器与试药
2.1. 仪器
万分之一电子天平(ME204E,瑞士梅特公司);超声波清洗仪(JOYN-10A,上海乔跃电子有限公司);磁力加热搅拌器(D1-1A,常州澳华仪器有限公司);粒径分析仪(DelsaMax PRO,苏州冠卓自动化科技有限公司);离心机(H1650,湖南湘仪实验室仪器开发有限公司);pH计(PHS-3C,上海仪电科学仪器股份有限公司);粒径分析仪(DelsaMax PRO,苏州冠卓自动化科技有限公司);气相色谱仪(Trace1300,赛默飞世尔科技(中国)有限公司);色谱柱(USP579947H,安捷伦科技有限公司)。
2.2. 药物与试剂
龙脑对照品(110881-201709,成都普思生物科技股份有限公司);水杨酸甲酯(PS000861,成都普思生物科技股份有限公司);环己烷(20211201,重庆江川化工有限公司);艾纳香油(20221114,江西海麟香料有限公司);吐温-80 (214H011,北京索莱宝科技有限公司);蓖麻油聚氧乙烯醚(C804845,上海麦克林生化科技有限公司);氢化蓖麻油(E873767,上海麦克林生化科技有限公司);正丁醇(20211101,重庆江川化工有限公司);无水乙醇(20210120,常熟市鸿盛精细化工有限公司);聚乙二醇-400 (802A011,北京索莱宝科技有限公司);艾纳香油(20221114,江西海麟香料有限公司);pH标准缓冲液(20221204,四川普西奥标物科技有限公司);亚甲基蓝(Q/12HB 3651-2010,天津科密欧化学试剂有限公司);油红O (808M051,北京索莱宝科技有限公司)。
3. 实验方法
3.1. 艾纳香纳米乳的制备工艺
本实验对艾纳香纳米乳制备工艺进行优化,以粒径和多分散系数(PDI)为指标,优化处方,进行如下处方筛选和单因素考察。
3.1.1. 表面活性剂和助表面活性剂的选择
在本实验中,选择了乳化效果偏好的吐温-80 (Tween-80)、蓖麻油聚氧乙烯醚(EL-40)和氢化蓖麻油(PEG-60)作为表面活性剂,选择了副作用和毒性都偏小的聚乙二醇-400 (PEG-400)、无水乙醇和正丁醇作为助表面活性剂。
参考袁珍珍、尹寿玉等 [14] 在杜香油纳米乳体外透皮吸收及药效学研究中杜香油纳米乳的制备方法,其表面活性剂与助表面活性剂的质量比为3:1,混匀后得到9种表面活性剂–助表面活性剂组合,由三种表面活性剂分别与三种助表面活性剂组成。再以艾纳香挥发油为油相,将表面活性剂–助表面活性剂组合和挥发油按8:2的比例混合,搅拌均匀后,边震荡边加入水相进行滴定,以观察是否形成了澄清透明的纳米乳液。
3.1.2. 单因素考察
① 乳化剂及助乳化剂比例的考察
从安全性和乳化效果的角度考虑,选择吐温-80和正丁醇为考察对象,为了考察乳化剂及助乳化剂比例在纳米乳液体系中包埋油脂的效果,改变乳化剂及助乳化剂比例进行了一系列试验。分别制备乳化剂及助乳化剂比例为6:1、5:1、4:1、3:1、2:1的纳米乳,通过粒径、多分散系数作为指标考察制剂性质变化。
② 艾纳香油投入量的考察
分别制备不同艾纳香油投入量(2%, 4%, 6%, 8%, 10%)的纳米乳,考察不同艾纳香油投入量对于纳米乳的影响,测出粒径及多分散系数。
③ 艾纳香水提物投入量的考察
分别制备不同艾纳香水提物投入量(45%, 50%, 55%, 60%, 65%)的纳米乳,考察不同艾纳香水提物投入量对于纳米乳的影响,测出粒径及多分散系数。
④ 搅拌温度的考察
固定基本处方中物料的用量,分别在搅拌温度为20℃、25℃、30℃、35℃、40℃下制备纳米乳,考察搅拌温度对于纳米乳的影响,测出粒径及多分散系数。
⑤ 搅拌速度的考察
固定基本处方中物料的用量,分别在搅拌速度为240 r/min、360 r/min、480 r/min、600 r/min、720 r/min下制备纳米乳,考察搅拌速度对于纳米乳的影响,测出粒径及多分散系数。
3.1.3. 正交试验优化艾纳香纳米乳处方
根据单因素试验结果,设计正交试验优化最佳处方。由于乳化剂及助乳化剂比例、艾纳香油投入量及艾纳香水提物投入量是影响纳米乳粒径最大的三因素,故选此三种用量做正交优化实验设计。根据预实验结果对上述三因素各取三水平,按L9 (33)正交设计试验表安排试验,以粒径为评价指标,以粒径均匀且粒径较小为好,优选用量,正交试验因素水平见表1。
3.1.4. 艾纳香纳米乳最佳处方工艺验证试验
根据正交试验筛选优化的最优处方工艺,平行制备三批艾纳香纳米乳,测定其粒径、PDI,评价该处方及工艺的重复性和稳定性。
3.2. 艾纳香纳米乳的质量评价
3.2.1. 外观观察
将艾纳香纳米乳置于实验台上,用肉眼观察纳米乳的外观形态,是否有絮凝、破乳、分层现象。
3.2.2. 结构类型鉴别
本实验采用了染色法来鉴别纳米乳的结构类型。取两份纳米乳,同时分别滴加蓝色水性染料亚甲基蓝和红色油性染料油红O各一滴,通过两者不同的分散速度判断纳米乳的类型,其中油红O分散较快时为W/O型,亚甲基蓝分散较快时则为O/W型。
3.2.3. pH值测定
取适量艾纳香纳米乳,用pH计测试其pH值。
3.2.4. 粒径分布和多分散系数(PDI)测定
取适量艾纳香纳米乳,用水稀释10倍,用粒度分析仪测定其平均粒径、多分散系数(PDI)。
3.2.5. 微观形态观察
在透射电子显微镜下观察艾纳香纳米乳液的微观形态。
3.2.6. 稳定性评价
① 离心稳定性
取适量艾纳香纳米乳于适宜的离心管内,4000 r/min的转速条件下,离心30分钟,观察纳米乳在离心后是否出现分层、破乳等现象,重复三次实验。
② 稀释稳定性
取等量的艾纳香纳米乳用水稀释至不同的倍数(10、50、100、200、400倍)观察其外观,测定平均粒径、多分散系数(PDI),评价其稀释稳定性。
③ 放置稳定性
取同一批次的艾纳香纳米乳样品,考察其在不同温度下稳定性的研究。具体如下:将艾纳香纳米乳分别放置在4℃及室温条件下,于0、7、14、21、28天取出,观察其外观,测定平均粒径、多分散系数(PDI),评价其放置稳定性。
3.3. 艾纳香纳米乳中左旋龙脑的含量测定
3.3.1. 色谱条件
色谱柱:以聚乙二醇(PEG-20M)为固定相的毛细管柱(柱长为30 m,内径为0.25 mm,膜厚度为0.5 μm);进样口温度为170℃;FID检测器温度为220℃;柱温为100℃;进样量1 μL;分流进样,分流比为10:1;定量方法为内标法。理论塔板数按龙脑峰计算应不低于6000。
3.3.2. 溶液的制备
① 内标溶液的制备
精密称取水杨酸甲酯25 mg,至100 mL量瓶中,加环己烷溶解并定容至刻度,摇匀,制成每1 mL含水杨酸甲酯为0.25 mg的溶液,作为内标溶液。
② 对照品溶液的制备
精密称取左旋龙脑对照品1.5 mg,用内标溶液(水杨酸甲酯0.25 mg/mL)溶解,并定容至10 mL量瓶中,即得左旋龙脑对照品贮备液。
③ 供试品溶液的制备
精密称取艾纳香样品2.00 g置于锥形瓶中,精密加入内标溶液(水杨酸甲酯0.25 mg/mL) 25mL,称质量并密封口塞,超声提取30 min,放冷,用内标溶液补足减失的质量,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,作为供试品溶液。
3.3.3. 专属性实验
取缺艾纳香纳米乳按“2.3.2”项下方法制得缺艾纳香阴性对照溶液。取对照品溶液、供试品溶液、阴性对照溶液,按选定色谱条件进行分析。
3.3.4. 线性关系
精密称取龙脑对照品适量,加环己烷制成每1 mL含龙脑1.0104 mg的对照品溶液。精密量取上述对照品溶液0.2、0.4、1、2、4 mL分别置5 mL量瓶中,精密加入上述水杨酸甲酯内标溶液(0.25 mg/mL)各1 mL,再用环己烷稀释至刻度,摇匀,分别进样,测定龙脑峰面积。
3.3.5. 精密度试验
精密吸取龙脑对照品溶液1 μL,连续进样6次,记录龙脑和水杨酸甲酯的峰面积考察仪器精密度。
3.3.6. 稳定性试验
取一份艾纳香纳米乳按照“2.3.2”供试品溶液的制备方法制备,分别于0、2、4、6、8、10 h,进样1 μL,以龙脑和水杨酸甲酯峰面积考察艾纳香纳米乳的稳定性。
3.3.7. 重复性试验
平行称取6份同一批次的艾纳香纳米乳样品,每份2 g,照“2.3.2”供试液制备方法制备供试液,精密吸取供试液1 μL进样,记录龙脑和水杨酸甲酯峰面积并计算其含量及RSD。
3.3.8. 加样回收试验
取同一批样品约0.2 g,精密称定,置具塞锥形瓶中,精密加入龙脑对照品溶液(浓度0.15 mg/mL) 2mL与水杨酸甲酯内标溶液(浓度0.25 mg/mL) 8mL,混匀,再按“2.3.2”供试品溶液制备方法制备,记录龙脑和水杨酸甲酯峰面积并计算其加样回收率及RSD。
3.3.9. 含量测定
取样品三份,每份约2 g,按“2.3.2”供试品溶液制备方法制备和“2.3.1”项下色谱条件测定,计算三份样品中龙脑含量。
4. 结果
4.1. 艾纳香纳米乳的制备
4.1.1. 表面活性剂和助表面活性剂的选择结果

Table 2. Formation of Blumea balsam oil nanoemulsion
表2. 艾纳香油纳米乳形成情况
观察表2可见在三种表面活性剂Tween-80、PEG-60、EL-40中,Tween-80形成的纳米乳性状优于PEG-60和EL-40。而在三种助表面活性剂正丁醇、PEG-400、无水乙醇中,Tween-80与正丁醇组合形成的纳米乳优于PEG-400和无水乙醇。因此选择Tween-80与正丁醇作为纳米乳的表面活性剂与助表面活性剂。
4.1.2. 单因素考察结果
① 乳化剂及助乳化剂比例的考察结果
乳化剂及助乳化剂比例对艾纳香纳米乳的影响见表3,结果表明随着体系中表面活性剂及助表面活性剂比例的增加,纳米乳的粒径越小,当表面活性剂及助表面活性剂比例为4:1时,粒径较小且PDI最小,表明此时乳液最稳定。

Table 3. The investigation results of the proportion of surfactants and cosurfactants
表3. 表面活性剂及助表面活性剂比例的考察结果
② 艾纳香油投入量的考察结果
由表4可看出随着体系中艾纳香油投入量的增加,纳米乳的粒径越大。当精油投入量为4%时,粒径较小且PDI最小,表明此时乳剂最稳定。

Table 4. Investigation results of the amount of Blumea balsam input
表4. 艾纳香投入量的考察结果
③ 艾纳香水提物投入量的考察结果
投入量结果如表5显示,当艾纳香水提物投入量为50%时,粒径最小且PDI最小。表明此时乳剂最稳定。
④ 搅拌温度的考察结果
搅拌温度结果如表6显示,当搅拌温度为25℃时,纳米乳的粒径和PDI最小,表明在该搅拌温度下形成的纳米乳最稳定。

Table 5. Investigation results of the amount of Blumea balsam input
表5. 艾纳香投入量的考察结果

Table 6. Investigation results of stirring temperature
表6. 搅拌温度的考察结果
⑤ 搅拌速度的考察结果
搅拌速度结果如表7显示,当搅拌速度为480 r/min时,纳米乳的粒径和PDI最小,表明在该搅拌速度下形成的纳米乳最稳定。

Table 7. County level planning schedule
表7. 县域等级规划一览表
4.1.3. 艾纳香纳米乳处方优化结果
根据单因素考察结果设置3因素3水平正交表进行正交试验,以粒径和PDI为评价指标,PDI值越小表明纳米乳分散越均匀稳定。对正交试验结果进行直观分析(表8)可知,3个因素中对于艾纳香纳米乳影响程度的大小顺序为艾纳香油投入量 > 艾纳香水提物投入量 > 表面活性剂及助表面活性剂比例。艾纳香油投入量对艾纳香纳米乳粒径具有显著性影响(P < 0.05),结果见表9。根据分析结果可知,筛选出的艾纳香纳米乳最佳处方为艾纳香油0.21 g,艾纳香水提物5.21 g,吐温80 4.00 g,正丁醇1.00 g。
4.1.4. 最佳制备工艺验证结果
称取适量的干燥的艾纳香叶,粉碎,过筛,提取溶剂为水,料液比为1:30,超声提取30分钟,即得艾纳香水提物,备用。称取吐温-80 4.00 g,正丁醇1.00 g,艾纳香油0.21 g,置于烧杯中,在25℃下磁力搅拌器以480 r/min的转速搅拌10 min,另称取5.21 mL艾纳香水提物溶液,缓慢加入正在搅拌的烧杯中,使油水两相混合均匀,即得艾纳香纳米乳。
按照最佳处方,平行制备三份艾纳香纳米乳,测出粒径,结果见表10。

Table 10. Optimal prescription particle size results table
表10. 最佳处方粒径结果表
4.2. 艾纳香纳米乳的质量评价结果
4.2.1. 外观
艾纳香纳米乳为浅棕色溶液,澄清度较好,肉眼未观察到不溶性物质。
4.2.2. 结构类型
如图1所示,艾纳香纳米乳在水性染料亚甲基蓝中的扩散速度更快,因此该纳米乳为水包油(O/W)型。

Figure 1. Staining method to determine the structure of nanoemulsion
图1. 染色法判断纳米乳结构
4.2.3. pH值
结果如表11显示,该实验制备的艾纳香纳米乳的pH值为6.69,性质相对安全、温和。
4.2.4. 纳米乳粒径与多分散系数(PDI)
本实验采用贝克曼粒径仪测定纳米乳的粒径、多分散系数(PDI),结果如表12所示,纳米乳的平均粒径为11.37 nm,多分散系数为0.23,质量良好。

Table 12. Results of particle size and polydispersity coefficient
表12. 粒径与多分散系数结果
4.2.5. 微观形态
图2. 艾纳香纳米乳的透射电镜图
由图2可知,艾纳香纳米乳在100 nm以内,微观状态下呈圆球形,大小均一,分布均匀,状态良好。
4.2.6. 稳定性评价
① 离心稳定性
艾纳香纳米乳在4000 r/min的转速下离心30分钟后,纳米乳体系未出现破乳、絮凝、分层等现象,颜色维持不变。
② 稀释稳定性
结果表明,艾纳香纳米乳的外观依旧保持稳定,且呈浅棕色,未出现分层、絮凝和沉淀等现象;如表13与图3所示,粒径保持在100 nm以内,PDI在0.3以内,都在允许范围内,因此具有较好的稀释稳定性。

Table 13. Dilution stability of Blumea balsamifera nanoemulsion
表13. 艾纳香纳米乳的稀释稳定性

Figure 3. Dilution stability of Blumea balsamifera nanoemulsion
图3. 艾纳香纳米乳的稀释稳定性
③ 放置稳定性

Table 14. Effects of different storage temperatures on the appearance of Blumea balsamifera nanoemulsion
表14. 不同的放置温度对艾纳香纳米乳外观的影响
由表14、图4和图5可知,在4℃下,艾纳香纳米乳28天内都呈现浅棕色透明液体,未发生变化,而其平均粒径略有增加趋势,但PDI变化不明显;但在25℃下的纳米乳在第28天观察发现其变得稍微浑浊,并且从第14天后其平均粒径和PDI都有较大的变化,说明温度是能够对艾纳香纳米乳的放置稳定性产生一定影响的,艾纳香纳米乳在4℃环境中放置28天是相对稳定的。因此,维持纳米乳系统的放置稳定性应该冷藏贮存。
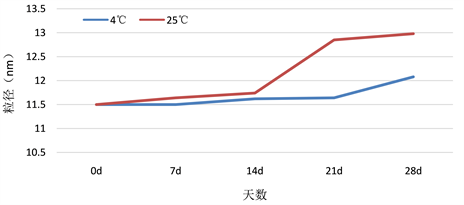
Figure 4. Changes in particle size of Blumea balsamifera nanoemulsion at different storage temperatures
图4. 不同放置温度下艾纳香纳米乳的粒径变化
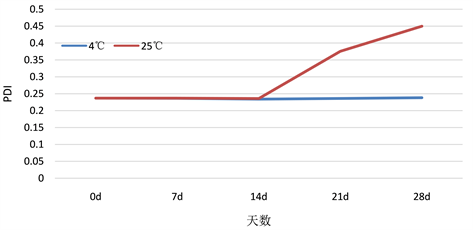
Figure 5. PDI changes of Blumea balsamifera nanoemulsion at different storage temperatures
图5. 不同放置温度下艾纳香纳米乳的PDI变化
4.3. 艾纳香纳米乳中左旋龙脑的含量
4.3.1. 专属性实验
专属性结果如图6所示,实验结果表明缺艾纳香阴性对照的色谱图中无干扰峰,表明该方法专属性好。
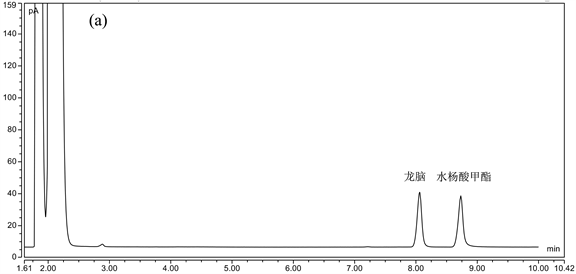
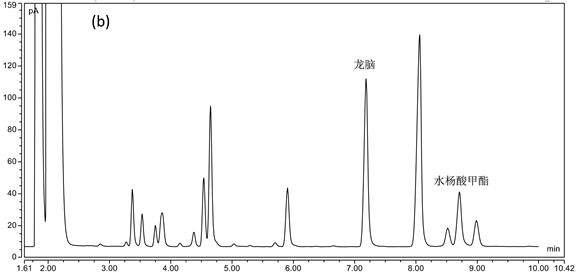
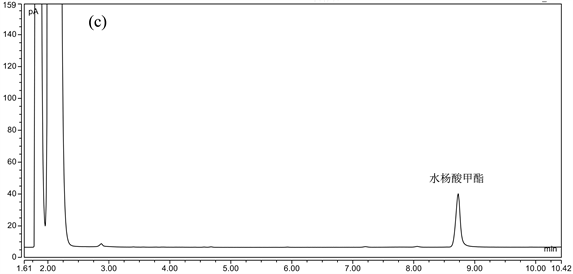
Figure 6. GC chromatograms of reference substance (a), sample (b) and methyl salicylate negative control (c)
图6. 对照品(a)、样品(b)、水杨酸甲酯阴性对照(c)的GC色谱图
4.3.2. 线性关系
以龙脑对照品溶液浓度为横坐标,以对照品与内标的峰面积比值为纵坐标,绘制标准曲线,计算回归方程:y = 29.12x + 0.3743,R2 = 0.9996。结果表明龙脑在0.040416~0.80832 mg/mL之间呈良好的线性关系(图7)。
4.3.3. 精密度试验
精密度实验结果见表15,其RSD为1.25%,说明仪器有着良好的精密度。
4.3.4. 稳定性试验
稳定性试验结果见表16,其RSD为2.09%,表明艾纳香纳米乳在10 h内稳定。
4.3.5. 重复性试验
重复性试验结果见表17,其RSD为1.06%,表明本方法有着良好的重复性。
4.3.6. 加样回收试验
加样回收试验结果见表18,平均加样回收率为96.14%,RSD为0.70%,结果符合要求。
4.3.7. 含量测定
样品含量测定结果见表19。
5. 结论
艾纳香是贵州苗药之一,有悠久的应用历史,中药艾片及民族药艾纳香油也源于艾纳香。艾纳香含有多种化学成分,包括挥发油、黄酮类、倍半萜类、苯丙素等,具有抗菌、抗炎、镇痛、抗癌,抗氧化等多种药理活性,目前已被加工成多种产品,其加工品具有不同疗效 [15] 。挥发油是艾纳香主要成分之一,是其独特的芳香气味来源,也使具有治疗烫伤的作用,在化妆品界被广泛使用,创造了不少的社会经济效益 [16] 。此外,研究表明艾纳香挥发油具有较好的抗炎止痛的功效,能有效抑制细胞炎症因子如白细胞介素1β、肿瘤坏死因子α、白细胞介素6和炎症介质前列腺素E2、白三烯B4、一氧化氮的释放和表达 [17] [18] 。因此,充分发挥艾纳香挥发油抗炎的作用对于促进其开发利用有一定意义。
纳米乳作为一种新剂型,经皮给药可以延缓药物释放、提高药物透皮速率,提高生物利用度,作为按摩介质十分合适。使用具有抗炎镇痛的民族药艾纳香的纳米乳作为介质治疗类风湿性关节炎,其毒副作用低,疗效好,具有广阔的市场前景,值得深入研究。
因此,本实验从艾纳香的抗炎活性成分出发,将其制备为纳米乳,作为介质,从而治疗类风湿性关节炎。本实验设计了诸多单因素考察和三因素三水平正交试验以优化处方,确定艾纳香纳米乳最佳处方为:吐温-80 4.00 g,正丁醇1.00 g,艾纳香油0.21 g,艾纳香水提溶液5.21 mL。所制备的艾纳香纳米乳为浅棕色澄清透明液体,结构为O/W型,pH值为6.69左右,平均粒径为11.37 nm,分散指数为0.23,在微观状态下呈圆球形且分布均匀。离心后未出现破乳、分层等现象,具有较好的稀释稳定性,并且其在4℃环境中放置28天是相对稳定的,因此结果表明该艾纳香纳米乳质量良好。利用气相色谱法测定艾纳香纳米乳中左旋龙脑的含量,在0.040416~0.80832 mg/mL之间呈良好的线性关系,精密度,稳定性,重复性,加样回收率等符合相关要求,最后测得艾纳香纳米乳中左旋龙脑的含量为0.8487 mg/g。
本实验以艾纳香油为油相,艾纳香水提溶液为水相制备的艾纳香纳米乳外观透明,质量良好,稳定性好。但只对其中左旋龙脑进行含量测定,后续研究可从其他抗炎成分出发进行研究,同时也可从体外透皮,体内药效等方面进行研究,有利于促进其开发。
基金项目
1. 国家自然科学基金,项目编号:82260770;2. 贵州省特色功能食品与中药制剂开发攻关大平台黔教合,项目编号:KY字[2020]006;3. 贵州中医药大学药用高分子材料研究中心,项目编号:贵中医党办发[2019]70;4. 贵州中医药大学博士启动基金,项目编号:贵中医博士启动[2021]14;5. 贵州省国内一流学科建设项目,项目编号:GNYL[2017]008;6. 贵州省药物新剂型新工艺科技创新人才团队项目,项目编号:黔科合平台人才[2017]5655。
NOTES
*通讯作者。