1. 引言
患者男,33岁,因“胸痛3 d”于2021年12月20日收住大理大学第一附属医院心内科。3天前无明显诱因突发心前区绞痛伴后背放射痛、大汗,持续未缓解,至当地医院查N末端脑钠肽前体、肌红蛋白、肌钙蛋白均升高,遂转至我院急诊科,查心电图示:下壁及正后壁导联ST段抬高(图1),拟诊“下壁及正后壁心肌梗死”收住心内科。既往史:2021年11月26日患者因“左下肢肿胀疼痛3 d”于我院血管外科住院,查狼疮抗凝物阳性,抗心磷脂抗体、抗β2糖蛋白I抗体高度阳性;诊断“1、左下肢深静脉血栓形成;2、抗磷脂综合征待观”,予“那屈肝素钙”抗凝,出院后口服利伐沙班15 mg (每日2次),2 w后改为20 mg (每日1次)。否认高血压、糖尿病病史;吸烟10余年,每天20支。否认结缔组织病、家族遗传史。入院查体:血压160/101 mmHg (1 mmHg = 0.133 kPa),体质量指数(BMI) 31.9 kg/m2。神清,颈静脉无充盈。双肺可闻及少许湿罗音,心界不大,心率100次/分,律齐,心音低钝,未闻及病理性杂音,无心包摩擦音,余查体未见异常。

Figure 1. 18-lead electrocardiogram of the patient on admission (pathological Q-wave and ST-segment elevation in leads II, III, aVF, V7, V8 and V9, indicating inferior and positive posterior myocardial infarction)
图1. 患者入院时18导联心电图(II、III、aVF、V7、V8、V9导联病理性Q波、ST段抬高,提示下壁及正后壁心肌梗死)
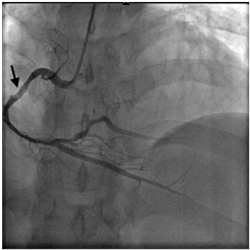
急诊行冠状动脉造影提示:冠脉分布呈右优势型,左主干、前降支及对角支、左回旋支及钝缘支均未见异常,右冠中远段及左室后支近段可见血栓影,左室后支远段及后降支血流TIMI血流3级(图2)。
 (a)
(a) 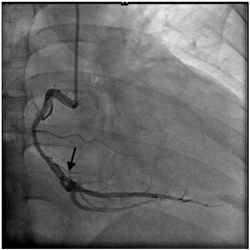 (b)
(b)
Figure 2. Coronary angiography results of the patient: A Thrombus in the middle and distal segment of the right coronary artery (arrow) in the proximal segment of the posterior left ventricular branch (arrow)
图2. 患者冠状动脉造影结果:(a)右冠脉中远段(箭头所示);(b) 左室后支近段可见血栓(箭头所示)
入院后完善检查:血常规:白细胞14.48 × 109/L (4~10 ×109/L),中性粒细胞绝对值11.28 ×109/L (2~7.5 ×109/L),余无明显异常。肝功:总胆红素36.3 umol/l (5.1~19.0 umol/l),直接胆红素13.1 umol/l (0~5.1 umol/l),间接胆红素23.2 umol/l (5.2~13.9 umol/l)。C反应蛋白85.5 mg/L (<10.0 mg/L)。心肌酶谱:肌酸激酶同工酶 > 80 ng/ml (0~4.3 ng/ml),肌红蛋白255 ng/ml (0~107 ng/ml),肌钙蛋白I20.9 ng/ml (0~0.4 ng/ml),BNP 265 pg/ml (<100 pg/ml),D-二聚体924 ng/ml (0~100 ng/ml)。抗磷脂抗体:抗心磷脂总抗体 > 400 RU/mL (0~20 RU/mL),抗心磷脂IgG抗体 > 400 RU/mL (0~20 RU/mL),抗β2糖蛋白总抗体 > 400 RU/mL (0~20 RU/mL),抗β2糖蛋白IgG抗体 > 400 RU/mL (0~20 RU/mL)。抗核抗体、抗nRNP/SM、抗Sm抗体、抗SSA抗体、抗RO-52抗体、抗SSB抗体、抗Scl-70抗体、、抗JO-1抗体、抗着丝点蛋白B抗体、抗PCNA抗体、抗dsDNA抗体、抗核小体抗体、抗组蛋白(H1)抗体、抗核糖体P蛋白抗体、抗AMA-M2、抗中心粒细胞胞浆抗体、抗肾小球基底膜抗体、抗蛋白酶3抗体、抗髓过氧化物酶抗体均阴性。凝血功能:PT 15.2S (10.5-14.5),PT-INR 1.24,APTT 123.2 s (31~44 s),FIB 6.6 g/L (2~4),TT未见异常。心脏彩超:节段性室壁运动减弱。颈部血管彩超:双侧颈总动脉内膜不光滑声像。双下肢血管彩超:1) 左侧髂外、股总静脉血栓形成声像(部分闭塞);2) 右侧股总、股浅、腘、胫前、胫后静脉,左侧股浅、腘、胫后静脉血流缓慢声像(血栓前期改变)。肺动脉CTA:部分肺动脉分支显影浅淡或不显影,肺动脉主干及其主要分支未见明显充盈缺损。睡眠呼吸检测:符合重度阻塞性睡眠呼吸暂停;夜间轻度低氧血症。
治疗上予华法林钠2.5 mg (每日1次)抗凝、铝镁匹林片81 mg (每日1次)抗血小板,以及美托洛尔片25 mg (每日2次)、依那普利片10 mg (每日1次)、瑞舒伐他汀钙片10 mg (每日1次)冠心病二级预防。出院后曾至昆明某医院复诊,遵医嘱停华法林,改为利伐沙班15 mg,每日1次。2022年02月患者因“肾周感染”再次于我院治疗,复查双下肢血管彩超正常;抗心磷脂抗体、抗β2糖蛋白1抗体仍高度阳性,请风湿免疫科会诊,诊断为抗磷脂综合征,排外禁忌后予加用羟氯喹0.2 g (每日2次)。后电话随访,患者规律服用上述药物,未再发生血栓栓塞事件。
2. 讨论
冠状动脉非阻塞性心肌梗死(myocardial infarction with non-obstructive coronary arteries, MINOCA)是指临床上诊断为心肌梗死,但冠状动脉造影显示冠状动脉狭窄程度< 50%或冠状动脉完全正常的临床综合征,其在急性心肌梗死的发病率约5%~10% [1]。其病因包括:冠状动脉痉挛、冠状动脉斑块破裂、自发性冠状动脉夹层、冠状动脉血栓、心肌桥、冠状动脉微血管功能障碍、2型心肌梗死以及其他未知的机制 [2]。2016年欧洲心脏病学会发表了MINOCA的定义 [1]。2019年美国心脏并学会采纳了《2018年第四版心肌梗死全球统一定义》 [3] 中对心肌梗的定义发布的《MINOCA诊断和管理科学声明》 [4]。近年来MINOCA开始在临床中引起关注,是目前临床研究热点。
抗磷脂综合征(APS)是一种抗磷脂抗体持续阳性的全身性自身免疫性疾病,临床上以反复发生静动脉或微血管血栓形成、血小板减少症、复发性自然流产等症状为表现 [5]。抗磷脂抗体主要包括狼疮抗凝物(LAC)、抗心磷脂抗体(aCL)、抗β2糖蛋白(β2GPI)抗体。APS通常分为原发性APS和继发性APS,后者多继发于系统性红斑狼疮、干燥综合征等结缔组织病。APS是引起血液高凝状态的常见原因,可致冠状动脉粥样硬化及冠状动脉血栓形成,约2.8%~5.5%的APS患者可能因此发生心肌梗死 [6]。有研究 [5] 发现14%的MINOCA患者存在易栓症。因此建议对MINOCA患者,尤其是青年、无冠心病危险因素、既往有血栓栓塞病史的患者,应常规筛查易栓症。
本例患者考虑为APS致MINOCA,主要依据如下:1) 本例患者符合急性心肌梗死的诊断标准,而冠状动脉造影未见明确狭窄,但右冠中远段及左室后支近段可见血栓,符合2019美国心脏病学会有关MINOCA科学声明 [4] 的诊断标准;2) 患者先后因下肢静脉血栓、心肌梗死的血栓栓塞事件就诊,入院肺动脉CTA显示部分肺动脉分支不显影,不能排外肺动脉栓塞,完善LAC阳性,>12 w后复查aCL、抗β2GPI抗体仍持续高度阳性,符合2006年悉尼修订APS分类诊断标准 [7];3) 患者青年男性,早发心肌梗死,考虑为APS的血液高凝状态致冠脉血栓形成。如行经心脏MRI检查,可进一步明确有无微血管病变;完善血管内超声、光学相干断层扫面可识别冠状动脉造影不能发现的冠状动脉粥样硬化,更能提供有利证据。
既往临床实践及多项研究均已证实,APS患者血栓再发风险显著增高,其中“三阳”(即aCL、抗β2GP I抗体、LAC三种磷脂抗体均阳性)患者尤为突出 [8]。简化整体抗磷脂综合征评分(aGAPSS)可较好的反映APS患者血栓再发风险 [9],该患者aGAPSS评分 ≥ 10分为血栓再发高危人群。且三种抗磷脂抗体均为阳性,根据2019年EULAR关于成人血栓性APS的治疗推荐意见汇总 [10],三磷脂抗体阳性的动静脉血栓事件者,不推荐应用利伐沙班,建议长期口服华法林抗凝治疗,根据个体出血和血栓复发事件风险设定为INR2.0~3.0或3.0~4.0,亦可考虑华法林标准抗凝联合阿司匹林。本例在下肢静脉血栓首次就诊时予院外口服利伐沙班15 mg,每日2次抗凝。2 w时患者在此基础上发生仍发生了冠脉血栓,因此在我院心内科改为华法林联合铝镁匹林片治疗。但患者出院后未规律复查凝血功能,外院复查时遵医嘱,华法林改为利伐沙班抗凝治疗。然而现有证据表明,在APS患者中新型口服抗凝剂在预防血栓复发方面不如华法林有效 [11]。患者同时合并吸烟、肥胖、高血压、重度阻塞性睡眠呼吸暂停的血栓高危因素 [12] [13],血栓事件再发风险亦显著增加。但患者依从性差,考虑到利伐沙班无需常规检测凝血指标,予继续利伐沙班联合铝镁匹林预防血栓,并加用羟氯喹。但目前免疫抑制剂疗效不明确,一般不常规使用。
此外,本例患者在未用肝素的情况下,APTT显著延长,PT未见明显异常,且无皮肤粘膜等出血表现。APTT延长混合血浆纠正试验可用于鉴别凝血筛选试验中APTT延长的原因——凝血因子缺乏或存在凝血抑制物 [14]。LAC可作用于凝血酶原复合物(Xa、Va、Ca2+及磷脂)和Tenase复合体(IXa、VIIIa、Ca2+及磷脂),导致磷脂依赖的凝血试验时间(如APTT、DRVVT、SCT等)延长 [15]。本例患者虽未作APTT纠正实验,但结合患者血浆中存在LAC,考虑凝血抑制物干扰APTT实验,导致结果升高。
目前对于MINOCA的治疗尚无统一意见。冠心病二级预防主要针对冠脉斑块的基础上继发血栓形成的过程 [4]。然而,在MINOCA患者中,动脉粥样硬化负荷小。冠心病二级预防在MINOCA患者的疗效不确定,提倡积极寻找病因,个体化治疗。本例患者存在原发性APS这一危险因素,因此应长期口服抗凝药物治疗。
3. 结论
综上,对于MINOCA患者,应积极寻找危险因素及病因,尤其是年轻患者反复出现血管栓塞事件,应警惕APS,筛查抗磷脂抗体、结缔组织疾病。对于血栓性APS高危患者长期服用华法林患者应规律监测INR值,以便及时调整抗凝治疗,预防多器官血栓形成,以期减少出血及栓塞等并发症。
NOTES
*通讯作者。