1. 引言
生物土壤结皮(Biological Soil Crust, BSCs)是由藻类、地衣、藓类等隐花植物及土壤中的微生物和相关的其他生物体与土壤表层颗粒等非生物体胶结形成的十分复杂的复合体,是荒漠生态系统组成和地表景观的重要特征 [1] [2] 。大多数荒漠生态系统是由非生物因素调控和胁迫的系统,尤其因受水分的限制,地表不可能支撑大面积、相对均一而连续分布的维管束植物群落;植物群落斑块状的分布为BSCs的拓殖和覆盖提供了空间和适宜的生态位,使BSCs的覆盖在干旱区占活体覆盖面积的40% [3] 。BSCs在不同生物气候区的荒漠景观过程,土壤生态、水文、生物过程,地球化学循环过程,以及干旱、半干旱地区的生态修复过程中发挥着重要作用 [4] [5] 。
BSCs在荒漠地区碳循环中所起的作用得到了研究者们的广泛的认可 [3] [4] [5] 。Wolfgang等人 [6] 对全球范围内BSC覆盖地区净碳固定量(光合固碳量–呼吸碳释放量)进行了估算,结果表明,BSCs每年能够固定3.9 P g C y−1 (2.1~7.4 P g C y−1),相当于陆生植物净初生产力的7% (56 P g C y−1);BSCs生物体中的碳含量为4.9 P g (3.0~8.2 P g),相当于陆生植物碳含量的1% (470~650 P g)。碳周转率方面,BSCs的周转率约为1.2 年,远远低于陆生植物的10年。Elbert等人 [7] 同样对全球范围内BSCs覆盖地区净碳固定量(光合固碳量–呼吸碳释放量)进行了估算,结果表明,BSCs每年能够固定3.6 P g C y−1,相当于陆生植物净初生产力的6%;BSCs生物体中的碳含量为10 P g,相当于陆生植物碳含量的2%。在Iberian Peninsula (40˚02'N~3˚37'W)干旱、半干旱地区,Castillo-Monroy等 [9] 对不同盖度BSC覆盖条件下,土壤碳释放特征进行了研究,结果表明,BSCs覆盖土壤每年释放240.4~322.6 g C m−2∙y−1;在这一生态系统中,BSCs的碳释放量占到碳释放总量的42% (植被占37%)。因此,BSCs作为干旱、半干旱地区碳循环的重要参与者和主要贡献者已得到广泛共识 [4] [5] [8] [9] 。
尽管,BSCs在荒漠地区碳循环中起着重要的作用,与生态要求的强调BSCs光合碳固定作用研究相比较,其在碳释放方面的研究却被长期忽视 [4] [10] [11] 。而目前已有的研究多集中在热带荒漠,对温带荒漠的研究鲜见报道。土壤呼吸温度敏感性一般用Q10表示,即温度每升高10℃,呼吸速率增加的倍数。从区域到全球尺度,多数生态系统模型(如Roth-C、PnET、TEM等)采用Q10函数来估算温度对土壤异养呼吸影响的量,但Q10常被视为常数2 [12] 。目前,仍鲜见BSCs温度敏感性及其影响因子的相关报道 [4] 。因此,加强BSCs碳释放对碳循环贡献和影响的研究是全面解析荒漠地区碳循环不可或缺的重要环节,是全面认知我国温度荒漠生态系统碳循环的重要基础和相关研究的重要补充,以及进一步研究荒漠生态系统如何适应和响应全球变化机制、提出区域科学对策的重要前提。
2. 研究方法
2.1. 研究区概况
中国科学院沙坡头沙漠研究试验站地处宁夏回族自治区,位于腾格里沙漠东南缘(37˚32'N,105˚02'E,海拔1340 m)。1月的平均气温为−6.9℃,7月为
24.3 ℃
。年均降水量仅为180 mm,降雨主要集中在5~9月,降雨量小于2 mm的降雨占总降雨的80%以上,年潜在蒸发量高达2800 mm。土壤基质疏松、贫瘠,属于典型的灰钙土、风蚀土壤。土壤稳定含水量介于3%~4%。地下水埋深80 m,不能为植物直接利用,降雨是该区植物生长的唯一水分来源。天然植被主要包括花棒(Hedysarum scoparium)和沙米(Agriophyllum squarrosum),其盖度仅1%。
始建于1956年的沙坡头人工固沙植被区经过50余年的演化,已由原来的以流动沙丘为主的景观演变成了复杂的人工—天然的荒漠生态系统,其中最为显著的变化是BSC 的拓殖与发育。目前,在1956年始建的植被区,BSC盖度已经超过80%,盖度较大且发育较好的结皮类型有藻类和藓类结皮 [4] [5] [13] 。
2.2. 试验方法
2013年10月,在腾格里沙漠东南缘沙坡头地区1964年始建的人工固沙植被区选择发育良好的藻类结皮、藓类结皮及混生(藻类、地衣和藓类等隐花植物混生)结皮(本研究中将某优势种盖度大于70%的定义为该类型的结皮)。为避免微地形环境和植被对结皮发育的影响,取样点选择在植被间的地势平坦的开阔地,用内径10.4 cm、高20 cm的PVC管取原状土。将采来的BSCs样品放置在阴凉通风处,待到样品重量恒定不变时开始试验。
在3个温度梯度(15℃、25℃和35℃)和7个水分梯度(3%、5%、10%、15%、20%、25%和30%质量含水量)测定土壤呼吸速率。采用Li-6400-09土壤呼吸室(Li-COR, INC, USA)测定土壤呼吸速率。水分添加采用喷壶喷洒的方法,均匀的喷洒在样品表面;每个水分梯度在设定的温度条件下培养2 h,开始土壤呼吸的测定。试验在人工气候室中进行,每处理设6次重复。
2.3. 数据分析
数据分析和图表绘制分别在SPSS16.0和Origin8.0中进行。
3. 结果与分析
3.1. 温度和水分对不同类型BSC呼吸速率的影响
图1描述了3个土壤温度和7个水分梯度条件下,不同类型BSC和流沙呼吸速率变化特征。在相同水分条件下,BSCs和流沙呼吸速率随着温度的增加而增加,35℃时BSCs和流沙呼吸速率达到最大值。而在相同温度条件下,不同类型BSCs和流沙呼吸速率随着水分的变化表现出不同的变化趋势。藓类结皮呼吸速率表现为随着水分增加而逐渐增加的趋势,15℃和35℃条件下,最大值均出现在25%含水量条件为1.33和3.38 μmol CO2 m−2∙s−1;25℃条件下,最大值出现在20%含水量条件为1.65 μmol CO2 m−2∙s−1。藻类结皮呼吸速率在15℃和25℃条件下表现为随着水分增加先急剧增加而后逐渐下降的趋势,最大值均
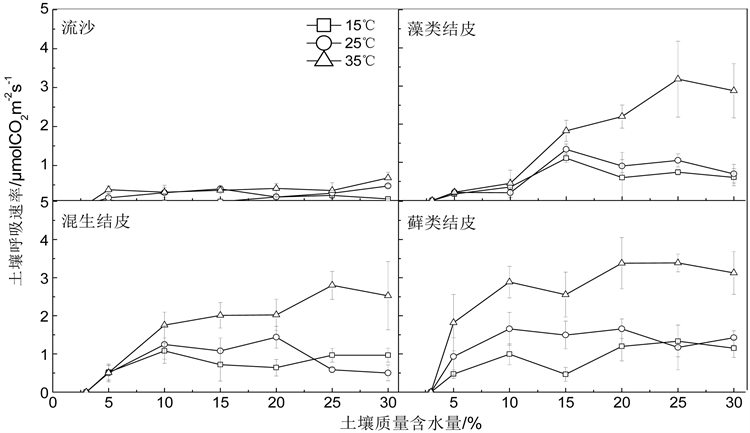
Figure 1. Effects of soil temperature and soil water content on BSC respiration rate (Mean ± SE)
图1. 土壤温度和水分对BSC呼吸速率(Mean ± SE)的影响
出现在8%含水量条件为1.10和1.34 μmol CO2 m−2∙s−1;而在35℃条件下,呼吸速率表现为随着水分增加而逐渐增加的趋势,最大值出现在20%含水量条件下为3.18 μmol CO2 m−2∙s−1。混生结皮呼吸速率在15℃条件下表现出随着水分增加先急剧增加而后逐渐下降的趋势,最大值均出现在6%含水量条件,为1.07 μmol CO2 m−2∙s−1;而在25℃和35℃条件下,呼吸速率表现为随着水分增加而逐渐增加的趋势,最大值出现在15%和20%含水量条件下为1.44和2.80 μmol CO2 m−2∙s−1。流沙呼吸速率表现出随着水分增加而逐渐增加的趋势,15℃条件下,最大值出现在15%含水量条件下,为0.23 μmol CO2 m−2∙s−1;而在25℃和35℃条件下,最大值均出现在17%含水量条件下分别为0.47和0.68 μmol CO2 m−2∙s−1。
3.2. 不同温度和水分条件下不同类型BSC呼吸速率差异性分析
对3个温度梯度下不同类型BSC间进行差异性分析表明,藓类结皮呼吸速率在3个温度梯度下均显著高于其他类型的BSC (P < 0.05),而流沙呼吸速率在3个温度梯度下均显著低于其他类型的BSC (P < 0.05,表1)。对7个水分梯度不同类型BSC间进行差异性分析表明,除了第1和6水分条件下,藓类结皮呼吸速率均显著高于其他类型的BSC (P < 0.05);3、4和5水分条件下,流沙呼吸速率均显著低于BSC的呼吸速率(P < 0.05,表2)。
不同温度和水分条件下对相同类型BSC呼吸速率进行差异性分析表明,在相同温度(15℃、25℃和35℃)条件下,水分含量大于10%时,藓类结皮呼吸速率显著高于其他含水量时的呼吸速率(P < 0.05)。15℃和25℃、含水量为8%时,藻类结皮呼吸速率显著高于其他含水量时的呼吸速率;35℃、含水量为20%~25%时,呼吸速率显著高于其他含水量时的呼吸速率。15℃和25℃、含水量为5%~16%时,混生结皮呼吸速率显著高于其他含水量时的呼吸速率;35℃、含水量为20%~25%时,呼吸速率显著高于其他含水量时的呼吸速率。5℃和25℃、含水量为1%时,流沙呼吸速率显著低于其他含水量时的土壤呼吸速率;35℃、含水量为16%时,土壤呼吸速率显著高于其他含水量时的土壤呼吸速率(P < 0.05) (表3)。

Table 1. Significant analysis of BSC dark respiration rate in the same soil temperature
表1. 相同土壤温度条件下不同类型BSC呼吸速率差异显著性分析
注:表中相同小写字母表示差异不显著P > 0.05水平。

Table 2. Significant analysis of BSC dark respiration rate in the same soil water content
表2. 相同土壤水分条件下不同类型BSC呼吸速率差异显著性分析
注:表中相同小写字母表示差异不显著P > 0.05水平。

Table 3. Significant analysis of BSC dark respiration rate in the different soil temperature and soil water content
表3. 不同温度、水分条件下相同类型BSC呼吸速率差异显著性分析
注:表中小写和大写字母分别表示相同类型BSC相同温度不同水分(横向)和相同水分不同温度(纵向)条件下差异显著性分析;相同小写和大写字母表示差异不显著P > 0.05水平。
在相同水分梯度条件下,藓类结皮,35℃条件下的呼吸速率显著高于15℃和25℃条件下的呼吸速率;10%~15%含水量,25℃条件下的呼吸速率显著高于15℃的呼吸速率。藻类结皮,当含水量大于7%时,35℃条件下的呼吸速率显著高于15℃和25℃条件下的呼吸速率;含水量在10%和20%时,25℃条件下的呼吸速率显著高于15℃条件下的呼吸速率。混生结皮,当含水量大于5%时,35℃条件下的呼吸速率显著高于15℃和25℃条件下的呼吸速率;含水量在15%时,25℃条件下的呼吸速率显著高于15℃条件下的呼吸速率。流沙,当含水量大于10%时,35℃条件下的呼吸速率显著高于15℃和25℃条件下的呼吸速率;水分含量在5%和16%时,25℃条件下的呼吸速率显著高于15℃条件下的呼吸速率。
3.3. 不同温度和水分条件下不同类型BSC呼吸速率差异性分析
对模拟试验结果用一般线形模型(General Linear Model, GLM)进行多因素方差分析。结果表明,BSC呼吸速率在BSC类型、土壤温度和土壤含水量均存在显著差异(P < 0.01),它们之间的二维和三维互作也存在着显著差异(P < 0.01)。整个一般线形模型结果可以解释88.2%的差异(表4)。
3.4. 不同类型BSC温度敏感性(Q10)
分别在15℃~25℃和25℃~35℃ 2个温度梯度、7个水分梯度条件下计算了不同类型BSC的Q10。结果表明,藓类结皮Q10在1.40~3.17间,藻类结皮在0.81~3.07间,混生结皮在0.55~3.84间,流沙在1.19~2.16间,各类型BSC和流沙25℃~35℃的Q10大于15℃~25℃。随着土壤水分含量的不断增加,藓类结皮Q10值不断增加;藻类和混生结皮,表现出先增加后降低的特征,当土壤含水量大于15%时,Q10迅速降低。根据平均值计算,Q10的大小顺序为藓类结皮 > 混生结皮 > 藻类结皮 > 流沙(图2)。

Figure 2. Q10 values of different BSC types (Mean ± SE)
图2. 不同类型BSC温度敏感性(Q10)

Table 4. Three way-ANOVA analyses on effects of BSC types, soil temperature and soil water content on BSC dark respiration rate
表4. BSC类型(BSC)、土壤温度(ST)和土壤含水量(SWC)对BSC呼吸速率影响的多因素方差分析
注:R2 = 0.882 (校正R2 = 0.851)。
4. 讨论
4.1. 影响BSCs碳释放的因素分析
4.1.1. BSC类型对土壤呼吸碳释放量的影响
本研究结果表明,演替后期的藓类结皮碳释放量高于演替初期的藻类结皮,即藓类结皮 > 混生结皮 > 藻类结皮 > 流沙,与Belnap and Lange [3] 和Evans and Lange [10] 研究结果相似。Grote等人 [11] 分别在野外和试验室条件下证明了,处于演替后期的深色结皮暗呼吸速率大于演替初期浅色结皮的暗呼吸速率。综上所述,处于演替后期的BSCs是碳释放的主要贡献者。BSC有机体的生物量差异是造成其碳释放差异的主要原因。通常BSCs有机体的生物量用叶绿素a + b表示,Li等人 [13] 对该试验区BSCs叶绿素a + b进行了测定,结果表明藓类结皮,藻类结皮和混生结皮的叶绿素a + b含量分别为7.34、3.80和5.45 μg C m−2,即藓类结皮 > 混生结皮 > 藻类结皮,叶绿素a + b含量随着演替阶段的推进而不断的增加。综上所述,BSCs有机体的生物量影响BSC的碳释放量。
4.1.2. 水分对土壤呼吸碳释放量的影响
土壤水分是影响干旱、半干旱地区土壤碳释放的重要因素 [14] [15] 。在干旱、半干旱地区,土壤水分主要来源于降雨。土壤水分过多或不足均会抑制土壤呼吸,土壤呼吸的最大速率出现在土壤水分含量适中时 [16] 。在农田和草原上对强降雨的研究指出,强降雨迅速降低或抑制了土壤呼吸。张红星等人研究发现 [17] ,土壤呼吸在强降雨中和雨后分别下降了33%和15%。一些来自室内模拟的研究同样表明,强降雨显著抑制了土壤呼吸 [18] 。从以上的大量研究可以看出,土壤含水量是影响土壤呼吸的重要因素,雨量和强度较大的降雨使得土壤表层的含水量增加,进而影响土壤碳的释放。大量研究表明,中等水平的自然降雨量能够促进土壤呼吸 [14] ,于此同时,大量针对不同生态系统的模拟试验也取得了和野外试验类似的结果 [19] 。本研究结果表明,水分含量较高的条件下,藻类和混生结皮的呼吸速率受到了明显抑制,而对藓类结皮的呼吸速率影响不明显。水分取代了土壤中CO2占据的位置的同时也使土壤的通透性变差,CO2在土壤中的扩散阻力因此增大,是导致土壤CO2排放量减少的主要原因 [20] 。藻类结皮和藓类结皮对水分的拦截能力不同。藻类在生长季节能够分泌大量胞外多聚糖,随这种多糖物质浓度的提高,土壤持水性能增大,土壤水分蒸发速率降低,水分在土壤中的运动速率降低,这使得降水过后水分大量集中在土壤表层。藓类植物叶子的季节变化也会影响土壤水文特性,许多藓类植物长有一定长度的尖梢,可以把水分引入植物体中间去,水分通过植物体向土壤深层入渗,降水过后水分不会大量的集中在土壤表层 [13] 。因此,处于演替高级阶段的藓类结皮能够很好地应对短期的极端降雨事件。
4.1.3. 温度对土壤呼吸碳释放量的影响
温度是影响BSC碳释放的重要环境因子。土壤呼吸随土壤温度变化呈现出日变化、季节变化和年际变化特征 [21] 。Castillo-Monroy等人 [9] 和Thomas and Hoon [22] 的研究证明了温度对BSC碳释放的影响,即BSC碳释放量随着温度的变化而变化。本研究结果表明,在相同水分条件下,BSC和流沙呼吸速率也随着温度的增加而增加。
4.2. 温度和水分对BSCs碳释放Q10的影响
4.2.1. 温度对BSCs碳释放Q10的影响
多数研究表明温度显著影响土壤呼吸Q10。Sjögersten 和Wookey对瑞典 Lapland 北部山地苔原土壤和附近山地白桦林土壤研究发现,7℃~12℃温度范围内的Q10值高于2℃~7℃温度范围内的 Q10值 [23] 。Nadelhoffer等对阿拉斯加 North Slope的土壤进室内培养实验,发现温度在3℃~9℃时,Q10约为1;当温度为9℃~15℃时,Q10约为3.1 [24] 。Howard 和 Howard发现英格兰泥炭土壤和渍水灰壤在不同水分条件,0℃~20℃温度范围内,Q10随温度升高而增加 [25] 。对不同季节Q10差异也揭示类似规律性。Lipson等将夏季和冬季取的高山干旱草甸土壤置于0℃和22℃温度下进行室内培养,发现冬季土壤Q10值(2.3)低于夏季土壤Q10值(3.6)。Castillo-Monroy等人 [9] 的研究表明,在相同水分不同温度条件下不同盖度BSCs覆盖土壤的Q10在1.65~1.80之间变化。Jia等 [26] 在5℃~40℃范围内,对腾格里沙漠东南缘3种藓类结皮Q10值进行了测定。研究发现,Q10值随着水分增加而增加。土生对齿藓结皮Q10值为2.23~2.79,刺叶赤藓结皮Q10值为2.08~2.71,真藓结皮Q10值为1.84~2.45。而在相同水分条件下,3种藓类结皮Q10值为土生对齿藓结皮 > 刺叶赤藓结皮 > 真藓结皮。本研究结果表明25℃~35℃条件下的Q10值高于15℃~25℃条件下,即Q10随温度升高而升高,与上述研究结果相似。因此,温度显著影响BSCs呼吸温度敏感性。
4.2.2. 温度对BSCs碳释放Q10的影响
大量研究表明水分影响土壤呼吸Q10 [27] [28] 。对南极洲附近Marion岛屿土壤进行室内培养研究发现,温度在 5℃~20℃间,水分含量在20%~100%间,Q10值与土壤水分含量成正相关关系 [28] 。在亚利桑那州对荒漠土壤的室内培养研究发现,温度在5℃~35℃范围内,土壤水势从−1.5 MPa 增至−0.03 MPa,Q10从2.1增加到3.2 [28] 。Howard 等将英格兰8种土壤类型表层10 cm土壤,在土壤含水量在10%~100%和温度0℃~20℃条件下培养,发现Q10随水分增加而升高 [25] 。张志山 [29] 对腾格里沙漠东南缘人工植被沙区土壤呼吸研究表明,温度对土壤呼吸的影响表现在只改变量的大小,而不引起质的变化。只有在水分充足的条件下,土壤呼吸速率才表现出与气温和地表温度一致的季节和日变化趋势。本研究结果发现,随着土壤水分含量的不断增加,藓类结皮Q10值不断增加;藻类和混生结皮,表现出先增加后降低的特征,当土壤含水量大于15%时,Q10迅速降低,与多数研究结果相似。因此,水分条件显著影响BSCs呼吸温度敏感性。
5. 结论
BSCs类型、水分和温度显著影响BSCs碳释放量。水分含量较高的条件下,藻类和混生结皮的呼吸速率受到了明显抑制,而对藓类结皮的呼吸速率影响不显著。因此,在全球变化大背景条件下,处于演替高级阶段的藓类结皮能够很好地应对短期的极端降雨事件。
基金项目
中国科学院前沿科学重点研究项目(QYZDJ-SSW-SMC011);国家自然基金(41501270和41471434)资助。
NOTES
*通讯作者。