摘要:
本文研究海藻提取物对甘蔗苗期叶片抗氧化酶活性、株高、生物量及叶片SPAD值的影响,为明确海藻提取物缓解甘蔗苗期干旱胁迫提供依据。采用水培方式以粤糖94-128幼苗为研究对象,在10% PEG6000模拟干旱胁迫条件下分别用浓度为0%、0.5%和1% (V/V)的海藻提取物施用于营养液,处理3天后分别测定甘蔗苗期叶片过氧化物酶(POD)、超氧化物歧化酶(SOD)和过氧化氢酶(CAT)活性以及丙二醛(MDA)含量,处理10天后分别测定株高、生物量鲜重及叶片SPAD值。研究结果表明,在干旱胁迫下施用海藻提取物能提高叶片POD、SOD和CAT等抗氧化酶活性,降低叶片MDA含量,使叶片脱水速率得到显著降低,相对含水量得到显著提高,电导率显著下降,增加甘蔗株高和生物量,显著提高叶片SPAD值(p < 0.05)。因此,海藻提取物有望成为一种新的甘蔗抗旱调节剂。
Abstract:
A hydroponic experiment was conducted to explore the effects of various rates of seaweed extracts (prepared from brown alga) on sugarcane growth and physiological response under stimulated drought stress. Yuetang 94-128 was selected based on seedling growth under drought and were planted in pots containing 10 liter of Hoagland solution. The seedlings were subjected to drought levels using 0% or 10% PEG6000 mixed with Hoagland solution. Three seaweed extract treatments consisting of 0%, 0.5%, and 1% (V/V) of the seaweed extract level in full strength Hoagland solution were applied. The activity of peroxidase (POD), superoxide dismutase (SOD) and catalase (CAT), the content of MDA and electric conductivity (EC) of leaves were measured after 3 days with treatments; the leaf dehydration rate (LDR), the relative water content (RWC), plant height and fresh weight were measured after 10 days with treatments. The results showed that the antioxidant enzymes activity in sugarcane leaves of POD, SOD and CAT were improved, the MDA content, the electric conductivity and the leaf dehydration rate were significantly decreased, while the relative water content, plant height, biomass, leaf SPAD value were greatly increased with the application of seaweed extract under drought stress (p < 0.05), which implied that seaweed extract has a potential for drought-resistant modulation.
1. 引言
甘蔗是我国最重要的糖料作物,既对蔗区农业经济和农民收入提供了有效支撑,同时也为满足我国食糖需求量提供了保障。但甘蔗生产上常年面临着严重影响甘蔗产量和品质的非生物因素——干旱 [1] 。甘蔗生物量大,植株体含水量高达70%,整个生育期对水分的需求量很大,因此缺水干旱对甘蔗生长极为不利。近年来干旱灾害频发,尤其是季节性干旱严重影响甘蔗产量和品质,致使甘蔗农业和制糖工业生产受到严重的阻碍,造成了巨大的经济损失 [2] 。甘蔗抗旱性的研究日趋受到国内外研究人员的重视。海藻提取物是从海藻中提取的一类具有促进作物生长、提高作物抗逆性的生物刺激素,含有钙、铁、镁、锌等矿质营养元素,含有褐藻糖胶、木聚糖、葡聚糖等海藻多糖,以及糖醇、氨基酸、维生素、甜菜碱以及酚类化合物等,此外,还含有生长素、细胞激动素、赤霉素、脱落酸等天然激素类物质 [3] ,从20世纪90年代开始其广泛在农业领域应用 [4] [5] [6] [7] 。海藻提取物既可单独施用,也可与化学肥料配施,它不仅能改善土壤状况 [8] [9] ,提高肥料的利用效率 [10] ,促进植物生长发育 [11] [12] [13] ,还可以提高作物的抗逆性 [14] [15] [16] 。在其施用量很少的情况下就能发挥很明显的作用,目前在多种作物上研究应用表明其对于提高作物抗旱性效果显著,如番茄 [17] 、小麦 [18] 、烟草 [19] 、黄瓜 [20] 和大豆 [21] 等,但甘蔗上未见其应用相关研究报道。鉴于海藻提取物在其他作物上的抗旱效果显著,我们尝试将其在甘蔗上展开应用研究。以期为海藻提取物在甘蔗农业生产上进行应用提供理论基础,对甘蔗产业的可持续性发展具有非常重要的理论和现实意义。
2. 材料与方法
2.1. 供试材料准备
本试验所用海藻提取物为华南农业大学资源环境学院根层调控实验室提供的棕褐色液态样品,其海藻酸含量15%,pH7.0。供试甘蔗品种为粤糖94-128。甘蔗在日光温室内培养,将甘蔗砍成单芽茎段,挑选好芽茎段,将茎段铺在育苗盘的石英砂上再覆盖一层石英砂进行育苗。待出苗后长到4~5片叶时移栽到纯净水中培养1周后转入1/2霍格兰营养液中培养2周,再转入霍格兰营养液培养2周后进行试验处理。采用聚乙二醇(PEG6000)加入营养液作为模拟干旱环境,根据之前的试验结果选择10%PEG浓度作为干旱胁迫 [22] 。
2.2. 试验处理
试验设置6个处理:1) CK:不胁迫,不施用海藻提取物;2) SE1:不胁迫,海藻提取物稀释100倍,即海藻提取物占营养液体积比为1.0%;3) SE2:不胁迫,海藻提取物稀释200倍,即海藻提取物占营养液体积比为0.5%;H300;4) PEG:10% PEG胁迫处理,每1 L营养液加入PEG6000 (聚乙二醇) 100 g,不施用海藻提取物;5) PEG + SE1:10% PEG胁迫,海藻提取物稀释100倍,海藻提取物占营养液体积比为1.0%;6) PEG + SE2:10%PEG胁迫,海藻提取物稀释200倍,海藻提取物占营养液体积比为0.5%。每个处理移栽6株幼苗作为6次重复,其中3株用于生理指标测定,3株用于生物量相关指标分析。
2.3. 测定指标及方法
处理3天后取3株植株正1叶进行叶片抗氧化酶、电导率、等生理指标分析,取正2叶进行离体脱水速率测定,正3叶用于叶片相对含水量测定。
过氧化物酶(POD)、超氧化物歧化酶(SOD)、过氧化氢酶(CAT)及丙二醛(MDA)含量均采用试剂盒方法测定(购自南京建成生物工程研究所)。
电导率测定方法(EC):称0.5 g叶片剪碎加入25 ml纯水在32℃恒温2 h后用电导率仪测定原电导率,然后在沸水浴中保持20 min后测定总电导率,电导率 = 原电导率/总电导率 × 100% [23] 。
离体叶片脱水速率(LDR)测定方法:取一片叶片称量脱水前鲜重W1,将其室温放置12 h后再次称重W2,离体叶片脱水速率 = (脱水前鲜重W1 − 脱水后鲜重W2)/脱水时间(12小时) [23] 。
叶片相对含水量(RWC)采用饱和称量法:选取正3叶片将其摘下后迅速称其鲜质量(Mf),用蒸馏水浸泡4 h后擦干测定叶片饱和质量(Mt),然后于105℃下杀青30 min后,在70℃下烘干至恒量,测定叶片干质量(Md)。按公式
计算叶片相对含水量 [23] 。
剩余3株甘蔗于处理10 d后收获,收获时测量正2叶片SPAD值、植株株高和鲜重生物量。叶片SPAD值用SPAD502仪测量,直尺测量株高,擦干根系水分后称取植株鲜重。
所有数据通过Excel整理收集,采用SPSS19.0进行统计分析,方差分析采用邓肯比较。
3. 结果与分析
3.1. 不同处理对甘蔗幼苗叶片抗氧化酶活性的影响
根据表1结果所示,在PEG模拟干旱胁迫下,SOD、POD和CAT含量显著低于正常对照处理(CK),说明叶片受到干旱胁迫后抗氧化酶活性发生改变。正常处理下施用海藻提取物处理(SE1/SE2)的SOD酶活性显著高于对照处理,而POD和CAT与对照差异不显著,三种酶活性在SE1与SE2之间差异不显著。干旱胁迫下加入不同浓度海藻提取物的两个处理的SOD、POD和CAT含量均显著高于PEG胁迫处理,

Table 1. Effects of different treatments on antioxidant enzyme activity of sugarcane leaves
表1. 不同处理对甘蔗幼苗叶片抗氧化酶活性的影响
注:每列数字后字母不同则表示存在5%显著差异。Note: The different letter in a line means significant at 5%.
且与正常对照处理无显著差异,而两个不同浓度的海藻提取物处理(SE1/SE2)之间并无显著差异。说明在干旱胁迫下施用0.5%~1.0%的海藻提取物能提高叶片抗氧化酶活性,使其恢复到正常水平。
3.2. 不同处理对甘蔗幼苗叶片MDA含量的影响
如图1所示,干旱胁迫下,甘蔗幼苗叶片MDA含量显著高于正常对照CK处理,说明蔗叶受到干旱胁迫而累积了大量的MDA,是正常对照处理的两倍之多。非干旱胁迫下施用海藻提取物处理MDA含量相比正常对照并无显著差异。在干旱胁迫下,施用海藻提取物处理的MDA含量相比不施用海藻提取物处理显著下降,但仍高于正常对照处理,说明干旱胁迫下施用海藻提取物对于降低叶片MDA含量具有较好的作用,但不能完全清除干旱造成的MDA积累。
3.3. 不同处理对甘蔗幼苗叶片水分及质膜透性的影响
结果如表2所示,在干旱胁迫下,甘蔗幼苗离体叶片脱水速率显著高于正常对照CK,达到其两倍之多。叶片相对含水率则相比正常处理显著下降,同时电导率显著增加,这些结果说明干旱胁迫导致甘蔗脱水速度加快,含水量下降,细胞质膜透性增加。非干旱胁迫下施用海藻提取物对于3个指标没有显著影响。而干旱胁迫下加入海藻提取物处理相比不施用海藻提取物处理可以使叶片脱水速率得到显著降低,相对含水量也得到显著提高,电导率显著下降,但这3个指标仍未恢复到正常对照处理水平。
3.4. 不同处理对甘蔗幼苗株高的影响
从图2的结果可以看出,在处理10天后,干旱胁迫处理的甘蔗幼苗株高显著低于正常对照处理,而干旱胁迫下施用海藻提取物的两个处理甘蔗株高均显著高于PEG胁迫处理,且与对照处理无显著差异;非胁迫下施用海藻提取物处理甘蔗株高相比对照有所增加,但无显著差异。这些结果表明,干旱胁迫抑制了甘蔗生长,施用海藻提取物有利于促进甘蔗生长并一定程度上缓解干旱胁迫对甘蔗株高的不利影响。
3.5. 不同处理对甘蔗幼苗生物量鲜重的影响
从图3可以看出,在处理10天后,PEG胁迫处理的甘蔗幼苗鲜重显著低于正常对照及其他所有处理,其中SE1和SE2两个非胁迫下海藻提取物处理与正常对照处理之间无显著差异,干旱胁迫下施用海藻提取物处理(PEG + SE1、PEG + SE2)生物量鲜重比PEG处理有所提高但差异不显著,而且与CK差异也不显著。这些结果表明,干旱胁迫抑制了甘蔗生物量鲜重积累,施用海藻提取物有利于促进甘蔗生长并一定程度上缓解干旱胁迫带来的不利影响。

Figure 1. Effects of different treatments on MDA content of sugarcane leaves. Note: The different letter on the column diagram means significant at 5%
图1. 不同处理对叶片MDA含量的影响。注:柱形图上方小写不同字母表示5%差异显著水平
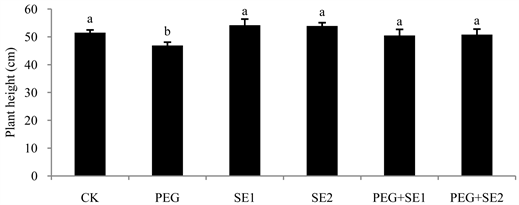
Figure 2. Effects of different treatments on plant height of sugarcane seedlings. Note: The different letter on the column diagram means significant at 5%
图2. 不同处理对甘蔗幼苗株高的影响。注:柱形图上方小写不同字母表示5%差异显著水平

Figure 3. Effects of different treatments on fresh weight of sugarcane seedlings. Note: The different letter on the column diagram means significant at 5%
图3. 不同处理对甘蔗幼苗鲜重的影响。注:柱形图上方小写不同字母表示5%差异显著水平
3.6. 不同处理对甘蔗幼苗叶片SPAD值的影响
从图4可以看出,在处理10天后,PEG胁迫处理的甘蔗幼苗 + 1叶SPAD值显著低于正常对照及其他所有处理,其中PEG + SE1和PEG + SE2两个处理显著高于PEG处理,且与正常对照处理无显著差异。这些结果可以说明,干旱胁迫下甘蔗叶片叶绿素含量降低,而施用海藻提取物的处理可以提高叶绿素含量,从而促进光合作用,有利于增强抗旱性。
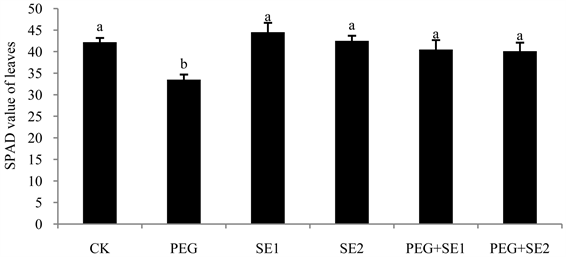
Figure 4. Effects of different treatments on SPAD value of sugarcane leaves. Note: The different letter on the column diagram means significant at 5%
图4. 不同处理对甘蔗叶片SPAD的影响。注:柱形图上方小写不同字母表示5%差异显著水平

Table 2. Effects of different treatments on relative water content and conductivity of sugarcane leaves
表2. 不同处理对甘蔗幼苗叶片水分及电导率的影响
注:每列数字后字母不同则表示存在5%显著差异。Note: The different letter in a line means significant at 5%.
4. 讨论与结论
干旱胁迫是植物最常见的逆境胁迫,也是限制植物生长的重要因素之一。干旱胁迫造成的伤害大多与超氧阴离子自由基等活性氧有关,植物在遇到胁迫时,活性氧物质加速积累,细胞渗透性增加及膜脂过氧化,造成膜系统损伤 [24] 。超氧化物歧化酶(SOD)是动植物体内天然存在的超氧自由基清除因子,它可以把有害的超氧自由基转化为过氧化氢,之后过氧化氢酶(CAT)和过氧化物酶(POD)会立即将过氧化氢分解为水,三种酶形成一个抗氧化系统 [25] [26] [27] [28] 。因此本研究也针对这三种酶在干旱胁迫下甘蔗叶片中的变化情况进行分析,结果表明SOD、POD和CAT三种酶活性在干旱胁迫下均会显著降低,MDA含量显著增加,而施用海藻提取物在会显著提高三种抗氧化酶活性,减少MDA含量,使其恢复到接近正常水平。他人的一些相关研究也表明海藻提取物处理明显提高了干旱胁迫下番茄的抗旱性,主要是提高了番茄叶片可溶性糖含量和SOD 酶活性,叶肉细胞的粘滞性增强,从而降低了自由基对细胞膜的伤害 [17] 。干旱条件下施用海藻糖能减轻干旱胁迫对质膜的伤害,减缓小麦叶片含水量的降低,降低MDA含量 [29] 。干旱胁迫下施加外源褐藻胶寡糖的小麦苗长、根长、鲜重和相对水含量得到显著增加。此外,抗氧化酶活性明显增强,MDA含量显著减少 [18] 。外源海藻糖处理后的烟草幼苗在干旱胁迫下可明显提高叶片的相对含水量和叶绿素的含量,降低电导率和MDA的含量,提高POD、CAT和SOD酶活性 [19] 。这些结果与本研究结果均一致,因此,海藻提取物具有作为抗旱物质开发研究的可能性 [30] 。本研究采用水培+PEG模拟干旱胁迫,与田间试验的环境存在差异,同时本研究只针对苗期进行试验,后期效果如何并不清楚。因此,将进一步在田间种植条件下,对整个生育期进行试验。
本研究结果表明,在干旱胁迫下施用0.5%~1.0%的海藻提取物能提高叶片POD、SOD和CAT等抗氧化酶活性,降低叶片MDA含量,使叶片脱水速率得到显著降低,相对含水量也得到显著提高,电导率显著下降,增加甘蔗株高和生物量,提高叶片SPAD值。因此,在干旱胁迫下,施用海藻提取物有利于缓解干旱胁迫给甘蔗带来的伤害,增强甘蔗苗期抗旱性。
致谢
本试验所用海藻提取物为华南农业大学资源环境学院根层调控实验室耿银银提供,广州甘蔗糖业研究所实验员方届群与李美容参与生理指标测试分析,在此一并致谢。
基金项目
广东省省级科技计划(2017A070701030,2014B070705002);广东省科学院院属骨干科研机构创新能力建设专项(2017GDASCX-0105);现代农业产业技术体系专项(CARS-170203);广东省甘蔗改良与生物炼制重点实验室开放运行(2017B030314123)。