1. 引言
人博卡病毒1型(Human bocavirus 1, HBoV1),是Allander等人于2005年首次发现,归属于细小病毒科,细小病毒亚科,博卡病毒属 [1] 。HBoV1后被证实是一种全球流行的重要呼吸道病原体,感染呼吸道可引起上、下呼吸道感染,并常与其他病原体产生共感染 [2] [3] [4] 。HBoV1本身是一种体积较小、具有二十面体衣壳、无包膜的单链线性DNA病毒,病毒粒子直径约为26 nm。目前仅有一例HBoV1完整基因组被测序,其长度为5543 nt (JQ923422),其基因组序列、转录谱和表达谱分析表明,其至少表达两种衣壳蛋白:VP1和VP2;两种非结构蛋白NS1和NP1。其中VP1、VP2分别有672aa、542aa,具有典型的基因重叠区,其中VP1-N端为非重叠区,长度为129aa,即VP1独特区(VP1-unique, VP1u)、后面为两个衣壳蛋白的重叠区(VP1/2),长度542aa,序列完全相同 [1] [5] [6] 。HBoV1由于其感染具有很强组织特异性,有文献报道其与AAV2/HBoV1形成的嵌合病毒有作为肺囊性纤维化(cysticfibrosis, CF)基因治疗载体的潜质 [7] [8] 。研究表明HBoV1的VP2可独立形成病毒样颗粒(Virus-like particles, VLP) [9] ,而HBoV1的VP1u区有磷脂酶A2样活性(Phospholipase A2-like activity),可以破坏细胞紧密连接 [10] [11] ,可见VP1u在HBoV1的感染和组织特异性方面可能都起到重要的作用。
为进一步对HBoV1进行深入研究,本研究针对VP1u区进行原核表达、纯化并通过免疫小鼠获得其抗体,为后续HBoV1感染研究奠定基础。
2. 材料与方法
2.1. HBoV广州株VP1u片段扩增
1) 主要抗原片段PCR引物设计
本研究针对前期获得的来源于60岁女性肺炎患者的HBoV1广州株(Access number: GU338055)进行抗原VP1u (aa 1–129)片段PCR引物设计,产物长度390 bp。
其中正向引物VP1u-gst-SalIF为5’-AAAGTCGACATGCCTCCAATTAAGAGACAGCCTA-3’;
反向引物VP1u-gst-NotIR为5’-AAAGCGGCCGCTTATGAGGTTCCTGGTTTAGGTTCACTC-3’。
2) 扩增条件:使用HBoV1广州株(Access number: GU338055)构建的反向遗传系统全长质粒(pHBoV-S2)作为模板,使用PrimeSTAR® Max DNA Polymerase 25 μl体系(Takara)对VP1u目标片段进行扩增反应
反应条件如下:预变性94˚C 5 min;循环条件(30×):98˚C 10 sec、55˚C 15 sec、72˚C 30 sec;延伸温度72˚C 5 min。1%琼脂糖凝胶电泳检测2 μl扩增产物。
3) 扩增产物纯化:使用Axygen® AxyPrep™ DNA Gel Extraction Kit(爱思进生物技术(杭州)有限公司)进行目标DNA的凝胶回收及纯化。
2.2. 原核表达载体构建、蛋白表达及纯化
2.2.1. 利用pGEX-4T-3质粒构建HBoV1 VP1u原核表达载体pGEX-VP1u。
1) 质粒与纯化的扩增片段酶切
使用Sal I和Not I(NEB)对pGEX-4T-3及PCR扩增的VP1u片段进行双酶切,50 μl酶切条件如下:
至37˚C水浴中2 h后,使用Axygen® AxyPrep™ DNA Gel Extraction Kit进行目标DNA的凝胶回收及纯化。
2) 连接
使用T4 DNA ligase (NEB)连接酶切的pGEX-4T-3与VP1u的双酶切产物,构建原核表达载体pGEX-VP1u。10μl连接条件如下:
至于16˚C中2 h。
3) 转化
使用E. coli TOP10感受态细胞(天根生化科技(北京)有限公司)转化连接产物,步骤如下:冰上融化感受态细胞,吸取连接产物至感受态中,冰浴30 min,42˚C热激45 sec,迅速转至冰浴2 min,加入无抗性LB培养基 500 μl至37˚C摇床中250 rpm 1 h,取200μl涂布氨苄青霉素LB固体平板(LB-Amp+平板),37˚C培养箱中倒置过夜培养。
4) 挑取单菌落并验证
挑取平板上的单菌落至含0.8 ml LB-Amp+液体培养基的1.5 ml离心管中,37˚C摇床中250 rpm培养4~5 h,使用菌落PCR进行阳性克隆筛选,即使用前述VP1u扩增引物VP1u-gst-SalIF/VP1u-gst-NotIR1中各片段扩增引物进行分别验证。菌落PCR条件如下:
反应条件:预变性95˚C 5 min;循环条件(30×):94˚C 30 sec、55˚C 30 sec、72˚C 30 sec;延伸温度72˚C 5 min。1%琼脂糖凝胶电泳检测扩增片段。挑选2例测序验证。
5) 使用AxyPrep质粒DNA小量试剂盒(Axygen)提取最终确认正确的pGEX-VP1u。使用0.5 μl提取质粒转化E. coli BL21感受态细胞(天根生化科技(北京)有限公司),方法同前述。
2.2.2. 蛋白表达及纯化
1) 蛋白表达
使用IPTG (Sigma)诱导蛋白表达,为获得可溶性蛋白,调整IPTG浓度、诱导时间、诱导温度,但最终目标蛋白未能获得可溶性目标蛋白,使用KCL染色切胶回收目标蛋白。步骤如下:挑取pGEX-VP1u阳性E. coli BL21接种至10 ml LB-Amp+液体培养基,37˚C摇床中220 rpm培养过夜;将培养物接种至100 ml LB-Amp+液体培养基中,37˚C摇床中220 rpm培养1~2 h,加入IPTG进行蛋白诱导表达;诱导条件为:IPTG终浓度0.8 mM、37˚C 220 rpm诱导5 h。
2) 蛋白纯化
5000 rpm 4˚C离心15 min收集菌体,加入10 ml PBS重悬细菌,使用冰上超声破碎细菌(20 sec开、5 sec停、70%功率、10~20 min)至菌液变青色。10,000 rpm 4˚C离心30 min弃上清。沉淀中加入8 ml PBS重悬沉淀,加入2 ml 5 × SDS上样缓冲液,100˚C变性5 min,10,000 rpm 4˚C离心30 min获得上清。使用上清进行SDS-PAGE,用经过预冷的0.25M KCL对蛋白胶进行染色(目标条带呈白色)。用干净的刀片切下目标条带,在蒸馏水中润洗脱盐,取出至干净的管中。剪碎凝胶,加入过量PBS,放入4˚C冰箱中过夜。第二天收集浸泡液(吸之前振荡),再加入PBS 4˚C过夜浸泡收集一次。使用10KD超滤管(Millipore)浓缩目标蛋白;12% SDS-PAGE检测目标蛋白,Bradford法检测蛋白浓度。
2.3. 小鼠免疫及效价检测
1) 目标蛋白使用100 μl完全弗氏佐剂(Sigma)与100 μl含50 μg目标蛋白充分乳化,腹腔注射BALB/c 六周龄小鼠,总计4次免疫。免疫后取血清。
2) 使用制备的抗原及临床HBoV1阳性样品分别进行ELISA抗体评价。将所用抗原用包被液稀释到2.5 μg/ml(制备的蛋白抗原)或使用确认的临床病毒阳性样品,酶标板每孔加入100 μl, 置4˚C,24 h包被;弃去孔中液体,使用150 μl封闭液37˚C封闭2 h;弃去孔中液体并洗涤5次,每次3 min;加入不同稀释梯度的血清样品进行检测,使用未免疫小鼠血清作为阴性对照,置于37˚C,30 min。用洗涤液满孔洗涤5遍,每遍3 min;加入酶标抗体(HRP-羊抗鼠)37˚C,30 min之间;洗涤5次后使用TMB-过氧化氢尿素溶液底物反应(Millipore),37˚C避光放置3~5 min,加入终止液显色,测A450。
2.4. 抗体在HBoV1免疫荧光实验中的应用
使用所制备的VP1u抗体血清对转染HBoV1反向遗传系统全长质粒pHBoV-S2的AD293细胞进行免疫荧光实验。
1) 提前一天于24孔板中接种AD293细胞,使用Lipofectamine 3000化转试剂转染质粒至细胞,转染后在37˚C 5% CO2培养箱中培养72 h。
2) 使用所制备抗体进行VP1u的免疫荧光检测。步骤如下:24孔板中细胞PBS浸洗3次,每次3 min;用4%的多聚甲醛固定15~30 min,PBS浸洗孔3次,每次3 min;0.5% Triton X-100 (PBS配制)室温通透20 min;PBS浸洗孔3次,每次3 min,吸干PBS,在孔中加正常10%山羊血清,室温封闭30 min;吸掉封闭液,每孔加足够量的稀释好的所制备的一抗血清(1:50),并使用阴性小鼠血清作为阴性对照,放入湿盒,37˚C 1 h;PBST浸洗孔3~6次,每次3 min,吸干孔中多余液体后滴加稀释好的荧光二抗(FITC-羊抗鼠) (联科生物),湿盒中37˚C孵育1 h,PBST浸洗孔3次,每次3 min;(注意:从加荧光二抗起,后面所有操作步骤都尽量在较暗处进行)。吸干孔中的液体,用含抗荧光淬灭剂的封片液封片,然后在荧光显微镜下观察采集图像。
3. 实验与结果
3.1. HBoV1 VP1u片段原核表达载体构建
实验通过PCR获得了VP1u的目标片段(图1),并利用pGEX-4T-3构建了原核表达载体pGEX-VP1u(图2),并最终通过测序验证正确。
3.2. 蛋白表达与纯化
通过KCL染色切胶回收,获得VP1u目标蛋白(GST-VP1u融合蛋白分子量为40.2KD) (图3),浓度
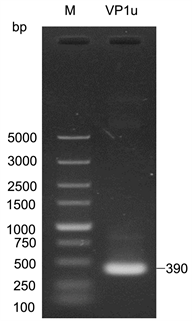
Figure 1. The DNA fragments of HBoV1 antigen VP1u; M: DNA marker
图1. HBoV1抗原VP1u DNA扩增产物;M:DNA marker
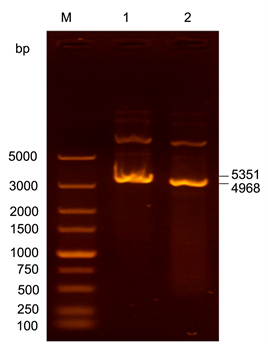
Figure 2. Construction of prokaryotic expression plasmids for HBoV1 antigen VP1u; M: DNA marker; 1: pGEX-VP1u; 2: pGEX-4T-3
图2. HBoV1 VP1u原核表达载体构建;M:DNA marker;1:pGEX-VP1u;2:pGEX-4T-3
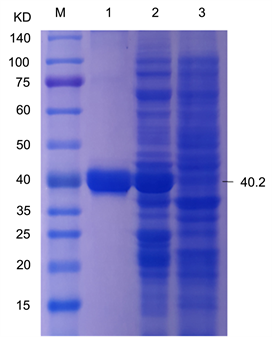
Figure 3. SDS-PAGE test for proteins of HBoV1 VP1u; M: Protein marker; 1: GST-VP1u fusion protein; 2: IPTG-induced E.coli BL21-VP1u; 3:Non-IPTG-induced E.coli BL21-VP1u
图3. HBoV1 VP1u蛋白SDS-PAGE;M: Protein marker;1:GST-VP1u融合蛋白;2:IPTG诱导菌;3:IPTG未诱导菌
为1.055 μg/μl。
3.3. 免疫与抗体效价
通过免疫BALB/c小鼠,获得一批免疫血清,分别使用蛋白抗原和阳性临床标本对其进行评价(表1) (表2)。与阴性小鼠血清对比2倍以上升高的稀释度起始于1:1,000,000;使用阳性样品进行的评价表明,其在1:50情况下约有4倍升高。
3.4. 抗体在HBoV1免疫荧光实验中的应用
使用制备的抗体,对利用反向遗产系统制备的HBoV1进行主免疫荧光检测(图4)。实验结果显示VP1u在细胞中的分布。
4. 讨论
HBoV1是全球流行的重要呼吸道病原体,由于其很难获得纯培养病毒,对其的研究还处于初始阶段,更无相应的动物模型建立,所以对其感染及致病的机制还需更多的研究。目前体外研究表明感染HBoV1后可导致分化的组织样支气管上皮细胞(HAE)的纤毛减少、紧密连接遭到破坏、细胞肥大,这些特点与肺损伤的组织变化非常相似 [5] ,在一定程度上解释了HBoV1的致病机制,而研究表明VP1u的磷脂酶A2样活性(Phospholipase A2-like activity)具有损坏紧密连接的作用 [10] [11] ,说明了VP1u在病毒致病中

Table 1. A450 values at different serum dilutions in ELISA using protein antigen
表1. 蛋白抗原ELISA检测不同血清稀释度下的A450值
注:实验设置3个平行复孔,数据为A450值Mean ± SD。Note: The experiment set three parallel tests, the data for the A450 value Mean ± SD.

Table 2. A450 values at different serum dilutions in ELISA using clinical HBoV1-positive sample antigen
表2. 临床HBoV1阳性样品ELISA验证不同血清稀释度下的A450值
注:实验设置3个平行复孔,数据为A450值Mean ± SD。Note: The experiment set three parallel tests, the data for the A450 value Mean ± SD.
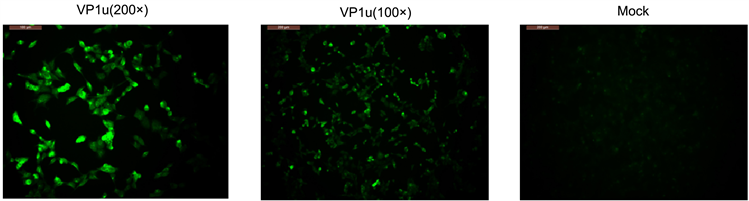
Figure 4. Immunofluorescence detection of HBoV1 antigen VP1u using antibody preparation. Note: Using 1:50 dilution of the preparation antibody as primary antibody, using negative mouse serum as a primary control, using FITC-goat anti-mouse antibody as secondary antibody.
图4. 利用制备抗体对HBoV1抗原VP1u进行免疫荧光检测。注:使用1:50稀释的制备抗体作为一抗,使用阴性小鼠血清作为一抗对照,使用FITC-羊抗鼠抗体作为二抗。
的重要作用。HBoV1的感染对气道上皮细胞的纤毛和紧密连接的破坏,可能导致人体防御外来侵害的第一道防线遭到破坏,可能导致人体对外部病原体更加易感,也一定程度上解释了HBoV1存在的高共感染率。这些证据表明HBoV1感染的影响可能不仅仅局限于自身导致疾病的产生,同时也在于导致其他病原体易感。
本研究针对HBoV1 VP1u进行抗体制备。研究利用pGEX-4T-3质粒成功构建了pGEX-VP1u表达载体(图1、图2),并通过诱导表达获得目标蛋白(图3)。实验通过腹腔免疫小鼠获得抗体血清,并分别利用目标蛋白和临床阳性标本评价抗体效价(表1、表2)。在利用阳性标本进行的评价中,三种血清1:50稀释后,A450均可获有4倍提升(表2),说明所制备的抗体可以满足用于后续的实验应用。为进一步验证抗体的效果,实验针对HBoV1广州株反向遗传系统转染制备的病毒进行免疫荧光检测(图4),获得了良好的效果,证明了其具有良好的应用效果。
本研究针对HBoV1 VP1u抗原进行了抗体制备,实验证明所制备抗体具有良好的效果,为HBoV1的研究提供了重要的工具,为其后续研究奠定重要的基础。
基金项目
国家自然科学基金-青年基金项目(31500143);国家“艾滋病和病毒性肝炎等重大传染病防治”科技重大专项(2018ZX10102001, 2017ZX10103011)。
NOTES
*通讯作者。