1. 引言
龋病是广泛流行的细菌感染性疾病,是世界卫生组织公布的需要重点防治的三大慢性非传染性疾病之一 [1] 。在我国,大约有4亿人患有龋齿,每年相关的治疗费用高达100亿 [2] 。2017年全国第四次口腔流行病学调查结果显示,儿童患龋率在过去十年内有所上升,在5岁和12岁儿童中分别达到70.9%和34.5% [3] 。龋病一旦发生就不可逆,占中老年人群失牙原因的80% [4] 。面对我国人口结构老龄化的趋势,用预防手段加强对于老年人、儿童等重点人群的龋病干预,进行龋病防治是当今急需解决的公共卫生问题。
随着基因工程及分子生物技术的发展,通过转基因的方法使植物表达外源蛋白,生产出口服疫苗是当前疫苗研发的热点。表达与龋病发生密切相关的抗原蛋白的防龋疫苗,通过直接口服给药的方式,不仅能引起广泛的体液免疫和细胞免疫,递呈至口腔、肠道粘膜淋巴组织中的抗原还能激活特异性免疫应答,具有安全、有效、经济、易推广的优点,在龋病预防领域具有广阔的发展前景。
表面蛋白抗原(Cell surface protein antigen, PAc)是变异链球菌致病的主要毒力因子,在细菌黏附牙面的过程中起着重要作用,对其全分子或部分片段进行主动或被动免疫均可有效控制变异链球菌在牙面的黏附, 降低患龋率 [5] 。对表面蛋白抗原的研究表明,其结构中具有两个高度保守的区域,包括黏附功能A区(PAcA)及免疫活性P区(PAcP),前者是位于氨基端的富含丙氨酸的区域,后者位于中间区域并富含脯氨酸,是重要的抗原区域 [6] 。霍乱毒素B亚单位(Cholera toxin B, CTB)是一种较强的免疫佐剂和抗原输送载体,通过与小肠黏膜细胞GM1神经节苷脂受体的特异性结合促进抗原成分与细胞的广泛接触,诱导黏膜和血清特异抗体产生,增强免疫反应 [7] 。
将龋病预防与转基因可食植物结合的防龋策略是目前龋病防治领域极具科研转化潜能的研究方向,现有研究中对植物疫苗中外源蛋白表达的报道较少。本课题组将表面蛋白PAc的A区、P区的编码基因(pacA和pacP)分别与霍乱毒素B亚单位CTB的编码基因ctxB融合,得到外源目的基因,并经农杆菌转化法得到转基因可食防龋番茄疫苗。在前期研究中,转基因番茄已被证实能成功地表达外源蛋白 [8] ,免疫原性表现较好 [9] ,并且具有生态安全性和免疫动物安全性 [10] 。本实验对连续四代的防龋番茄中的外源蛋白进行检测,得到筛选出的高效表达植株,并对外源蛋白的变化进行监测,确定生产采集的最佳时期,进一步为未来的研究以及疫苗商品化打下基础。
2. 材料与方法
2.1. 材料
含目的基因pacA-ctxB和pacP-ctxB片段的原代番茄种子(课题组前期制备),红抗219番茄种子(山西豪丰种苗有限公司),变异链球菌表面蛋白抗原PAc、抗PAc抗体(课题组前期分离纯化),辣根过氧化物酶标记的羊抗兔IgG (Genetex,美国)。
2.2. 方法
2.2.1. 番茄植株的种植培养
田间种植培养含目的基因pacA-ctxB和pacP-ctxB的转基因番茄及其后代番茄植株F0、F1、F2、F3及对照红抗2019番茄,每代11株,共99株番茄植株。
2.2.2. 转基因番茄果实和叶片总蛋白的提取
在植株的开花坐果期,每周对番茄果实及叶片进行留样,液氮研碎成粉,加入10 mL经4℃预冷的蛋白提取缓冲液(Na2HPO4 3.581 g,KH2PO4 0.408 g,NaCl 5.844 g,抗坏血酸钠4.953 g,聚乙烯吡咯烷酮(Polyvinylpyrrolidone, PVP40) 5 g,纤维二糖0.343 g,甲基吡喃糖苷0.194 g,植物蛋白酶抑制剂5 mL,双蒸水定容至1 L),充分匀浆,冰上静置4 h。4℃,13,000 rpm离心10 min,取上清液过滤,得到可溶性蛋白溶液。分装并标记样本,−20℃保存。
2.2.3. 转基因番茄中目的蛋白的Western印迹检测
沸水浴加热蛋白质样品5 min,SDS-PAGE电泳分离蛋白质,转膜。封闭后加入用PBST按1:80稀释的抗PAc抗体,洗涤后加入用PBST按1:1000稀释的辣根过氧化物标记的羊抗兔抗体。洗膜,漂洗并加入显色剂,读片观察。
2.2.4. BCA法测定总蛋白的含量
依据试剂盒使用说明,用BCA法对样品进行检测及初步的定量。用酶标仪测取样品的OD562值,根据标准曲线计算出可溶性总蛋白浓度。
2.2.5. ELISA检测外源重组蛋白的表达
取PAc转基因番茄蛋白提取液、抗原包被液及标准蛋白浓度梯度液包被酶标板,4℃过夜后洗板并加入150 μL抗原包被液,放置于室温3 min后加入100 μL封闭液继续孵育2 h。洗板后加入用PBST按1:80稀释的抗PAc抗体,孵育2 h,洗涤后加入用PBST按1:1000稀释的羊抗兔抗体,孵育1 h,洗板,加入底物反应液暗反应15 min后加入终止液。用酶标仪记录样本的OD490 nm值,根据标准曲线算出外源蛋白浓度。
2.3. 结果分析
用SPSS统计软件实验分析数据。转基因番茄表达阳性率比较用卡方检验分析,多组间比较采用卡方检验分析,多组间比较采用单因素方差分析,两组间方差齐时采用LSD进行检验,反差不齐时采用Tamhane检验。以均数 ± 标准差表示数据。P < 0.05时认为有统计学差异,P < 0.01时认为有统计学显著性差异。
3. 结果
3.1. 转基因番茄及对照番茄果实
如图1所示,转基因番茄果实与对照番茄果实大小有较大差异。
3.2. Western蛋白印迹检测
如图2中,样本在曝光图片上出现了明显低密度条带,相对分子质量约55 KD。
表达外源蛋白的植株共62株,其中含目的基因pacA-ctxB表达外源蛋白的为31株,含目的基因pacP-ctxB的植株中28株表达外源蛋白,对照组中2株表达外源蛋白,具体分布如表1所示。含目的基因pacA-ctxB的植株表达阳性率为70.5%,pacP-ctxB组为63.6%,对照组为22.2%,总体转基因植株中外源蛋表达阳性率为67.1%。经卡方检验,转基因番茄外源蛋白表达阳性率两两比较,无统计学意义(P < 0.05)。

Figure 1. The fruits of transgenic tomato
图1. 转基因番茄果实及对照番茄
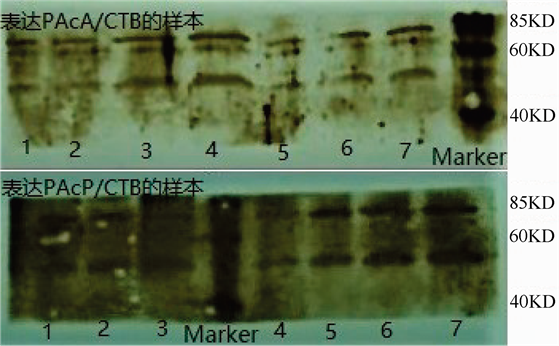
Figure 2. The Western blot results of heterologous protein expressing of transgentic tomatoes
图2. 转基因番茄表达外源蛋白Western蛋白印迹结果

Table 1. Distribution of transgenic tomatoes with exogenous protein
表1. 表达外源重组蛋白的转基因番茄植株
3.3. BCA法检测转基因番茄中总蛋白量
根据BCA法检测并绘制标准曲线,得回归方程:Y = 0.2117X + 0.1027,回归系数为0.9923。如图3所示,可见OD值随蛋白浓度增加而增大,在0~0.5 mg/ml范围内线性关系良好。t检验P < 0.01。说明两变量之间具有相关性。
3.4. ELISA法检测外源蛋白的表达
根据ELISA 法检测并绘制标准曲线,得回归方程为:Y = 0.1586X + 0.1199,回归系数为0.9877。如图4所示,OD 值随蛋白浓度增加而增大,在0~1 mg/ml范围内线性关系良好。对其进行t检验P < 0.01。说明两变量间有相关性。
3.5. 转基因番茄不同子代果实外源重组蛋白表达量分析
如图5所示,表达目的蛋白的四代植株中,F0代果实表达PAcA/CTB、PAcP/CTB的比重最高,分别达到总蛋白含量的0.247%和0.307%。表达PAcA/CTB的果实中外源蛋白含量逐代降低明显,在F1,F2,F3分别为0.087%、0.103%、0.077%;表达PAcA/CTB的果实中F1,F2表达稳定,F3代明显降低,含量分别为0.300%、0.278%、0.176%。
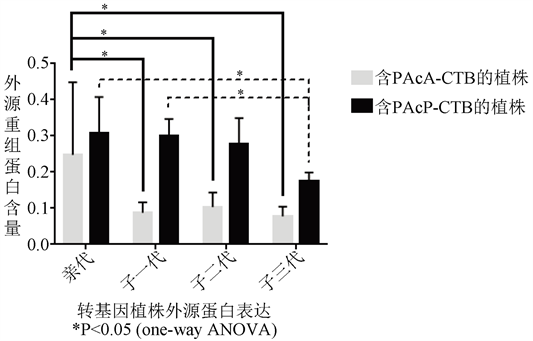
Figure 5. Expression content of PAcA/CTB, PAcP/CTB between generations
图5. 子代成熟果实含PAcA/CTB、PAcP/CTB含量对比图
3.6. 生长发育中外源重组蛋白表达分析
3.6.1. 植株叶片中外源重组蛋白含量
如图6所示,含目的基因pacP-ctxB的植株叶片中外源蛋白含量较含pacA-ctxB的高,在植株叶片中外源蛋白含量均值为0.024%~0.04%。

Figure 6. Expression content of PAcP/CTB and PAcP/CTB in transgenic leaves
图6. 转基因番茄植株叶片PAcP/CTB,PAcA/CTB含量
3.6.2. 转基因番茄果实中外源重组蛋白表达含量分析
如图7所示,在番茄果实中外源蛋白含量均值为0.06%~0.59%,较叶片高,含目的基因pacP-ctxB的番茄果实中外源蛋白含量比含pacA-ctxB的高。在番茄植株开花坐果期的第6至8周最适宜采摘,此时番茄果实中蛋白表达含量高而稳定。
3.6.3. 转基因番茄植株不同果实表达外源重组蛋白的水平分析
如图8所示,同期成熟的不同果实中外源重组蛋白含量差异明显。
4. 讨论
变异链球菌(Streptococcus mutans, S. mutans)作为龋病的主要致病菌之一,通过其表面蛋白分子PAc (Cell surface protein antigen, PAc)的作用介导细菌在牙齿表面的黏附和集聚,因此是重要的毒力因子,也是用于龋齿预防的有效抗原 [11] 。通过转化此黏附基因进入植物,获得防龋植物疫苗能够直接通过口服给药,在机体中广泛地诱导免疫应答 [12] [13] 。植物转基因技术是指通过微生物、人工载体介导、显微注射及基因枪轰击等方法,导入目的基因使外源基因与植物细胞DNA整合,实现基因水平的有效调控,使植物生产出具有生物活性的目的蛋白质并稳定遗传。此种疫苗利用植物的独特优势,相比细菌、酵母及哺乳动物细胞等传统疫苗具有明显优势:1) 独特的细胞壁作为“生物胶囊”起作用,2) 能通过口服的方式诱导黏膜免疫,3) 完整的真核系统能表达具有生物活性的产物,4) 便于生产、运输、保存,成本低廉,5) 疫苗安全,避免污染等。
转化的外源基因在植物中的遗传稳定性,对于转基因植株的商业化生产非常关键。理论上一旦有外源基因整合到DNA中,就能稳定地遗传给子代,但尚有还未明确的分子机制对外源基因的表达进行调控。将基因检测结果与Western Blot检测结果进行对比,结果显示部分含有目的基因的番茄植株发生基因翻译水平上的不表达(或异源表达):转入pacA-ctxB的FA2植株及FA3植株分别有1株和3株出现外源蛋白不表达,转入pacP-ctxB的FP2植株有4株不进行表达。转化基因时的插入位置效应(position effect)及同源诱导或重复序列诱导都可能造成基因沉默(gene siliencing) [14] [15] [16] 。针对这点,学者们提出不少解决方案如在外源基因两端添加GC序列、添加启动子、选择能特异性调控的增强子、限制基因拷贝等。
基因逃逸(gene flow)是指目标基因在一定范围内的植株及野生株间转移,导致野生株发生基因水平上的改变,一般通过花粉传播的途径进行漂移 [17] 。学者们在多种转基因植物中均发现基因逃逸现象。除报道的马铃薯、棉花、水稻、油菜、草莓、玉米之外,本课题组前期实验 [18] 发现距离转基因番茄0.5 m处的非转基因番茄有1株F2植株中检测出外源基因。邸宏 [19] 等研究发现,转基因玉米的漂移率与距离成

Figure 7. Expression content of PAcP/CTB and PAcP/CTB in transgenic fruits
图7. 转基因番茄果实中外源重组蛋白PAcA/CTB,PAcP/CTB含量
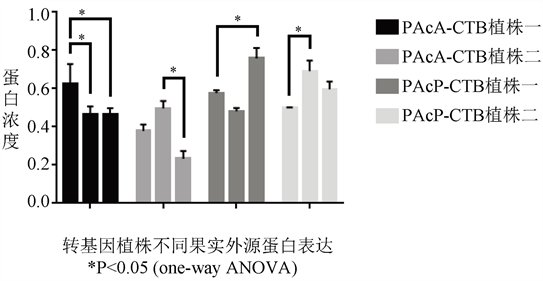
Figure 8. Expression content of exogenous protein in one transgenic plant same time
图8. 转基因番茄同株同期果实A15、A17;同株P15、P17果实中外源蛋白表达含量
正相关。水稻试验显示,转基因稻与非转基因稻之间距离大于10米时,产生株间基因逃逸的概率就会下降,概率为万分之几。将外源基因转入叶绿体也能明显减少基因逃逸。本实验对照组中检测到外源蛋白的表达,可能由于株间距离过小(田间种植行距为100 cm)而发生基因漂移,外源基因可能通过花粉、根系、土壤感染对照组植株。
自1990年Curtiss等 [20] 首次报道了烟草表达的链球菌属的表面蛋白spaA具有免疫原性以来,植物口服疫苗经过20多年的发展,成功实现了外源蛋白在烟草、马铃薯、番茄、大豆和谷类等近200种植物中的表达 [21] 。众多已报道的研究中,外源基因所表达的外源重组蛋白大约只占植物可溶蛋白的0.01%~0.37% [22] ,较低的生产效能限制了其运用。有学者提出 [23] ,今后转基因发展的一大问题就是如何使外源基因高效表达,同时避免基因沉默 [24] 。对此,目前的研究报道主要集中在转化技术优化及载体构建方面 [25] 。转基因技术的遗传机制尚未明确,且难以精准控制整合位点和基因拷贝,可能导致表达效率低,表达不稳定等问题。基因扩散也存在生态问题的隐患。通过外源基因转化叶绿体可以加以改进:1) 叶绿体拷贝量大,可以增加基因的表达量2) 叶绿体基因通过同源重组可以实现定点整合,避免了位置效应及基因沉默3) 叶绿体独特的母系遗传特性避免了基因逃逸4) 叶绿体基因独特的操纵子存在形式可以使多个外源基因同时表达。有文章报道,外源蛋白表达占可溶性总蛋白的1%以上就是较好的结果 [26] 。本室验获得的转基因番茄果实中,最高表达量可达可溶性总蛋白的0.65% [27] 。在提取蛋白质的过程中严格控制离子强度和pH值、低温操作、加入适量的除污剂或蛋白酶抑制剂均可以防止蛋白变性及
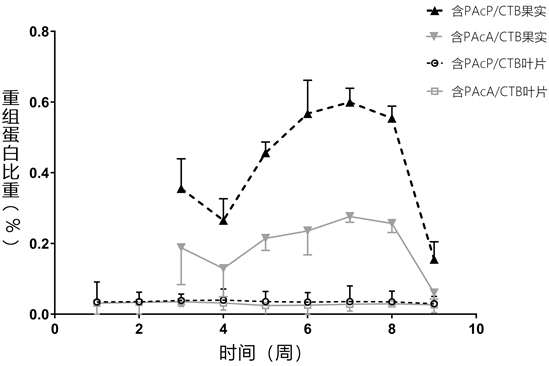
Figure 9. Expression content of PAcP/CTB and PAcP/CTB in transgenic tomatoes and leaves
图9. 转基因番茄果实及叶片的外源蛋白PAcA/CTB,PAcP/CTB含量
降解,利于蛋白质提取的效率,便于蛋白的测定 [28] [29] [30] 。另外,优化启动子、使用信号肽、修饰转译序列等都是在基因调控层面提高外源蛋白表达水平的可行途径。田间种植的番茄植株不可避免地受到低温等环境因子的影响,不同的植物种类、器官、发育阶段和生理状态等因素会对植物造成程度不同的危害。番茄为冷敏感作物,有研究发现 [31] ,番茄在温度低于10℃时生长发育受阻。陈桂敏等 [32] 构建了油菜热休克蛋白启动子表达GUS基因的载体并转入烟草,发现热处理促进了gus基因表达,热休克蛋白基因启动子可以利用温度控制基因表达。张西倩等 [33] 发现来自丝状真菌瑞氏木霉的小分子疏水蛋白质也具有提高外源基因在植物中表达水平的作用。叶片是植物的营养器官,而果实属于植物繁殖器官,二者受到不同基因组基因的控制,已有学者证实果实和叶片中可溶性总蛋白的含量与成分并不相同,对外源蛋白的表达偏好也不同。本实验发现番茄果实表达的蛋白含量比叶片高,叶片中外源蛋白的表达总体含量不高,含量变化波动也不明显。
番茄的生长发育有一定的阶段性,有学者已经证实外源蛋白在植物各个发育阶段中的表达并不相同。张俊等 [34] [35] 发现蛋白含量在棉花中的表达随时间呈现动态变化,并与棉花的抗性变化基本吻合。本研究结合预实验结果,主要采集开花坐果期样本,此时蛋白含量高。Western Blot检测结果显示,番茄果实在开花坐果期的第6至8周中具有最高的外源蛋白表达量,而在叶片中外源蛋白含量变化不大(如图9)。不同代植株其外源蛋白表达量有统计学差异。外源蛋白表达随着传代而下降,但无持续下降的趋势,表明外源蛋白在后代植株中能够较为稳定地表达。植株不同器官表达外源蛋白的效率也不同,果实表达两种目的蛋白的效率高于叶片。两种目的蛋白表达效率相比,外源蛋白PAcP/CTB表达效率在果实及叶片中均高于PAcA/CTB,并且在果实发育生长的不同发育阶段中,外源蛋白PAcP/CTB的表达含量也均高于PAcA/CTB。这些现象可能由多种原因造成:融合基因及连接肽的CG含量不同、植物对密码子的表达偏好不同、mRNA含有不稳定信号、外源基因的整合效率有差异、拷贝数不同、整合区域转录活性不同、插入位点不同等造成的位置效应等。
达到提高外源重组蛋白表达量可以从以下几个方面着手 [36] [37] [38] [39] [40] :1) 选择能高效表达外源蛋白的叶绿体转化系统。2) 选择能够高效表达的启动子。3) 添加高效翻译元件如密码子、增强子。4) 针对选用植物器官特异性启动子、增强子,提高疫苗果实表达。5) 添加免疫佐剂激发免疫。
总之,外源基因在植物中的表达机制尚未明确,表达效率受到多种因素影响,相信通过对外源基因表达效率的研究,能在未来针对现存的问题进行改进,生产出具有推广应用潜力的转基因可食防龋疫苗产品。
基金项目
国家自然科学基金项目《新型转基因植物防龋疫苗的研制及其口服免疫机制研究》(合同号:81260164);贵州省科技支撑计划项目《转基因番茄防龋疫苗高效表达和稳定性及安全性研究》(合同号:黔科合SY字(2012)3086号);贵州省普通高等学校口腔疾病研究特色重点实验室开放课题《口腔新型抗菌材料生物安全性研究》(课题号:SKLODR201701,课题本编号:K-025)。
NOTES
*并列第一作者。
#通讯作者。