1. 引言
亚稳态分子间复合物(metastable intermolecular composites, MICs)是一种由纳米尺度的还原剂(一般为Al、Mg、Ti等金属元素)与氧化剂(一般为金属氧化物)颗粒均匀混合而成的复合含能材料,并因其具有较高的能量密度与较快的放热速率而在军工或民用领域广受关注 [1] 。迄今为止,对MICs的研究多集中于通过设计新颖的制备方法针对复合材料的形貌结构进行优化,进而对其放热性能进行改进 [2] [3] 。经过优化改性的MICs在放热量上显示出明显提升,但其反应放热速率通常较为缓慢,因而难以适用于诸如原位焊接等对需要复合材料快速释放大量热量的应用领域 [4] 。针对此问题,静电自组装 [5] 、热蒸镀 [6] 以及3D结构模版构建法 [7] 被开发应用,通过实现复合物组分间最大程度的接触,从而提升材料的反应放热速率。然而,由于上述制备过程通常需要借助特殊的设备或方法,难以适应批量化生产的要求,因此距离实际应用仍有较大距离。因此设计开发一种简捷高效并可以实现亚稳态分子间复合物高放热量与快放热速率的制备方法是该领域的研究热点之一。
石墨烯是一种具有良好的导热性与导电性,并具有较高比表面积的二维材料。氧化石墨烯作为其衍生物在具有石墨烯的性质的同时,亦具有丰富的含氧官能团,并可以借此与金属或金属氧化物纳米颗粒表面形成静电或化学作用力,因此可用来组装MICs [8] 。通过氧化石墨烯经历“光-费顿反应”而制备的石墨烯量子点(graphene quantum dots, GQDs)在具有上述性质的同时,其尺寸(约为10 nm)更匹配于纳米颗粒 [9] ,因而被证明可用于制备MICs,并且在水体系中所制备MICs较之于相同条件下物理共混产物,放热量与放热速度得到明显提升 [10] 。然而,受限于在水体系中,Al纳米颗粒存在的团聚现象与其表面氧化层的不断生成,所制备的MICs放热速率较为平缓,反应放热量也有待改善。
因此,本文设计两步法通过引入异丙醇作为有机体系,通过GQDs作为媒介自组装制备Al/GQDs/CuO MICs。所制备的MICs反应放热量与水体系制备的复合物相比有显著提升,并通过在有机体系中使用乙酸(acetic acid, HAc)对Al纳米颗粒表面进行刻蚀,复合材料的反应放热速率得到进一步提升。
2. 实验
2.1. 材料制备
MICs的自组装制备过程如图1所示。首先,将19.3 mg CuO纳米颗粒通过超声分散在150 mL去离子水中得到其水分散液;将与CuO纳米颗粒质量比为1:90的GQDs加入到CuO纳米颗粒分散液中,充分搅拌1 h,蒸发去除其水分并收集产物,得到CuO/GQDs复合物。
之后,将所制备的CuO/GQDs复合物与6.2 mg Al纳米颗粒分别分散在100 mL异丙醇中。随后将CuO/GQDs复合物的分散液逐滴加入到处于搅拌状态下的Al纳米颗粒异丙醇分散液中,充分搅拌共混1 h后,抽滤并干燥收集样品,得到Al/GQDs/CuO MICs (三者质量比为20:1:90)。
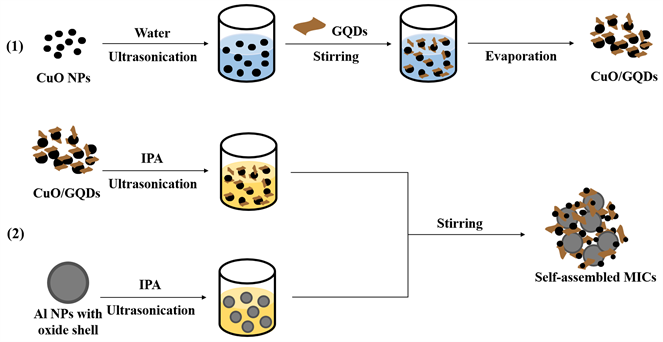
Figure 1. Schematic of the self-assembly procedure of MICs
图1. MICs的自组装过程示意图
对Al纳米颗粒表面Al2O3氧化层的刻蚀步骤在氮气保护下于异丙醇中进行。HAc的使用量依据反应式
的化学计量比,并定义等值比(equivalence ratio) x = (HAc/Al2O3)actual/(HAc/Al2O3)stoichiometric,其中x的值为1.0时表示所用HAc的量满足理论上反应掉Al纳米颗粒中所含Al2O3的需求量。x的值为0.5~2.5,代表HAc的用量由少量至过量呈现梯度变化。经HAc刻蚀后的Al纳米颗粒依照上述第二步制备复合材料,产物记作Alx/GQDs/CuOMICs。
2.2. 结构与性能表征
Al/GQDs/CuO MICs的微观结构采用德国蔡司Ultra 55扫描电子显微镜与日本JEOL JEM-2100F透射电子显微镜进行观测;采用英国马尔文NanoZS90 Zeta电位测试仪测量纳米颗粒及复合物表面电荷状态;MICs中组分间界面的X射线光电子谱采用日本岛津Krotos AXIS-Ultra DLD进行采集;采用布鲁克海文NanoBrook Omni动态光散射仪观测纳米颗粒在不同分散剂中的分散状态;采用德国耐驰STA
449 F
3 Jupiter差示扫描量热仪在高纯氩气气氛下对MICs的热性能进行表征,测试温度区间为25˚C~1000˚C,升温速率为10˚C∙min−1。
3. 结果与讨论
3.1. Al/GQDs/CuO MICs的形貌与化学组成分析
Al/GQDs/CuO MICs的两步法自组装制备过程首先在水体系中制备得到CuO/GQDs复合物,其微观形貌如图2(a)~(c)所示。可见CuO纳米颗粒的平均粒径为40~60 nm,呈现均匀分散形貌,并且其透射电子显微镜照片(图2(b))显示,直径约为5 nm的GQDs附着在CuO纳米颗粒表面。高分辨透射电子显微照片(high-resolution TEM, HRTEM)采集到复合材料的两种晶格条纹(图2(c)),其宽度为2.12 Å与2.76 Å,分别对应GQDs的(100)晶面与CuO的(110)晶面,证实CuO/GQDs复合物的形成。随后,将CuO/GQDs复合物于Al纳米颗粒在异丙醇中进行MICs的自组装,其产物Al/GQDs/CuO MICs的形貌如图2(d)~(f)所示。由图2(d)材料的扫描电子显微照片可知,CuO/GQDs复合物均匀的环绕在平均直径为80 nm的Al纳米颗粒周围,并且Al纳米颗粒亦表现为均匀分散,并且,通过高倍视野下的显微照片可进一步发现,CuO与Al纳米颗粒间紧密接触呈现较好的自组装形貌。图2(e)和图2(f)的透射电子显微照片进一步显示,GQDs出现在Al与CuO纳米颗粒的中间,证实其作为自组装媒介,将两种纳米颗粒紧密连接,增大了二者的接触面积。

Figure 2. (a) SEM, (b) TEM and (c) HRTEM images of CuO/GQDs composites; (d) SEM, (e) TEM and (f) HRTEM images of Al/GQDs/CuO MICs
图2. CuO/GQDs复合物的(a) SEM、(b) TEM与(c) HRTEM图;Al/GQDs/CuO MICs的(d) SEM、(e) TEM与(f) HRTEM图
通过Zeta电位与X射线光电子谱对GQDs与Al或CuO纳米颗粒间的具体作用进行研究。如表1中不同组分在不同分散剂中的Zeta电位测试结果所示,CuO纳米颗粒与GQDs在水中分别带正电与负电,因此静电作用力作为初始驱动力促进GQDs与CuO进行组装。进一步地,Al纳米颗粒与CuO/GQDs复合物在异丙醇中表面所带电荷相反,因此静电作用力同样驱使CuO/GQDs复合物与Al纳米颗粒进行自组装。而组分间的化学作用力则通过X射线光电子谱进行进一步研究。如图3(a)所示,Al/GQDs/CuO MICs的C 1s图谱中出现的四个分别位于284.7 eV、286.0 eV、287.8 eV与288.7 eV的信号峰,分别归属于复合物中C=C/C–C、C-O-Al、C=O与COOH基团 [9] 。同时,对Al/GQDs/CuO MICs的O 1s图谱进行拟合得到五个位于530.7 eV、531.6 eV、532.6 eV、529.7 eV与531.5 eV的信号峰,其分别为O=C、Al-O-C、C-O-C、O-Cu与O-Al [11] 。通过对比发现,GQDs所带的羟基(−OH)与Al纳米颗粒表面的Al-O键形成Al-O-C共价键,而并未与CuO纳米颗粒形成任何化学作用力,因此可以证实:GQDs与CuO之间通过静电作用力结合,而与Al纳米颗粒之间在静电作用力的基础上进一步形成共价键,加固了复合物间的界面接触。

Table 1. Zeta potential of counterparts in different dispersant
表1. 不同组分在不同分散剂中的Zeta电位
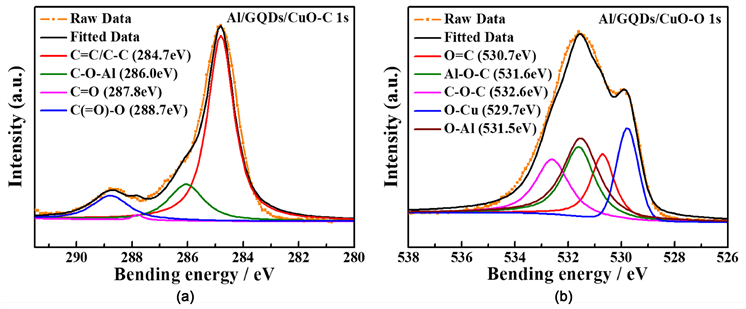
Figure 3. (a) C 1s and (b) O 1s XPS spectra of Al/GQDs/CuO MICs with Al:GQDs:CuO ratios of 20:1:90 (in weight)
图3. Al/GQDs/CuO MICs (质量比20:1:90)的(a) C 1s与(b) O 1sX射线光电子谱图
3.2. Al/GQDs/CuO MIC的放热性能分析
通过差示扫描量热法(differential scanning calorimetry, DSC)对所制备MICs的放热性能进行研究。如图4所示,Al/GQDs/CuO MICs (Al:GQDs:CuO质量比20:1:90)的DSC曲线在600˚C附近显示为单峰放热,表明Al与CuO之间发生放热反应,反应总放热量为1942.1 Jg−1。这一数值接近在水体系中所制备对应MICs放热量的二倍(1054 Jg−1) [10] 。其原因应归结于在异丙醇中,Al纳米颗粒分散性的提高而使得其表面可用来与GQDs进行自组装的作用位点增多,促进了Al与CuO纳米颗粒二者均匀紧密的接触。但是,Al/GQDs/CuO MICs的峰值瞬时热流率仍较低,意味着Al与CuO的反应速率较为平缓。由于在Al纳米颗粒的燃烧反应机理中,其内部活性Al原子与外侧金属氧化物分解释放的气态氧透过Al2O3钝化层进行的扩散过程是决定其反应引发快慢的决速步骤,因此对Al纳米颗粒外层Al2O3氧化层进行处理,促进物质传递,从而进一步提升反应速率。
通过HAc对Al纳米颗粒进行刻蚀,并制备的系列Alx/GQDs/CuO MICs (x = 0.5~2.5, x = 0表示未经HAc处理的Al纳米颗粒),其放热曲线如图5(a)所示。可见,当x的值为1.0~2.5,即HAc的使用量大于等于化学计量比需求量时,MICs的DSC曲线较之x为0或0.5时更为尖锐,并且呈现仅在600˚C附近(Al熔点之前)出现一个反应放热峰,说明MICs中Al与CuO纳米颗粒均在固态情况下进行反应,铝热反应
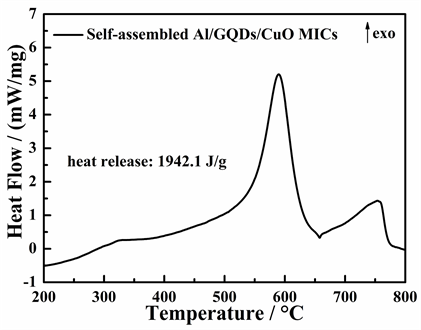
Figure 4. DSC curve of Al/GQDs/CuO MICs with Al:GQDs:CuO ratios of 20:1:90 (in weight)
图4. Al/GQDs/CuO MICs (质量比20:1:90)的DSC曲线

Figure 5. (a) DSC curves of Alx/GQDs/CuO with the mass ratios of 20:1:90. (b) heat release and peak heat flow of these series MICs
图5. (a) Alx/GQDs/CuO MICs的DSC曲线;(b) 反应放热量与峰值热流变化趋势图
以“固–固反应”的形式进行。如图5(b)所示,随着HAc使用量的提高,Alx/GQDs/CuO MICs的放热量与峰值瞬时热流皆显示出上升的趋势,而在x = 1.5时达到峰值,Al1.5/GQDs/CuO MICs的反应总放热量与峰值瞬时热流分别为2203 Jg−1与53.3 mW∙mg−1。这一现象说明,随着HAc加入,MICs的反应总放热量与反应放热速度都得到明显改善,而其原因应归结为通过HAc对Al纳米颗粒表层Al2O3钝化层进行处理,使得Al纳米颗粒内部的活性Al原子与外侧来自于金属氧化物分解产生的游离氧以较低的传质阻力透过氧化层进行扩散,促进了放热反应的引发与进行。这一推测通过对HAc处理后的Al纳米颗粒形貌进行观测得到进一步地印证。如图6所示,经过HAc处理后的Al纳米颗粒表面出现诸多缺陷与孔洞,而通过这些氧化层上较为薄弱的位点,活性Al原子与CuO分解释放的游离氧在一定温度下可以较为快速地透过氧化层进行扩散,从而促进了反应的快速引发,同时也提高了Al纳米颗粒的活性组分占比,从而综合提升了材料的反应放热量与反应放热速率。同时,过多的HAc会对活性Al内核进行腐蚀,这也造成了在HAc用量过多时(x的值为2.0与2.5),MICs反应放热量与瞬时峰值热流会呈现下降趋势。

Figure 6. TEM image of as-etched Al nanoparticles
图6. HAc刻蚀后的Al纳米颗粒的透射电子显微照片
4. 结论
本文设计GQDs引导的两步法自组装制备Al/GQDs/CuO MICs。GQDs与纳米颗粒之间通过静电作用力或以形成共价键的方式进行连结,促进Al与CuO纳米颗粒二者间的相互接触。同时,在有机体系中自组装制备的Al/GQDs/CuO MICs反应放热量较之于在水体系中制备的对应材料有显著提升,其原因归结于在异丙醇中Al纳米颗粒所具有的更好的分散性,从而实现的更为紧密的自组装形貌。此外,通过对Al纳米颗粒表面氧化层进行刻蚀,MICs的反应放热量与放热速率得到进一步提高。综合考虑制备方法的简捷高效性与所制备MICs良好的放热性能,GQDs引导的自组装制备方法有望实现高性能MICs在实际领域的应用。
NOTES
*通讯作者。