1. 引言
轻工、制药和化工等行业排放的废水普遍含有大量的硫酸盐,若这些废水不经处理直接排入水体,硫酸盐将被还原生成具有恶臭味和腐蚀性的硫化氢(H2S)气体,直接危害人体健康和水体生态平衡,对于富含硫酸盐的废水处理是当前亟待解决的问题 [1] 。
硫酸盐还原菌(SRB,sulfate reducing bacteria)广泛分布在自然环境中,是具有较强生命力的一种厌氧异养细菌,在无氧或极少氧条件下,硫酸盐还原菌可把硫酸盐、亚硫酸盐、硫代硫酸盐等硫氧化物以及元素硫还原成H2S,目前已知的硫酸盐还原菌种类达到40多种 [2] [3] 。利用SRB可处理含重硫酸废水、含重金属废水和含硫酸盐的废水,成本低且效果好。在处理煤化工废水以及酸性矿山废水方面,利用SRB对废水进行处理得到了广泛的关注。姜勇等考察了温度、pH、氯化钠以及重金属铜离子及亚铁离子对SRB还原硫酸盐的影响,发现SRB最适温度为35℃,最适pH为7,氯化钠质量分数大于1%时明显抑制SRB生长,高浓度重金属会显著抑制SRB生长 [2] ;徐师等的研究同样佐证了重金属会抑制SRB生长的结论 [4] 。但是对于SRB的生长代谢机理的研究并不明确,本文研究了不同电子供体对SRB生长代谢的影响,为SRB还原硫酸盐的机理研究提供了基础。
2. 材料与方法
2.1. 试验所用材料
2.1.1. 试验所用污泥
试验所用活性污泥取自上海市某污水处理厂二沉池。将污泥用自来水反复冲洗,去除里面粗大固体颗粒,然后将处理后的污泥倒入血清瓶密封保存于4℃冰箱中,2 h后将上层清液倾倒,得到经重力沉降的污泥备用。驯化污泥至全变为黑色,连续监测气态H2S产量稳定达到800 ppm以上。
2.1.2. 试验用水
试验用水为人工模拟废水,其中各物质组分浓度见表1。
2.2. 试验方案
本试验为序批次式试验。以乙酸钠、葡萄糖、乳酸钠、乙酸钠和葡萄糖混合电子供体、乙醇为电子供体研究培养条件下SRB的生长代谢特征。在500 mL血清瓶中加入电子供体,控制污泥浓度即MLSS在约6000 mg/L,加人工配水至400 mL刻度线,加入电子供体后混合液的COD控制在150 mg/L。持续通入N2,直至混合液的ORP降至−150 mV以下。将瓶口用橡胶塞密封后放入转速为150 rpm、温度为35℃的恒温摇床中分别培养12,24,36,48和60 h,到达预定培养时间后,取出培养瓶,先测定H2S

Table 1. Composition and content of experimental water
表1. 实验用水组分及含量
气体浓度,然后将培养瓶迅速转移至厌氧箱中,在厌氧箱中加药测定总硫化物(水中),取样品上清液经0.45 μm滤膜,滤液用于总有机碳(TOC)的测定。每3组为平行样,数据取平均值并计算标准偏差。
2.3. 测定方法
H2S气体浓度通过ADSK-4硫化氢气体浓度检测仪测定;总硫化物的测定使用哈希DR2800便携式分光光度计测定;TOC采用岛津TOC仪测定。
3. 结果与讨论
3.1. 电子供体种类对SRB厌氧产生H2S气体的影响
如图1所示,电子供体种类对SRB厌氧产生H2S气体有显著影响。SRB利用乙酸钠和葡萄糖混合电子供体产生的H2S气体最多,在60 h反应时间内达到957 ppm;其次为乳酸钠,SRB利用葡萄糖作电子
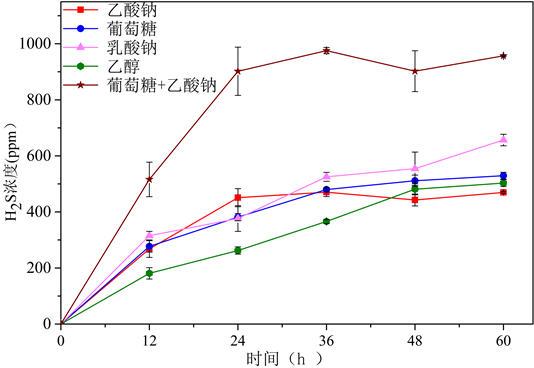
Figure 1. The concentration of hydrogen sulfide gas generated by SRB under anaerobic conditions using different electron donors
图1. SRB利用不同电子供体厌氧产生硫化氢气体浓度
供体在60 h反应时间内产生H2S气体656.67 ppm;产生H2S气体浓度最小的电子供体为乙酸钠,SRB在60 h反应时间内产生H2S气体469.67 ppm;葡萄糖、乙醇作电子供体时,该数据分别为529.33 ppm和503.36 ppm。按照SRB在60 h反应时间内产生H2S气体浓度的大小,电子供体的排序为:乙酸钠+葡萄糖>乳酸钠 > 葡萄糖 > 乙醇 > 乙酸钠。不论SRB利用何种电子供体,其厌氧产生的H2S气体浓度总体上呈现随反应时间增加而增加的趋势,并在60 h达到最高。
虽然SRB产生的H2S气体浓度总体上呈现随反应时间增加而增加的趋势,但SRB利用不同电子供体时,同一反应阶段H2S的产生速率各有不同。如表2所示,SRB利用5种电子供体高速率产生H2S气体均集中在0~12 h和24~36 h反应阶段,后三个反应阶段产H2S速率变化较为平缓。其中,SRB利用葡萄糖和乙酸钠混合电子供体时,H2S在0~12 h和12~24 h反应阶段的产生速率为5种电子供体中最高,分别为43 ppm/h和32.17 ppm/h。36~48 h反应阶段,SRB乙酸钠、乙酸钠和葡萄糖混合电子供体产生H2S速率出现负值,可能是因为溶液中H2S的电离平衡向右移动导致逸出水面H2S再次溶于水参加电离。

Table 2. Rate of hydrogen sulfide gas generated by SRB under anaerobic conditions using different electron donors
表2. SRB利用不同电子供体厌氧产生硫化氢气体速率(ppm/h)
3.2. 电子供体种类对SRB厌氧产生总硫化物(水中)的影响
SRB利用不同电子供体厌氧产生总硫化物浓度如图2所示(总硫化物包括S2−、HS−和溶解态H2S)。由图2可知,SRB利用不同种类电子供体时,所产生总硫化物浓度存在显著差异。SRB利用乙酸钠和葡萄糖混合电子供体在整个反应过程和不同反应阶段产生的总硫化物浓度均为5种电子供体中最高,这与H2S气体数据保持一致:5种电子供体中产生气态H2S最多的也是乙酸钠和葡萄糖混合电子供体。SRB利用乙酸钠和葡萄糖混合电子供体在12、24、36、48、60 h内分别产生总硫化物1526.67、2356.97、2346.67、2463.33、2493.33 µg/L。在60 h反应时间内,SRB利用乳酸钠产生的总硫化物浓度仅次于乙酸钠和葡萄糖混合电子供体,为2263.33 µg/L,这也和H2S气体数据一致;产生总硫化物浓度最小的电子供体为乙醇,SRB在60 h反应时间内产生总硫化物1150 µg/L;葡萄糖、乙酸钠作电子供体时,该数据分别为1133.33 µg/L和1290 µg/L。按照SRB在60 h反应时间内产生总硫化物浓度的大小,电子供体的排序为:乙酸钠+ 葡萄糖 > 乳酸钠 > 葡萄糖 > 乙酸钠 > 乙醇。SRB利用乙酸钠产生的气态H2S浓度低于乙醇,但产生的总硫化物浓度却略高于乙醇,这可能是因为乙酸钠为强碱弱酸盐,水解显碱性,消耗了一部分氢离子,使得逸出水面的H2S减少,大部分硫化物以离子态存在于水中。不论SRB利用何种电子供体,其厌氧产生的总硫化物浓度总体上呈现随反应时间增加而增加的趋势,并在60 h达到最高。除稍有差别的乙酸钠和乙醇外,按照SRB厌氧产生总硫化物浓度和按照气态H2S浓度高低的电子供体排序均保持一致。
虽然SRB产生的总硫化物浓度总体上呈现随反应时间增加而增加的趋势,但SRB利用不同电子供体时,不同反应阶段产生硫化物的比重不同。如表3所示,SRB利用5种电子供体所产生的总硫化物主要集中在0~12 h,除乙醇外,SRB利用其余电子供体在0~12 h产生的总硫化物占整个反应阶段的50%以上,乙酸钠和混合电子供体在12~24 h产生的总硫化物占整个反应阶段的比重依然在30%以上,其余电子供体在后续反应阶段均未超过25%。
SRB厌氧产生的硫化物包括S2−、HS−和溶解态H2S,除了部分以气态H2S的形式逸出水面外,其余硫化物均随着反应时间不断累积。累积的总硫化物会通过电离、平衡移动等原因引起混合液pH的下降(初始pH为7.0),而SRB最适生长pH条件为7~8。随着反应的进行,电子供体量不断减小,pH逐渐降低,混合液的条件已无法为SRB的生长代谢提供良好条件,所以在24h之后,SRB的代谢效率即厌氧还原
为S2−的效率逐渐下降,导致SRB利用5种电子供体产生的总硫化物均集中在0~24 h,而后续反应阶段产生的总硫化物的速率明显放缓。另外,硫化物的累积在一定程度上会对SRB本身造成一定的毒害作用,这也是SRB利用5种电子供体在24 h之后的反应阶段产生的总硫化物比重均显著下降的原因之一。
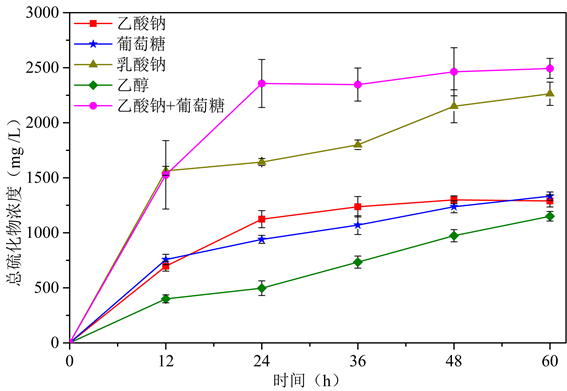
Figure 2. The concentration of total sulfide generated by SRB under anaerobic conditions using different electron donors
图2. SRB利用不同电子供体厌氧产生总硫化物浓度

Table 3. The ratio of the amount of sulfide produced by SRB under anaerobic conditions using different electron donors in different reaction stages to the total amount of sulfide produced during the reaction time
表3. SRB在不同反应阶段利用不同电子供体厌氧产生硫化物量占反应时间内产生硫化物总量的比例
3.3. SRB对不同电子供体的利用
由于试验所用5种电子供体均为含碳有机物且所配试验用水中不含其它含碳有机物,以总有机碳(TOC)浓度计量电子供体量,SRB对不同电子供体的利用情况如图3所示。由图3可知,SRB对不同电子供体的利用情况存在显著差异。随着反应时间的推移,SRB在不断利用电子供体,因此TOC浓度随反应时间的增加而降低。反应结束后,剩余乙酸钠和葡萄糖混合电子供体最少,TOC浓度为7.79 mg/L,同样SRB利用乙酸钠和葡萄糖混合电子供体时所产生的气态H2S和总硫化物均为5种电子中最高,表明SRB对乙酸钠和葡萄糖的利用程度最高。SRB对乙酸钠利用程度仅次于混合电子供体,乙酸钠对应的反应结束时TOC浓度为12.25 mg/L,但对照图1和图2中的数据,SRB利用乙酸钠产生的气态H2S和总硫化物在5种电子供体中分别为最少和第二少,这是由于乙酸钠属于一种快速可生物降解有机物,实验所用的SRB污泥中,不可避免的含有其他种类微生物,这些微生物的代谢生长同样需要电子供体。因此被利用乙酸钠所产生的电子并未全部用于SRB厌氧还原
产生S2−,才导致大部分乙酸钠被利用但气态H2S和总硫化物的产量不高的现象。SRB对乙醇的利用程度最低,反应结束时其对应TOC浓度为29.53 mg/L,剩余量为5种电子供体种最高,对照上述数据,SRB利用乙醇时所产生的气态H2S和总硫化物浓度分别为第二少和最少,这表明SRB不能很好利用乙醇这种电子供体,从而无法获取足够的电子推动还原
的反应进行,最终导致乙醇剩余量较高,而气态H2S和总硫化物产量低。SRB利用葡萄糖和乳酸钠时,反应结束时剩余TOC浓度分别为14.62 mg/L和16.89 mg/L。
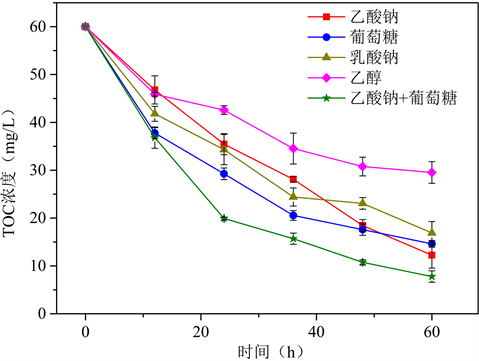
Figure 3. Utilization of different electron donors by SRB in different reaction stages
图3. SRB在不同反应阶段对不同电子供体的利用情况
SRB在整个反应过程中对不同电子供体的总利用率如图4所示。按照电子供体利用率高低排序:乙酸钠 + 葡萄糖 > 乙酸钠 > 葡萄糖 > 乳酸钠 > 乙醇。其中乙酸和葡糖糖混合电子供体的利用率高于其余电子供体,达到87.02%。乙醇的利用率为5种电子供体中最低,为64.54%。葡萄糖、乙酸钠和乳酸钠的总利用分别为77.31%,79.58%和71.84%。除乙酸钠外,其余电子供体的利用率基本和对应的SRB利用该种电子供体时产生的气态H2S和总硫化物量呈正比。
在高硫酸盐废水处理中,为提高硫酸盐还原率通常使用双基质即混合电子供体来提高SRB的活性。Ploprasert和Hass发现使用乙酸钠和葡萄糖双基质会显著提高SRB的活性,并大幅度提高硫酸盐的还原率,同时由于SRB对电子供体的高利用率出水COD极低。本章的实验结果也验证了上述研究成果,在五种电子供体中,SRB对乙酸钠和葡萄糖混合电子供体利用率最高,同样利用乙酸钠和葡萄糖混合电子供体产生的气态硫化氢和总硫化物也最多 [5] 。SRB可利用超过100种有机物作为电子供体,在废水脱硫

Figure 4. Total utilization of electronic donors of SRB
图4. SRB对电子供体的总利用率
处理中,优先选用乳酸盐作为电子供体,因为乳酸盐满足多种SRB生存所需,能够促进微生物系统中的多样性以及保持系统的稳定性 [6] 。Oyekolan以动力学方法研究了以乳酸盐为电子供体的硫酸盐生物还原还原过程的多种影响因素,结果表明硫酸盐浓度会在很大程度上影响SRB对乳酸盐类电子供体的利用 [7] 。本实验数据表明,SRB对乙酸钠和葡萄糖的利用率高于乳酸钠,利用乙酸钠和葡萄糖产生的硫化物也高于乳酸钠。乙醇在高硫酸盐负荷废水和重金属废水处理中常用作SRB的电子供体,可使硫酸盐的还原率达到80%以上 [8] 。但Yamashita等人通过研究发现,以乙醇作为SRB的电子供体存在利用率不高、出水COD偏高和成本偏高等问题 [9] ,本实验数据也同样表明SRB对乙醇的利用率相对其余电子供体较低。曹俊雅等人通过实验研究了SRB对包括挥发性脂肪酸盐类在内的多种电子供体的利用率,结果表明以乳酸钠作电子供体时的硫酸盐还原率要比乙酸钠高出20%,这与图1~3中数据相吻合:虽然反应结束后乙酸钠剩余量低于乳酸钠,但SRB在以乳酸钠作电子供体时,气态硫化氢和总硫化物的生成量要高于乙酸钠。

Table 4. The ratio of the amount of electron donor used by SRB in different reaction stages to the total electron donor
表4. SRB在不同反应阶段所利用电子供体量占总电子供体量的比例
表4更直观的反映了SRB在不同反应阶段对电子供体的利用情况:不论何种电子供体,SRB主要在0~12 h和12~24 h两个反应阶段进行利用。SRB在0~12 h和12~24 h利用的乙酸钠和葡萄糖混合电子供体占整个反应阶段利用的50%以上,乳酸钠和葡萄糖也被SRB在0~12 h和12~24 h大量利用,与之相对应的是:SRB利用电子供体在0~12 h和12~24 h产生气态H2S的速率高,产生的总硫化物占总反应时间的比例大。
4. 结论
SRB对5种电子供体的利用率大小排序为:乙酸钠 + 葡萄糖 > 乙酸钠 > 葡萄糖 > 乳酸钠 > 乙醇;SRB利用不同电子供体产生H2S气体浓度高低排序为:乙酸钠 + 葡萄糖 > 乳酸钠 > 葡萄糖 > 乙醇 > 乙酸钠;SRB利用不同电子供体产生总硫化物浓度高低排序为:乙酸钠 + 葡萄糖 > 乳酸钠 > 葡萄糖 > 乙酸钠 > 乙醇。综合来看,SRB对乙酸钠和葡萄糖混合电子供体的利用率最高,利用该电子供体时所产生的气态H2S和总硫化物均比其他电子供体高。0~12 h和12~24 h为SRB厌氧产生H2S的关键阶段:在这两个反应阶段,SRB利用的电子供体最多,产生的H2S的速率最快,产生的总硫化物最多。
NOTES
*通讯作者。