1. 引言
人体在正常的生理代谢过程中会产生少量的含氧自由基,如超氧阴离子、羟自由基、单线态氧等 [1] 。在正常的生理条件下,身体产生和消除氧自由基处于动态平衡状态,但当身体的形成和自由基的消除被打破时,当体内自由基水平增加时,由于自由基具有活性并具有强氧化能力,它们可以通过一系列氧化反应。破坏细胞的结构和功能,在体内造成不可逆的氧化损伤,从而诱发各种病理损害,如动脉粥样硬化,心血管疾病,糖尿病,肿瘤等 [2] [3] [4] 。如果可以消除太多的氧自由基,则可以防止由自由基引起的许多疾病。因此,人体适当地补充外源性抗氧化剂并从体内除去过量的氧自由基,这将产生有益效果。
人工合成抗氧化剂已经广泛用于食品、饮料等消费品中,但已有证据表明合成抗氧化剂对健康有负面影响 [5] 。因此,近年来对天然抗氧化剂的研究已成为研究趋势。目前已有许多天然抗氧化剂从各种植物材料如油料作物种子、谷物、蔬菜、水果、树叶、树皮和各种中药材中获得 [6] [7] [8] 。分离活性化合物的传统方法是分离纯化植物提取物中所有化合物,然后逐一进行活性测试。这种方法不仅消耗大量的人力、物力(大量溶剂、分离用填料和样品)和时间(几个月),而且样品在分离过程中可能发生氧化反应等变化,且分离的许多化合物通常主要是无活性或活性较低的化合物。即使在活性跟踪下分离纯化也同样存在流程长、人力物力消耗大、效率较低的弊病 [9] [10] 。
本实验室自行搭建了ASE-online SPE-HPLC/MS快速筛选平台,该平台不仅可以对快速溶剂萃取仪萃取样品进行净化前处理,缩短样品前处理流程,富集痕量化学成分,减少复杂基质对质谱的污染;同时可以对未知天然成分同时分别进行质谱定性研究和馏分收集开展活性测试,为确定天然成分的种类与活性奠定基础。本文利用该平台对康定鼠尾草中的天然抗氧化活性成分开展了筛选工作,以期为该药材的开发利用提供基础。
2. 材料与方法
2.1. 材料与试剂
康定鼠尾草(Salvia prattii)采自青海省玉树藏族自治州玉树市小苏莽乡(图1)。甲醇、乙腈(色谱纯)购自云南新蓝景化学工业有限公司。
2.2. 仪器与设备
Agilent 1100-MSD液相色谱–离子阱质谱联用仪(美国安捷伦公司);ASE-350快速溶剂萃取仪(美国戴安公司);Foxy R2馏分收集器(德国Knauer公司)在线SPE系统(实验室自行研制);PL203型电子分析天平(瑞士梅特勒–托利多公司);UPT-Ⅱ-10T型超纯水机(四川优普超纯科技有限公司)。实验室自行搭建的ASE-online SPE-HPLC/MS活性筛选平台装置如图2所示。

Figure 2. Schematic diagram of the apparatus (A: ASE-350 accelerated solvent extraction instrument, B: peristatic pump, C: changeover valve 1, D: quantitative ring, E: waste liquid bottle, F: changeover valve 2, G: solid phase extraction column, H: Agilent 1100 chromatographic pump, I: mobile phase liquid storage bottle, J: chromatographic column, K: detector, L: mass spectrometer, M: plunger pump, N: elution liquid storage bottle)
图2. 设备流程图(A:ASE-350快速溶剂萃取仪,B:蠕动泵,C:切换阀1,D:定量环,E:废液瓶,F:切换阀2,G:固相萃取柱,H:Agilent 1100色谱泵,I:流动相储液瓶,J:色谱柱,K:检测器,L:质谱仪,M:柱塞泵,N:洗脱液储液瓶)
2.3. 实验方法
2.3.1. 实验流程
称取约1.0 g康定鼠尾草样品置于ASE-350快速溶剂萃取仪中萃取;萃取完成后,将萃取液泵入在线固相萃取装置,开展样品洗脱除杂;利用Agilent 1100液相色谱仪对在线固相萃取完成的样品开展分离;通过定比分流阀,40%流动相进入离子阱质谱检测,60%流动相收集到96孔板中,开展抗氧化活性测试。
2.3.2. 快速溶剂萃取条件
准确称取1.0 g康定鼠尾草样品,置于34 mL不锈钢萃取池中,以60%的甲醇溶液为提取溶剂,提取两次,提取时间6 min,提取温度75℃,压力10 MPa。
2.3.3. 在线固相萃取条件
Megres Si SPE柱(100 mm × 4.6 mm, 5 μm, 江苏汉邦科技有限公司);进样量2 mL;洗脱剂乙腈,洗脱时间3 min,流速0.5 mL/min。
2.3.4. 色谱条件
CAPCELL PAK C18 MG II色谱柱(250 mm × 4.6 mm, 5 μm, 日本资生堂公司);流动相A:乙腈-B:水(0.2% H3PO4)梯度洗脱:0~10 min,5%~10% A;10~13 min,10%~18% A;13~30 min,18%~25% A。紫外检测波长:330 nm;流速:1 mL/min;进样量10 µL,柱温:30℃。
2.3.5. 质谱条件
ESI离子源;负离子模式;雾化气N2;雾化气压力30 psi;干燥气体流速11 L/min;干燥气体温度350℃。
2.3.6. DPPH抗氧化活性筛选条件
将96孔板馏分收集器收集的馏分置于氮吹仪下吹干,加入100 μL水和100 μL DPPH储备液(50 μg/mL),摇匀后,置于暗处反应10 min,在酶标仪上于517 nm比色,测其吸光度值计算其清除率。
3. 结果与讨论
3.1. 快速溶剂萃取条件优化
快速溶剂萃取(ASE)是样品在高温和高压条件下,用有机溶剂短时间提取目标产物的一种新型样品前处理方法。与传统方法相比,ASE提取时间短、萃取效率高,有机溶剂用量少,操作简单、自动化程度高等优势。

Table 1. Results of orthogonal test
表1. 正交试验结果
在该实验中,通过正交试验优化了快速溶剂萃取中的甲醇浓度,萃取时间,萃取温度和萃取时间等参数(表1)。以康定鼠尾草中等代表性成分迷迭香酸为指标,确定快速溶剂萃取的适宜工艺条件。由表2可知,影响康定鼠尾草中迷迭香酸萃取率的各因素主次顺序为:萃取次数 > 萃取时间 > 萃取温度 > 甲醇浓度。选定最佳提取工艺为:萃取次数2次,萃取时间15 min,萃取温度75℃,甲醇浓度80%。
3.2. 在线固相萃取条件优化
本实验中比较了5种填料(Megres C18、Megres Si、Hedera C18、Hedera Si和Nucifera C18H)的固相萃取小柱(100 mm × 4.6 mm,5 μm,江苏汉邦科技有限公司)的除杂效果。结果显示,采用Megres Si固相萃取小柱时,萃取液中的小极性成分脱除效果理想,且保持了较好的色谱峰型(图3),因此选择Megres Si (100 mm × 4.6 mm, 5 μm)的固相萃取柱。

Figure 3. HPLC chromatogram of S. prattii
图3. 康定鼠尾草HPLC色谱图
实验比较了采用60%乙腈水溶液洗脱时,不同洗脱时间(3、5和7 min)的洗脱效果。结果显示,在3种洗脱时间下,萃取液中酚酸类成分的色谱峰信号响应没有显著差异,说明经过3 min的洗脱,酚酸类成分已从固相萃取小柱上完全洗脱。因此选择洗脱时间为3 min。
3.3. 抗氧化活性成分筛选与ESI-MS辨识
在ESI负离子模式中,针对雾化器压力,干燥气体流量和干燥气体温度等条件开展优化。随着雾化压力的增加,酚酸化合物的质谱检测信号变强,噪声变小;当干燥空气流量太小时,样品溶剂可能不会充分干燥,而气流太大会导致检测灵敏度降低,选择11 /min时可获得更好的质谱信号;同时,还研究了干燥气体温度对质谱信号的影响,在350℃下,质谱响应值较好(图4)。
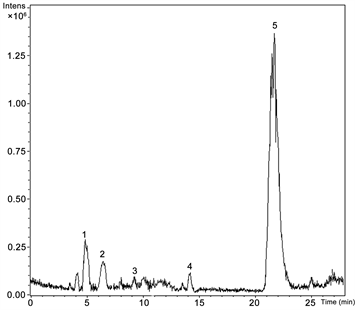
Figure 4. Total ion chromatogram of S. prattii
图4. 康定鼠尾草总离子流图
96孔板收集的馏分DPPH抗氧化活性测试结果显示,康定鼠尾草中有5个成分显示出一定的抗氧化活性(图5)。根据1~5号色谱峰的准分子离子峰、二级质谱碎片离子以及DAD光谱图信息,参考相关文献将1~5号化合物鉴定为丹参素、原儿茶醛、咖啡酸、异迷迭香酸苷和迷迭香酸(表2,图6)。

Figure 5. DPPH inhibits activity of S. prattii
图5. 康定鼠尾草DPPH抑制活性图

Table 2. Mass spectrometry information of antioxidants in S. prattii
表2. 康定鼠尾草中抗氧化活性成分的质谱信息

Figure 6. Structure of the antioxidants (1: tanshinol, 2: protocatechualdehyde, 3: caffeic acid, 4: salviaflaside, 5: rosmarinic acid)
图6. 抗氧化活性成分结构式(1:丹参素,2:原儿茶醛,3:咖啡酸,4:异迷迭香酸苷,5:迷迭香酸)
4. 结论
本研究基于ASE-online SPE-HPLC/MS快速筛选平台,建立了快速筛选康定鼠尾草中抗氧化活性成分的方法。基于谱效关系,筛选出康定鼠尾草中5个具有抗氧化活性的化合物,并通过质谱数据鉴定为丹参素、原儿茶醛、咖啡酸、异迷迭香酸苷和迷迭香酸。该方法与传统抗氧化活性成分筛选方法相比,具有前处理高效、操作简单、重现性良好等优势。该模式将活性测试与质谱鉴别相结合,更适用于从复杂基质的中藏药材中快速筛选并鉴别抗氧化活性成分,大大提高了筛选效率。
基金项目
中国科学院兰州区域中心2017年度仪器功能开发项目:基于ASE与HPLC-MSD天然活性成分筛选系统的开发(No. 2019gl09)。