1. 引言
甲壳素是世界上含量第二多的天然生物聚合物 [1],其脱乙酰基的衍生物——壳聚糖,因具有低毒性、可生物降解、生物相容、抗菌活性好等优点,使其具有广泛的应用价值 [2]。天然的壳聚糖分子由于结晶度高而呈现出“不溶性”,它仅能溶解于某些酸性水溶液,这大大地限制了它的应用范围。另一方面,壳聚糖分子中含有-NH2等化学反应活性基团,这为壳聚糖的化学改性提供了基础。近些年,有关壳聚糖改性的其它方法报道也很多,其中季铵化就是一种广泛用于改善-NH2水溶性的有效方法 [3]。Tonimar DA Senra等 [4] 通过正交实验法探索得到了获得最高季铵化度和粘度的水溶性N,N,N-三甲基壳聚糖的反应条件。孙丽萍等 [5] 通过一定的化学反应合成了季铵化羧甲基壳聚糖。通过对壳聚糖的改性为壳聚糖产品在食品、医药、化妆品等领域的实际应用提供了基础 [6] [7] [8] [9]。
壳聚糖作为自然界中唯一的碱性多糖高分子物质,也是合成开发天然高分子表面活性剂的优质原料。本文拟对壳聚糖分子中-NH2进行化学改性,通过在氮原子上引入部分的疏水烷基与亲水基团,合成制备一系列具有梳型的甜菜碱高分子两性离子表面活性剂,为壳聚糖产品的开发、应用提供一种探索。
2. 实验部分
2.1. 试剂与仪器
主要试剂:壳聚糖、乙醛、C8~C12醛、氯乙酸钠等试剂由市场采购并直接使用。
主要仪器:红外光谱仪(Avatar 370,美国 Nicolet Co.);核磁共振波谱仪(Avance 400 MHz,德国Bruker Co.);元素分析仪(Vario micro,德国Elementar Co.);视频光学接触角测量仪(OCA-20,德国Dataphysics Co.)。
2.2. 实验方法
本实验制备壳聚糖高分子表面活性剂的合成路线如图1所示。
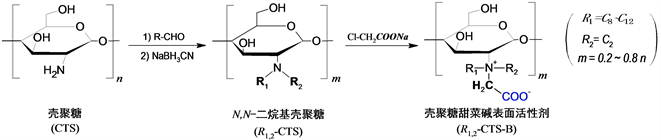
Figure 1. The synthetic route of chitosan betaine surfactants
图1. 壳聚糖甜菜碱表面活性剂(R1,2-CTS-B)的合成路线
2.2.1. N,N-二烷基壳聚糖(R1,2-CTS)的制备
实验方法及操作具体可参照文献 [10]。通过控制脂肪醛/壳聚糖的投料比,先制备得到不同烷基链长及取代度的N-单烷基壳聚糖(R1-CTS);继而用乙醛(按化学计量)重复上述反应步骤,合成制得中间体——N,N-二烷基壳聚糖(R1,2-CTS)。
2.2.2. 梳型甜菜碱型表面活性剂的制备
取定量R1,2-CTS、混合溶剂(异丙醇:水 = 4:1,v/v)于反应釜中,再加入氯乙酸钠(按实验计量),在100℃~120℃下搅拌反应12~18 h。反应结束后,先脱除溶剂得粗产品,经水洗纯化后得到黄色固体产物——壳聚糖“梳型”甜菜碱两性离子表面活性剂(R1,2-CTS-B)。
2.2.3. 羧酸基团(-COOH)含量测定
壳聚糖甜菜碱型表面活性剂(R1,2-CTS-B)采用酸碱滴定的方法对产物中-COOH含量进行测定 [11]。原理:KOH + RCOOH → RCOOK + H2O,步骤:称取一定量的产物试样(mg),用稀盐酸溶液进行酸化并干燥,再用吡啶溶解并以酚酞作指示剂,然后使用C = 0.02 mol/L的KOH乙醇溶液进行酸碱滴定,最后按以下公式计算。
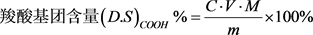
式中:V——KOH乙醇溶液消耗的体积,ml;M——中间体(R1,2-CTS-B)的摩尔质量,g/mol。
3. 结果与讨论
3.1. 产物结构表征
图2(a) (以R1 = C10为例)是壳聚糖及衍生物的红外谱图。在2920 cm−1和2856 cm−1处有明显的-CH2-伸缩振动吸收峰(尤其是R1,2-CTS与R1,2-CTS-B衍生物),这表明长链烷基已引入壳聚糖的氨基上;并且由于烷基链的引入,破环了壳聚糖部分的分子内氢键,致使游离羟基含量增加,谱图中3400 cm−1处对应的-NH2、-OH的振动吸收峰变得尖锐;谱图中1605 cm−1归属于羰基(-CO-)的伸缩振动吸收峰,由于羧基(-COOH)的引入,最终产物R1,2-CTS-B中的吸收峰更为明显。
图2(b)是壳聚糖甜菜碱型表面活性剂R10,2-CTS-B的核磁共振氢谱图,其中化学位移δ = 4.7 ppm处是溶剂D2O峰,谱图中其它各个化学位移处的峰与产物分子结构均一一对应(见图2(b)中),其中δ = 4.0 ppm对应于羧基邻位的亚甲基峰。
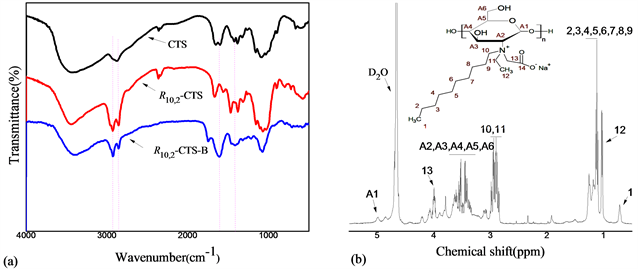
Figure 2. The IR (a) and1H NMR (b) spectrum of chitosan and its derivatives
图2. 壳聚糖及其衍生物的红外(a)与核磁共振氢谱图(b)
3.2. 烷基化反应
为获得一系列“枝链型”(不同的支链长度与支链数)的烷基壳聚糖中间体(R1,2-CTS),实验选用三种长链脂肪醛(C8、C10和C12醛)为原料,并分别合成取代度(D.S)为20%、40%、60%、80%与100%的N-单烷基壳聚糖(R1-CTS)。通过元素分析测定(C/N)值,计算出R1-CTS的单取代度及产物收率 [10],实验结果如表1所示(以R1 = C10为例)。

Table 1. The degree of substitution and yield of R1-CTS
表1. N-单烷基壳聚糖(R1-CTS)取代度及产物收率
a:癸醛/壳聚糖的摩尔比;b:括号中的数值为设计的“目标取代度”;c:收率% = 转化率% × 选择性 = 实际取代度/理论取代度 × 选择性 × 100%,选择性 = 1。
由表1可以看出,通过调整投料比可以达到设计的N-单烷基壳聚糖取代度,但100%取代度的中间产物则难以得到。同时发现R1-CTS的产率随着取代度的增加而降低,这是因为随着N-单烷基取代度的增加,分子侧链的烷基数(即支链数)增多,使空间位阻增大,导致游离氨基(-NH2)的接枝反应变得困难,致使产物收率下降。
将所有N-单烷基化壳聚糖(共12个),再与过量乙醛反应,进行第二次的还原胺化反应,取代所有R1-NH或-NH2基团中的H,并制得相应的中间体——N,N-二烷基化壳聚糖(R1,2-CTS) (其中R1 = C8、C10和C12;R2 = C2),以待后用。
3.3. 季铵化反应
中间体(N,N-二烷基化壳聚糖)经季铵化反应引入-COOH基团,生成梳型甜菜碱两性离子表面活性剂。具体的反应参数与实验结果如表2所示。

Table 2. The quaternization reaction of R10,2-CTS and the yield of products
表2. 中间体(R10,2-CTS)季铵化反应及产物收率
a:氯乙酸钠/中间体的摩尔比;b:括号中的数值为设计的“目标含量”;c:收率% = 转化率% × 选择性 = 实际取代度/理论取代度 × 选择性 × 100%,选择性 = 1。
由表2可看出,为了匹配疏水烷基的取代度,保持分子亲水/疏水的平衡性,实验通过调整反应物的投料比,来获得“对等亲水基团含量”的季铵化产物——“梳型”甜菜碱壳聚糖两性离子表面活性剂。同时发现,中间体的取代度的越大,产物季铵盐的收率越低。这是因为D.S值越大,分子中烷基侧链接枝度越高,氮原子的季铵化反应就越难,空间位阻越大,季铵化反应越难。换个角度说,要达到预设的目标含量值,反应物的投料比将逐渐增大,即意味着反应转化率的逐渐下降。
3.4. 合成产物(R1,2-CTS-B)的表面张力
图3(a)~(d)分别是取代度为20%、40%、60%、80%时,不同烷基链(C8、C10与C12)的表面张力扫描曲线。
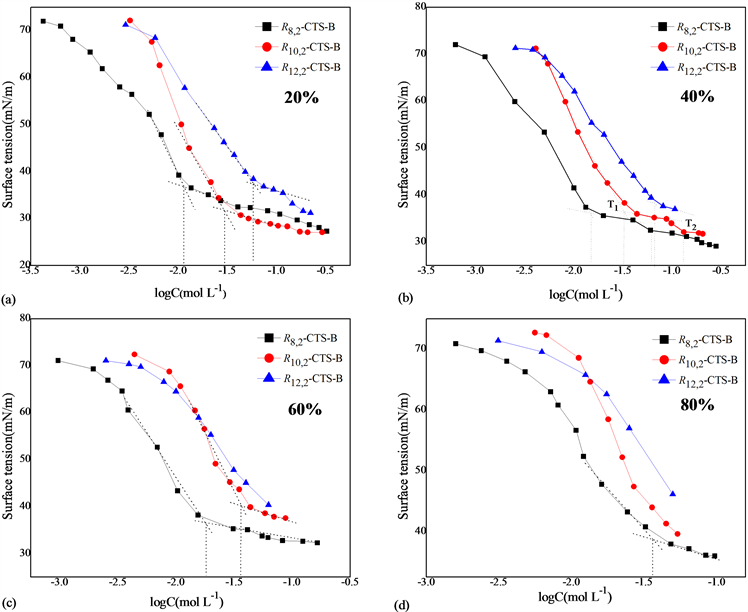
Figure 3. Surface tension curve of betaine surfactants
图3. 甜菜碱型表面活性剂(R1,2-CTS-B)的表面张力曲线
由图看出,除产物R12,2-CTS-B-80%外,其余的11个合成产物均有明显的表面活性。进一步地,随着烷基碳链增长或烷基取代度的增大,其降低表面张力的能力逐渐减弱(即最低表面张力值增大)。同时,表面张力曲线的“拐点”(c.m.c/c.a.c)越来越“模糊”或未出现,这或许是由于疏水性的增加,产物的水溶性降低,高分子链自身趋于“卷曲”,使得其在界面上的定向吸附变弱,致使表面活性下降。但当取代度较低即在40%以下时,因为烷基疏水链的引入,降低了分子内的氢键作用,高分子链在水中易于“伸展”,此时侧链的亲水、疏水结构(外形)类同于单分子表面活性剂,既易于在界面定向吸附,也能在溶液中形成分子间与分子内的“胶束”,在表面张力曲线图上出现二个“拐点”或台阶(参见图3(a)、图3(b))。另外,由图可以获知,烷基碳链为C8、C10较为适宜,相应的合成产物均具有良好的表面活性(g < 40 mN/m),尤其是当取代度为20%~40%时,产物R10,2-CTS-B-20%的表面张力值可降至27.07 mN/m,显示出优异的性能,为进一步的开发、应用提供了基础。
3.5. 产物(R1,2-CTS-B)的润湿性
接触角是反映固~液或液~液相互间润湿关系的指标之一。图4分别显示了纯水~玻璃(a)、纯水~石蜡(c)以及含R10,2-CTS-B-20%的水溶液与玻璃(b)、石蜡(d)的接触角影像。
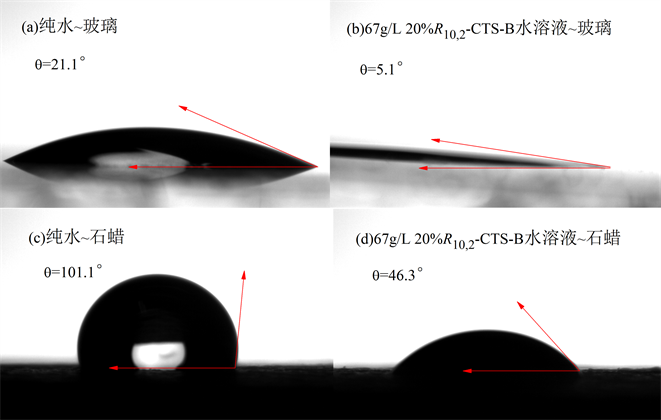
Figure 4. Contact angle of R1,2-CTS-B aq. with glass/paraffin
图4. R1,2-CTS-B水溶液与玻璃/石蜡的接触角
比较可知:含R10,2-CTS-B-20%的水溶液有着优异的润湿或渗透性,将水~玻璃界面的接触角从θ = 21.1˚降至θ = 5.1˚,下降幅度达75.8%;将水~石蜡之间的接触角降低了54.20% (由θ = 101.1˚降至θ = 46.3˚),充分表明合成制备的高分子表面活性剂具有良好的表面活性及润湿性。
4. 结论
本文以壳聚糖为原料,采用简单的化学反应,成功制得了系列化“梳型”壳聚糖甜菜碱两性离子高分子表面活性剂。通过FT-IR、1H NMR、EA对产物结构进行了表征,基于元素分析等方法测定长链烷基的取代度(即侧链枝化度)及产物的收率,实验表明,合成的产物具有典型的疏水~亲水平衡性,并显出良好的表面活性。表面张力扫描曲线表明:烷基侧链长度以C8~10最适宜,取代度控制在40%以下,产物R10,2-CTS-B-20%表面张力可降低至27.07 mN/m,同时,接触角测试结果显现出优异的湿润性,为此系列表面活性剂的后续开发、应用提供有效的基础。
NOTES
*通讯作者。