1. 引言
在肿瘤发生发展过程中,由于肿瘤抗原长期持续的刺激,T细胞表现出功能缺陷的状态 [1],包括细胞表面抑制性受体的增加,细胞因子分泌能力的降低,细胞毒作用丧失等 [2],即为T细胞耗竭状态。相关研究证实,在卵巢癌、黑色素瘤、肝癌、前列腺癌、乳腺癌等肿瘤中均存在PD1+的肿瘤浸润T细胞(tumor infiltrating lymphocytes, TILs),其产生细胞因子的能力及细胞毒活性均下降 [3],且其他转移病灶中的T细胞也可出现功能缺失,不能有效分泌细胞因子,同时PD-1、CTLA-4和TIM-3等抑制性受体明显上调 [4]。临床治疗上,可通过单克隆抗体封闭PD-1、TIM-3的方式恢复T细胞功能,从而达到逆转T细胞耗竭的 [5]。但抗PD-1和TIM-3抗体价格昂贵,且在不同的研究中其作用也存在较大差异。
中医治疗肿瘤的历史悠久,中草药可能是逆转T细胞耗竭的途径。《黄帝内经》云:“正气存内,邪不可干,邪之所凑,其气必虚”,认为肿瘤的发生与正气不足有关。而“正气”相当于机体的免疫功能,T细胞在其中发挥着不可缺少的作用。T细胞耗竭,其介导的免疫应答减弱,肿瘤细胞发生免疫逃逸,形成实体瘤。与祖国医学的“积之成也,正气之虚也,正气虚而后积成”不谋而和。因此“扶正抗癌”贯穿于肿瘤的治疗始终,即所谓的“养正积自消”。“扶正”能调动机体的免疫功能,从而对体液、细胞免疫及细胞因子活性起到增强作用。
本研究通过构建Lewis肺癌荷瘤鼠模型,拟采用具有养阴扶正作用的养阴扶正汤来逆转肺癌荷瘤鼠的T细胞耗竭,探索中医临床治疗肿瘤T细胞耗竭的思路。
2. 材料与方法
2.1. 动物及试剂
Lewis肺癌细胞株购自武汉博士德生物工程有限公司。C57BL/6小鼠(6~8周龄,雄性,SPF级,20 ± 2 g/只)购于黑龙江中医药大学实验动物中心[证书编号:SYXK(黑)2016004]。本实验通过《齐齐哈尔市第一医院试验动物管理办法(试行)》伦理审核(NO. 2018-01)。小鼠IL-2、IFN-γ、IL-10、TGF-β ELISA检测试剂盒购自武汉博士德生物工程有限公司。养阴扶正汤购自齐齐哈尔市第一医院。PD-L1抑制剂(阿特珠单抗,Atezolizumab)购自罗氏基因泰克公司。
2.2. 方法
2.2.1. 养阴扶正汤的制备方法
黄芪30 g、党参20 g、沙参30 g、天冬12 g、麦冬15 g、生白术15 g、山药30 g、白花蛇舌草30 g、拳参30 g、绞股蓝15 g、茯苓20 g、莪术15 g。添加10倍量水,浸泡30 min后,于中药煎药壶中煎煮60 min,用纱布过滤。残余药渣中再添加10倍量水,再煎煮60 min后纱布过滤。合并滤液并旋转蒸发浓缩至含生药浓度5.25 g/ml,4℃存放,备用。以上药材由齐齐哈尔市第一医院制剂室提供,并经过该院药剂科鉴定。
2.2.2. PD-L1+Lewis肺癌荷瘤鼠模型的建立
体外培养Lewis肺癌细胞系,待细胞至增殖期,应用免疫磁珠筛选出PD-L1+Lewis肺癌细胞系。将PD-L1+Lewis肺癌细胞系及Lewis肺癌细胞系分别传代培养,将密度为2 × 1010个/L的PD-L1+Lewis肺癌细胞悬液及Lewis肺癌细胞悬液分别接种于小鼠右侧腋窝皮下(0.2 ml/只),分别构建PD-L1+Lewis肺癌荷瘤鼠模型及Lewis肺癌荷瘤鼠模型。接种10 d后,待皮下移植瘤长至1 cm3左右,剥取1只皮下移植瘤行病理检测均为癌细胞,说明造模成功。
2.2.3. 实验分组
将造模成功的荷瘤鼠按随机数字表法分为以下8组,每组6只:A) PD-L1+Lewis肺癌荷瘤鼠分组:模型组、PD-L1抑制剂组(阿特珠单抗)、养阴扶正汤组、联合组(养阴扶正汤 + 阿特珠单抗);B) Lewis肺癌荷瘤鼠分组:模型组、PD-L1抑制剂组(阿特珠单抗)、养阴扶正汤组、联合组(养阴扶正汤 + 阿特珠单抗)。
2.2.4. 给药方式
1) 模型组:0.2 mL生理盐水、灌胃、共10 d,第1 d、3 d、5 d生理盐水0.4 mL、腹腔注射。
2) PD-L1抑制剂组:0.2 mL生理盐水、灌胃、共10 d,第1 d、3 d、5 d阿特珠单抗0.4 ml (60 mg/kg)、腹腔注射。
3) 养阴扶正汤组:0.2 ml养阴扶正汤(52 g/kg/d)、灌胃、共10 d,第1 d、3 d、5 d生理盐水0.4 mL、腹腔注射。
4) 联合组:0.2 ml养阴扶正汤(52 g/kg/d)、灌胃、共10 d,第1 d、3 d、5 d阿特珠单抗0.4 ml (60 mg/kg)、腹腔注射。
2.2.5. 荷瘤小鼠脾脏单个淋巴细胞的分离
停药第2日颈椎脱臼处死各组荷瘤小鼠,取出脾脏。无菌分离荷瘤小鼠脾脏单个淋巴细胞,加入1 ml含有双抗和胎牛血清的完全RPMI1640培养液。用牛鲍氏计数板进行细胞计数,调整所需的细胞浓度为1 × 107 cells/ml。
2.2.6. 荷瘤小鼠脾单个淋巴细胞分泌IL-2、IFN-γ、IL-10、TGF-β的水平检测
取已调整好细胞计数的脾单个淋巴细胞悬液1 ml铺入24孔板,按照试剂盒的说明书进行操作,酶标仪450 nm处读取OD值,检测细胞因子IL-2、IFN-γ、IL-10、TGF-β的水平。
2.3. 数据分析
应用Excel2007进行数据处理,t检验比较两组之间的差异。以P < 0.05定义为差异有统计学意义。
3. 结果
1) 养阴扶正汤治疗组PD-L1+Lewis肺癌荷瘤鼠及Lewis肺癌荷瘤鼠脾淋巴细胞分泌IL-2、IFN-γ水平均增高。
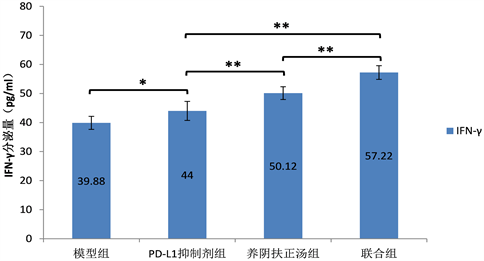
将PD-L1+Lewis肺癌各组荷瘤小鼠脾淋巴细胞悬液均匀铺于24孔板中,ELISA检测上清中IL-2、IFN-γ的含量,结果如图1、图2所示。比较PD-L1+Lewis肺癌荷瘤鼠模型组、PD-L1抑制剂组、养阴扶正汤组及联合组中IL-2、IFN-γ的含量显示,养阴扶正汤组及联合组IL-2、IFN-γ分泌量较模型组、PD-L1抑制剂组明显上升,差异具有统计学意义(P < 0.01)。将Lewis肺癌各组荷瘤小鼠脾淋巴细胞悬液均匀铺于24孔板中,ELISA 检测上清中IL-2、IFN-γ的含量,结果如图3、图4所示。比较PD-L1+Lewis肺癌荷瘤鼠模型组、PD-L1抑制剂组、养阴扶正汤组及联合组中IL-2、IFN-γ的含量显示,养阴扶正汤组及联合组IL-2、IFN-γ分泌量较模型组、PD-L1抑制剂组明显上升,差异具有统计学意义(P < 0.01)。比较PD-L1+Lewis肺癌及Lewis肺癌各组荷瘤小鼠脾淋巴细胞悬液IL-2、IFN-γ的含量,结果如图5、图6所示,差异无统计学意义(P > 0.05)。
 注:**P < 0.01。
注:**P < 0.01。
Figure 1. The levels of IL-2 secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines (n = 6)
图1. PD-L1+Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IL-2的水平(n = 6)
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 2. The levels of IFN-γ secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines (n = 6)
图2. PD-L1+Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IFN-γ的水平(n = 6)
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 3. The levels of IL-2 secreted by spleen lymphocytes of mice with tumor transplanted by Lewis lung cancer cell lines (n = 6)
图3. Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IL-2的水平(n = 6)
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 4. The levels of IFN-γ secreted by spleen lymphocytes of mice with tumor transplanted by Lewis lung cancer cell lines (n = 6)
图4. Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IFN-γ的水平(n = 6)
 注:#P > 0.05。
注:#P > 0.05。
Figure 5. The levels of IL-2 secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines and transplanted by Lewis lung cancer cell lines (n = 6)
图5. PD-L1+Lewis肺癌细胞株及Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IL-2的水平(n = 6)
 注:#P > 0.05。
注:#P > 0.05。
Figure 6. The levels of IFN-γ secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines and transplanted by Lewis lung cancer cell lines (n = 6)
图6. PD-L1+Lewis肺癌细胞株及Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IFN-γ的水平(n = 6)
2) 养阴扶正汤治疗组PD-L1+Lewis肺癌荷瘤鼠及Lewis肺癌荷瘤鼠脾淋巴细胞分泌IL-10、TGF-β水平均降低
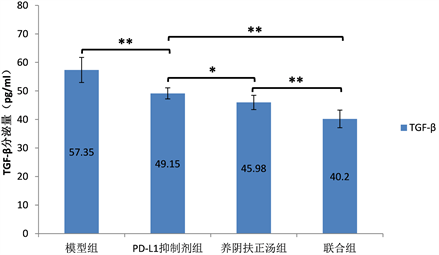
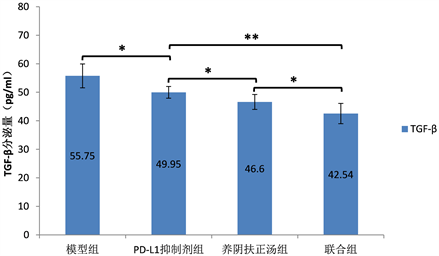
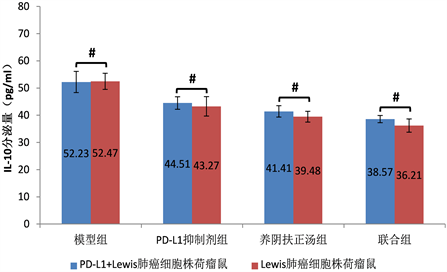
将PD-L1+Lewis肺癌各组荷瘤小鼠脾淋巴细胞悬液均匀铺于24孔板中,ELISA检测上清中IL-10、TGF-β的含量,结果如图7、图8所示。比较PD-L1+Lewis肺癌荷瘤鼠模型组、PD-L1抑制剂组、养阴扶正汤组及联合组中IL-10、TGF-β的含量显示,养阴扶正汤组及联合组IL-10、TGF-β分泌量较模型组、PD-L1抑制剂组明显降低,差异具有统计学意义(P < 0.01)。将Lewis肺癌各组荷瘤小鼠脾淋巴细胞悬液均匀铺于24孔板中,ELISA检测上清中IL-10、TGF-β的含量,结果如图9、图10所示。比较PD-L1+Lewis肺癌荷瘤鼠模型组、PD-L1抑制剂组、养阴扶正汤组及联合组中IL-10、TGF-β的含量显示,养阴扶正汤组及联合组IL-10、TGF-β分泌量较模型组、PD-L1抑制剂组明显降低,差异具有统计学意义(P < 0.01)。比较PD-L1+Lewis肺癌及Lewis肺癌各组荷瘤小鼠脾淋巴细胞悬液IL-10、TGF-β的含量,结果如图11、图12所示,差异无统计学意义(P > 0.05)。
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 7. The levels of IL-10 secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines (n = 6)
图7. PD-L1+Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IL-10的水平(n = 6)
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 8. The levels of TGF-β secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines (n = 6)
图8. PD-L1+Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌TGF-β的水平(n = 6)
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 9. The levels of IL-10 secreted by spleen lymphocytes of mice with tumor transplanted by Lewis lung cancer cell lines (n = 6)
图9. Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IL-10的水平(n = 6)
 注:**P < 0.01,*P < 0.05。
注:**P < 0.01,*P < 0.05。
Figure 10. The levels of TGF-β secreted by spleen lymphocytes of mice with tumor transplanted by Lewis lung cancer cell lines (n = 6)
图10. Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌TGF-β的水平(n = 6)
 注:#P > 0.05。
注:#P > 0.05。
Figure 11. The levels of IL-10 secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines and transplanted by Lewis lung cancer cell lines (n = 6)
图11. PD-L1+Lewis肺癌细胞株及Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌IL-10的水平(n = 6)
 注:#P > 0.05。
注:#P > 0.05。
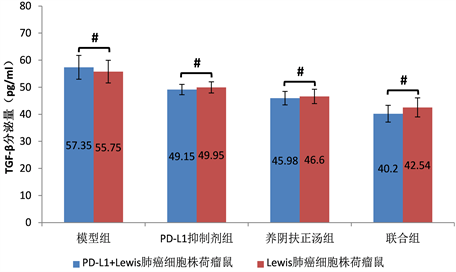
Figure 12. The levels of TGF-β secreted by spleen lymphocytes of mice with tumor transplanted by PD-L1+Lewis lung cancer cell lines and transplanted by Lewis lung cancer cell lines (n = 6)
图12. PD-L1+Lewis肺癌细胞株及Lewis肺癌细胞株各组荷瘤鼠脾淋巴细胞分泌TGF-β的水平(n = 6)
4. 讨论
T细胞的耗竭是一个动态发展的过程,随着耗竭严重程度的增加,T细胞表面抑制性受体表达的数量和种类也逐渐增多 [6] [7]。PD1通路中的PD1及其配体PD-L1是T细胞耗竭过程中主要的抑制性受体,在T细胞耗竭过程中起到极其重要的作用。PD-L广泛表达在肺癌、乳腺癌、肝癌、卵巢癌等癌组织上,而肿瘤邻近的正常组织中仅呈现低水平表达,故提示其可能参与肿瘤发生发展 [8]。当T细胞表面的PD-1与肿瘤细胞表面的配体PD-L耦联后,导致下游信号受到抑制,进而减弱对免疫细胞的活化作用 [9],最终抑制T淋巴细胞增殖和相关细胞因子的分泌。T细胞耗竭早期,表现为分泌IL-2的能力下降及T细胞的增殖、体外杀伤能力的下降。进展至耗竭晚期,IFN-γ产生能力显著受损 [10],直至最终T细胞死亡。
同时,T细胞耗竭过程中,IL-10、TGF-β等细胞因子的分泌能力增加。IL-10和T细胞功能缺失有关,阻断IL-10可以促进T细胞反应,增强其功能 [11]。TGF-β也可促进T细胞耗竭发生,阻断T细胞接收TGF-β信号的能力可以提高CD8+T细胞功能,阻止T细胞耗竭发生 [11]。
T细胞耗竭导致机体的细胞免疫功能障碍,进而导致免疫功能低下。临床上,养阴扶正方常用于调节肿瘤晚期患者的免疫功能。本研究中的方剂成分由沙参、天冬、麦冬、黄芪、党参、生白术、茯苓、山药、拳参、白花蛇舌草、绞股蓝、莪术构成,具有滋阴、免疫调节的功效。方剂中沙参、天冬、麦冬为滋阴扶正常用中药。药理试验证明,沙参粗多糖可增强阴虚小鼠脾脏NK细胞杀伤率和T淋巴结细胞转化功能,增加血清IgG和IgM含量,进而增强特异性免疫及非特异性免疫功能 [12]。麦冬多糖能通过调节IL-2、TNF-α、IFN-γ及IL-10的表达增强免疫功能。临床研究证实,“脾虚”时消化功能紊乱,机体免疫功能下降。方剂中的黄芪、党参、生白术、茯苓、山药亦均具有补脾益气、增强机体免疫功能的作用。药理实验证明,黄芪多糖可通过激活TLR4介导的MyD88依赖性信号传导途径来调节宿主生物的免疫功能 [13]。党参多糖可通过增加小鼠巨噬细胞系细胞中TNF-α和IL-6分泌参与机体的免疫调节 [14]。白术多糖 [15] 能有效的促进小鼠脾脏淋巴细胞增殖,且对细胞因子IL-2、IL-10、TGF-β1的分泌具有明显的促进作用。茯苓多糖能增强细胞免疫和体液免疫 [16]。山药多糖可促进淋巴细胞转化,有增强免疫的作用 [17]。另外,方剂中的白花蛇舌草、绞股蓝、莪术的现代药理学研究均显示有抗肿瘤作用。养阴扶正汤中的各味汤药合用,既可调节免疫功能,亦可抗肿瘤。其调节免疫功能的作用,均与免疫增强有关,该方剂对T细胞耗竭具有一定的调节作用。
本研究PD-L1+Lewis肺癌荷瘤鼠模型经养阴扶正汤治疗后,T细胞分泌IL-2和IFN-γ的能力显著增强,而分泌IL-10、TGF-β的能力显著减弱。其作用机制可能是通过下调 T 细胞耗竭信号上游分子PD-1的表达,阻止耗竭T细胞免疫抑制信号的传递,进而逆转T细胞耗竭状态,恢复T细胞功能。因此,养阴扶正汤有望成为有效逆转PD-1+T细胞耗竭的中药方剂。
参考文献
NOTES
*第一作者。