1. 前言
B4C具有高硬度(仅次于金刚石和立方氮化硼)、低密度(2.52 g/cm3)、高熔点(2450℃)以及高中子吸收截面(600b)等优点,广泛应用于防弹材料、耐磨和自润滑材料、切割研磨工具、防辐射材料和原子反应堆控制和屏蔽材料等;军火工业中可用作制造枪炮喷嘴 [1] [2] [3] [4]。工业生产B4C的方法是电弧炉碳热还原法,即首先矿热炉碳热还原得到碳化硼结晶块,经破磨,湿法酸洗净化得到碳化硼粉体,该工艺存在粒度大(微观晶粒尺寸10~20 µm,微米级碳化硼超微粉 < 2.0 µm)、杂质含量高、烧结活性差等缺馅,且破碎磨细过程 [5] [6] [7] 造成二次污染,导致产品纯度下降。激光诱导化学气相沉积法是以含有碳源及硼源的气体(BCl3、B2H6、CHCl3、CH4等)为原料,在激光辐射下混合气体迅速升温反应生成B4C纳米颗粒,再经过处理得到具有纯净的纳米B4C粉 [8]。溶胶–凝胶法也是制备B4C超细粉的一种新方法,Sinha用硼酸/柠檬酸凝胶前驱体在1000℃~1450℃保温2 h,得到平均粒径为2.25 µm的B4C微粉 [9]。目前,B4C超细微粉制备仍旧是研究热点和难点,其制备技术只有少数几个国家掌握。燃烧合成法作为一种超细粉体的方法,制备的粉体具有高活性等优点 [9] - [15]。本文系统研究了工艺条件对燃烧合成制备B4C粉体品质的影响。
2. 实验
2.1. 实验步骤
按比例称量氧化硼,镁粉,碳粉,混匀并压制成块体;然后将压块置于自蔓延反应器中以镁粉为引燃剂点燃,冷却至室温收集燃烧产物;接着将燃烧产物进行盐酸浸出;最后过滤、洗涤、干燥得到B4C粉体。浸出条件:浸出温度为80℃,搅拌转速为200 rmp,浸出时间为2 h,固液比为1:15,盐酸浓度为6 mol/L。
2.2. 检测分析
釆用德国Bruker公司的D8型X-射线衍射仪对燃烧产物和浸出产物进行物相分析,采用Cu-Kα射线,扫描范围10˚~90˚,扫描速度为8˚/min,步长为0.01˚;采用日立SU-8010型扫描电子显微镜对燃烧产物和浸出产物进行微观形貌分析,扫描电压10 KV;采用Malvern MS2000粒度分析仪对浸出产物进行粒度表征。
3. 结果与讨论
3.1. B2O3-Mg-C反应的热力学分析
对于一定的反应体系,只有绝热温度大于1800 K时,反应才能以自蔓延方式自我维持进行。对于自蔓延的反应体系:
:
式中,
为体系的热效应,由于假设该体系与外界无热量的交换,所以其值为0。
为在298 K时反应的标准摩尔反应焓变,由反应物与产物的标准摩尔生成焓相减得,单位是kJ∙mol−1;
为产物在温度T下的热容,单位是J∙K−1∙mol−1。
可近似的用以下公式计算:
A1,A2,A3,A4,A5可由无机热力学数据手册査得。
对于
,
,
解得,
,反应能以自蔓延反应模式自发维持发生。
(1)
(2)
(3)
(4)
(5)
(6)
(7)
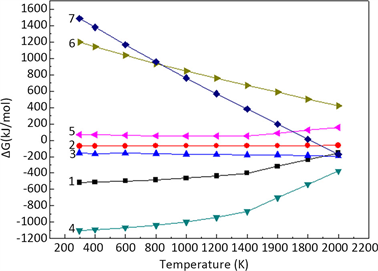
Figure 1. The Gibbs free energy changes of the SHS reaction
图1. 自蔓延反应过程中可能反应的吉布斯自由能变
由图1知,反应5、6在所研究的温度范围内反应的吉布斯自由能变均 > 0,反应无法发生;反应2的吉布斯自由能变随温度升高而增大,但均 < 0,说明反应可以发生;反应7需要在高温下才能发生;反应4的吉布斯自由能变是最负的,说明反应最容易发生。
3.2. B2O3配料量对燃烧合成反应的影响
考察B2O3配料量对自蔓延反应结果的影响,试验条件:压块压力为20 MPa、球磨时间为30 min、球料比为4、球磨转速为150 rpm。图2为不同B2O3配料量时燃烧产物的SEM照片,其中,(1) 为B2O3配料量过量5%,(2) 为B2O3配料量过量10%,(3) 为化学计量比。由图2可看出,燃烧产物中充满了孔洞和孔隙,且出现分层现象。其中,白色颗粒为MgO,黑色基体主要为Mg3B2O6和B4C的混合物。

Figure 2. SEM photographs of combusted products at different B2O3 contents; (1) Excess 5% B2O3; (2) Excess 10% B2O3; (3) Stoichiometric ratio
图2. 不同B2O3含量下的燃烧产物的SEM照片;(1) B2O3过量5%;(2) B2O3过量10%;(3) 化学计量比
燃烧产物出现分层和孔洞可以认为是如下原因所致:1) 试样燃烧时呈不稳定模式,即出现周期性燃烧波运动停止。燃烧波宏观上快位移和慢位移交替现象,使燃烧产物出现明显的宏观分层;2) 反应高温度原料中易挥发的物质(Mg和B2O3)以及原料所吸附水分的蒸发造成的孔洞;3) 随着反应温度的升高,B2O3融化在毛细作用下进入试样的空隙中,B2O3原来的位置变成了孔隙。由图2可知,随着B2O3配料量的增加,孔隙和分层现象越来越不明显。因为B2O3配料量的增加,过量B2O3的存在会在高温反应过程中形成液相烧结。另外,Mg被氧化生成MgO,而MgO的熔点很高,固化的MgO因表面能作用而收缩成团。
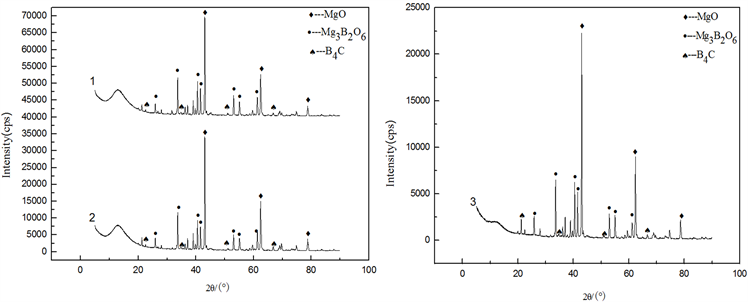
Figure 3. XRD patterns of combusted products at different B2O3 contents; (1) Excess 5% B2O3; (2) Excess 10% B2O3; (3) Stoichiometric ratio
图3. 不同B2O3含量下的燃烧产物XRD图谱;(1) B2O3过量5%;(2) B2O3过量10%;(3) 化学计量比
图3是不同B2O3配料量时燃烧产物的XRD图谱,其中,(1) 为B2O3配料量过量5%,(2) 为B2O3配料量过量10%,(3) 为化学计量比。由图3知,燃烧产物主要由MgO、Mg3B2O6和B4C组成。随着B2O3配料量的增加,Mg3B2O6的衍射峰相对强度增加,说明B2O3过量使反应中生成Mg3B2O6的几率增加。由此,推测自蔓延合成反应机理为:
(8)
(9)
图4是不同B2O3配料量下的浸出产物的SEM照片,其中,(1) 为B2O3配料量过量5%,(2) 为B2O3配料量过量10%,(3) 为化学计量比。由图4可知,B4C颗粒大小不均匀,一部分颗粒生长较大,另一部分颗粒还未完全长大。分散的单颗粒B4C呈立方体,这与B4C为立方型晶体非常吻合。小颗粒的表面能比大颗粒的表面能大,使得小颗粒之间的吸附能增加而团聚在一起,这些团聚的小颗粒呈多孔的蜂窝状。

Figure 4. SEM photographs of leached products at different B2O3 contents; (1) Excess 5% B2O3; (2) Excess 10% B2O3; (3) Stoichiometric ratio
图4. 不同B2O3配料量的浸出产物的SEM照片;(1) B2O3过量5%;(2) B2O3过量10%;(3) 化学计量比
图5为不同B2O3配料量时浸出产物的XRD图谱,其中,(1) 为B2O3过量5%,(2) 为B2O3过量10%,(3) 为B2O3理论配料量。由图5可知,浸出产物主要由B4C、BxCy相和少量的Mg3B2O6组成,少量的Mg3B2O6相的存在,说明浸出除杂条件不够充分。
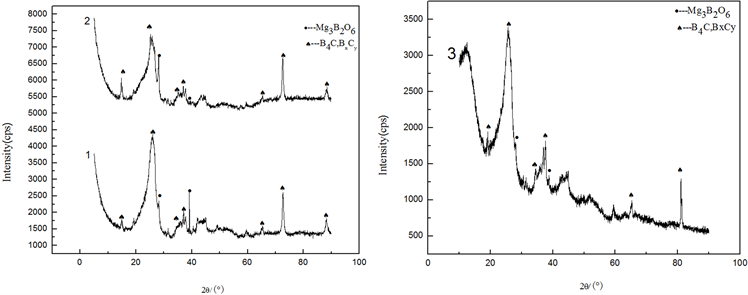
Figure 5. XRD patterns of leached products at different B2O3 contents; (1) Excess 5% B2O3; (2) Excess 10% B2O3; (3) Stoichiometric ratio
图5. 不同B2O3配料量的浸出产物的XRD图谱;(1) B2O3过量5%;(2) B2O3过量10%;(3) 化学计量比
由此推测浸出反应机理如下:
(10)
(11)
不同B2O3配料量时的浸出产物中Mg和C化学分析结果如表1所示。可知,浸出产物中C含量与B4C中C理论含量21.73%存在比较大差距。

Table 1. Mg and C content of leached products at different B2O3 contents
表1. 不同B2O3配料量浸出产物的Mg和C含量
图6为不同B2O3配料量的浸出产物的粒度分布,其中,(1) 为B2O3过量5%,(2) 为B2O3过量10%,(3) 为B2O3理论配料量。其D50依次为20.132 µm、19.741 µm和19.301 µm。平均粒径过大,与晶粒发育不完整,团聚现象严重有关。结合图4的SEM照片可知,碳化硼粉体的单体颗粒多数在3 µm以下,因此燃烧合成法制备微米级碳化硼颗粒是可行的。
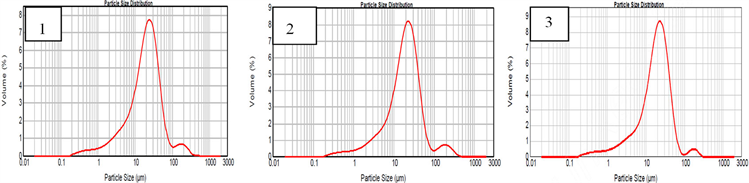
Figure 6. Particle size distribution curve of at different B2O3 contents; (1) Excess 5% B2O3; (2) Excess 10% B2O3; (3) Stoichiometric ratio
图6. 不同B2O3配料量的浸出产物粒度分布曲线;(1) B2O3过量5%;(2) B2O3过量10%;(3) 化学计量比
3.3. 制样压力对燃烧合成反应的影响
反应条件:球料比为4、原料配比B2O3:Mg:C (摩尔比)为2.1:6:1时,考察了坯样压力对燃烧合成反应的影响。图7是不同压块压力下的燃烧产物XRD图谱,其中,(1) 为制样压力20 MPa,(2) 为制样压力40 MPa,(3) 为制样压力60 MPa,(4) 为制样压力80 MPa。由图7可知,随着坯样压力的增大,燃烧产物中MgO和Mg3B2O6的衍射峰相对强度上升,但60 MPa时MgO和Mg3B2O6的衍射峰相对强度均略低于40 MPa时衍射峰的强度,但仍高于20 MPa时MgO和Mg3B2O6的衍射峰强度,适当的坯样制样压力可促进反应进行,但是坯样压力不宜过大。图8是不同压块压力时浸出产物的SEM照片,随着坯样压力的增加,浸出产物的粒度逐渐变小,但过大的制样压力会导致产品粒度分布变的不均匀。
图9是不同坯样压力时浸出产物的XRD图谱,其中,(1) 为坯样压力的20 MPa,(2) 为坯样压力40 MPa,(3) 为坯样压力60 MPa,(4) 为坯样压力80 MPa。由图9可知,浸出产物主要为B4C相,还有BxCy相以及少量的Mg3B2O6相。少量的Mg3B2O6相存在说明浸出除杂效果不充分。随着压块压力的增加各物相衍射峰先随之下降后上升,说明坯样压力的增加,对燃烧反应是先抑制后促进。
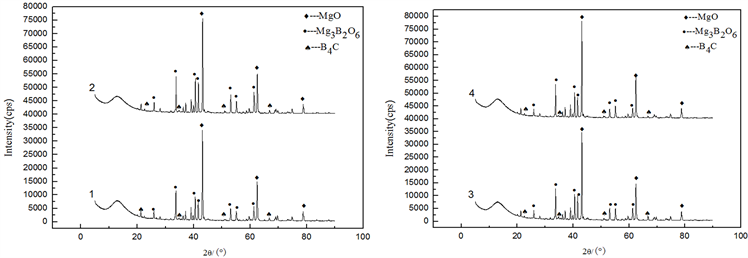
Figure 7. XRD patterns of combusted products at different sample preparation pressures; (1) 20 MPa; (2) 40 MPa; (3) 60 MPa; (4) 80 MPa
图7. 不同压块压力下的燃烧产物XRD图谱;(1) 压力20 MPa;(2) 压力40 MPa;(3) 压力60 MPa;(4) 压力80 MPa


Figure 8. SEM photographs of combusted products at different sample preparation pressures; (1) 20 MPa; (2) 40 MPa; (3) 60 MPa; (4) 80 MPa
图8. 不同压块压力下的浸出产物的SEM照片;(1) 压力20 MPa;(2) 压力40 MPa;(3) 压力60 MPa;(4) 压力80 MPa
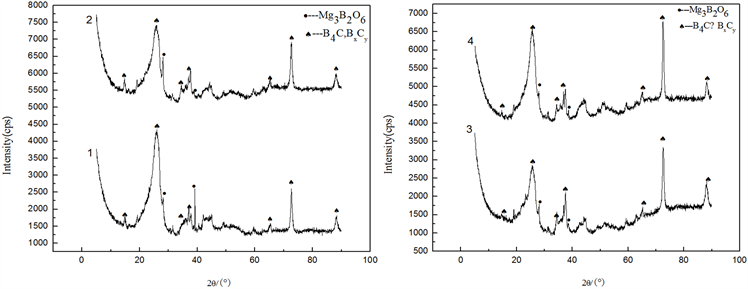
Figure 9. XRD patterns of leached products at different sample preparation pressures; (1) 20 MPa; (2) 40 MPa; (3) 60 MPa; (4) 80 MPa
图9. 不同压块压力下的浸出产物的XRD图谱;(1) 压力20 MPa ;(2) 压力40 MPa;(3) 压力60 MPa;(4) 压力80 MPa

Table 2. Mg and C content of leached products at different sample preparation pressures
表2. 不同压块压力浸出产物的Mg和C含量
由表2可知,随着坯样压力的增加,浸出产物中碳含量先降低后上升,表明一定范围内压块压力的增加会相应的减少最终产物中碳的含量,使碳的含量逐渐趋于生成碳化硼时的理论值,坯样压力为60 MPa时,产品中C含量为23.4%,与B4C中21.73%的理论碳含量接近。从反应现象看:随着坯样压力的增加,燃烧产物从完整的块状变成小碎块,适当的增加坯样压力可促进反应进行,但过高的坯样压力会导致反应引发困难,而且一旦引发反应会十分剧烈,造成严重的喷溅,一旦喷溅炸裂会导致体系温度快速降低,不利于反应转化。
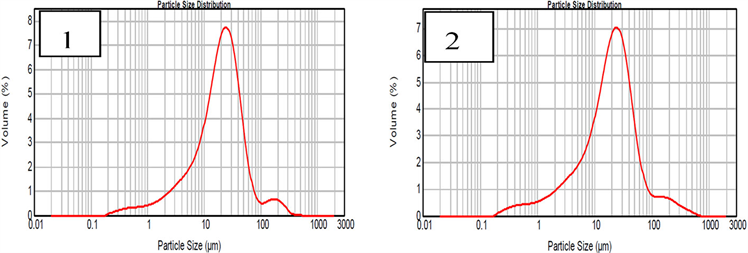
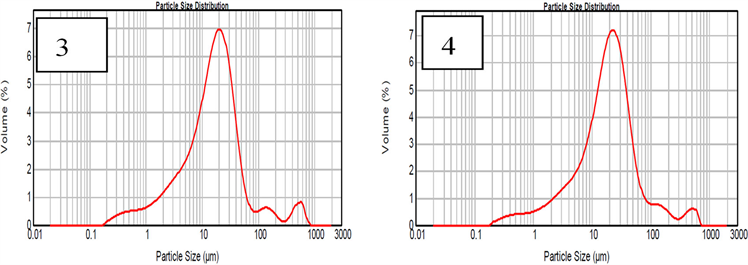
Figure 10. Particle size distribution curve at different sample preparation pressures (1) 20 MPa, (2) 40 MPa, (3) 60 MPa, (4) 80 MPa
图10. 不同坯样压力时浸出产物的粒度分布曲线;(1) 压力20 MPa;(2) 压力40 MPa;(3) 压力60 MPa;(4) 压力80 MPa
如图10所示为不同坯样压力的浸出产物粒度分布曲线,其中,(1) 为压力20 MPa,(2) 为压力40 MPa,(3) 为压力60 MPa,(4) 为压力80 MPa。由图可知,其D50依次为20.132 µm、19.776 µm、16.276 µm和19.180 µm。随着坯样压力的增加,浸出产物的粒度先减少后增加。由其粒度分布曲线对比可看出,随着坯样压力增大其粒度分布向两侧分散。说明在坯样压力为40~80 MPa时浸出产物的平均粒径D50值最小。
4. 结论
1)
体系的绝热温度为2750 K,大于1800 K的热力学判据,说明反应可以自我维持发生。燃烧产物主要由B4C、MgO以及少量Mg3B2O6相组成;采用盐酸浸出可有效除去其中的MgO和Mg3B2O6相,得到B4C粉体。
2) 随氧化硼配料量增加可降低产品中的Mg含量,但对产物粒度无明显影响;坯样压力为60 MPa时,浸出产物中C含量为23.4%,与B4C中C理论含量21.73%接近,此时平均粒径为16.276 µm。