1. 引言
天然气水合物作为一种新兴能源,具有储量大、热值高和燃烧污染小等优点,被认为是21世纪最具有开采价值的环境友好型化石能源。它由水分子和一些被称为客体分子的小分子量气体在低温高压的环境下生成,已有的研究表明,甲烷、乙烷、二氧化碳以及液相的四氢呋喃等均可与水分子生成水合物,并可根据生成水合物微观结构的不同而分为1型,2型和H型水合物 [1] [2] [3]。
在标准状态下,1体积的水合物可以储存164~180体积的甲烷气体 [4],因此,其优良的气体储存能力以及安全性使其在工业应用领域扮演越来越重要的角色,比如天然气的储存与运输、气体分离、二氧化碳捕集、海水淡化以及制冷等行业 [5] [6] [7] [8]。研究表明,改善水合物生成过程中的传热传质条件,能够显著地加快其生成速度 [9]。而多孔介质和表面活性剂的加入则可以通过增加水合物生成体系传热能力和降低气液界面表面张力的方式改善该体系的传热和传质条件 [10] [11],进而改善水合物的生成情况;Linga等 [12] 分别在硅砂颗粒内和纯水中进行水合物生成实验,结果表明,在硅砂中水合物的生成速率明显比水溶液中高。Mohammadi等 [13] 分别在纳米银颗粒与SDS (十二烷基硫酸钠)的单一体系和两者的复配体系中进行了水合物的生成实验,最终发现该复配体系中气体的消耗量提升较大。周诗岽等 [14] 则通过将纳米石墨颗粒和SDS (十二烷基硫酸钠)复配来研究其对诱导时间的影响,结果表明,两者的引入可以使水合物生成的诱导时间相对于纯水体系明显缩短,并且其效果较于相同量的单一添加剂更好。
目前,关于对水合物在多孔介质颗粒和表面活性剂溶液中生成特性的研究较多,也有着较为丰硕的研究成果,但是,对于水合物两者共存体系中的生成情况,尤其是在多孔介质孔隙环境下水合物的生成特点和表面活性剂对水合物的促进机理,目前的研究仍有待加强。为此,本文通过采用不同粒径的氧化铝和二氧化硅颗粒,研究了该条件下水合物在纯水和表面活性剂十二烷基苯磺酸钠(SDBS)溶液中的生成特性,探讨了多孔介质颗粒粒径,多孔介质种类以及表面活性剂的存在对于水合物生成促进的影响,有利于实现水合物的快速生成进而促进水合物的工业应用。
2. 实验部分
2.1. 实验材料
粒径为分别为100,200,300目的硅砂颗粒和氧化铝颗粒,天然气(甲烷纯度 ≥ 84.6%),由沈阳科瑞特种气有限公司提供;去离子水,实验室自制;十二烷基苯磺酸钠(SDBS),纯度 ≥ 90.0%,由青岛优索化学科技有限公司提供,规格为5.5 cm × 6.5 cm的塑料容器,材质为聚对苯二甲酸乙二醇酯(PET)。
2.2. 实验仪器

Figure 1. Experimental apparatus for hydrate dynamics
图1. 水合物动力学实验装置
为模拟水合物生成过程,需要达到水合物生成所需的温压条件,即通过调整反应釜中气液两相的温度压力条件以生成水合物,因此本文采用图1所示的实验装置进行水合物生成过程的模拟。该装置主要由高压反应釜、恒温水浴、温压传感器、数据采集系统组成,反应釜材料为不锈钢,有效容积350 ml,最高工作压力为25 MPa,工作温度范围−10℃~90℃。反应釜的温度由恒温水浴控制,恒温水浴的控制精度为0.1℃。釜内的温度由两个100/3铂电阻测量,精度为0.1℃,反应釜内的压力传感器测量范围0~30 MPa,精度为0.01 MPa。
该水合物生成动力学装置主要分为三个模块,其功能和主要设备分别为:
稳压供气模块:提供稳定高压气流,提供反应釜、平衡釜所需要的反应气源。主要设备为:12 MPa高压气瓶、12 MPa高压气罐、压力调节阀。
温度控制模块:提供模拟管道运行实验中所需的温度,所提供的温度范围是:−10℃~90℃。主要设备为:一套可连续高低温恒温水浴、电加热器、PID程序控温仪、探灯。
数据采集模块,本主要采集数据有:2支温度传感器测量的温度,2支压力传感器测量的压力,将数据传至计算机集中处理、记录与显示。上述温度、压力均自动逐时采集。
2.3. 实验步骤
由于实验中水合物在多孔介质中生成,孔隙中水合物的生成情况难以观测,因此为了便于观察水合物生成形态及其分布位置,将底部直径为5.5 cm,高6.5 cm的塑料容器放入反应釜中,加入多孔介质及气液两相,使水合物在该容器中生成,实验结束后,可将其取出,以更好地研究水合物生成特点。
1) 使用电子天平称重,配制浓度为300 ppm的表面活性剂SDBS溶液,保存待用;
2) 用去离子水将反应釜内壁和塑料容器内部和外部壁面反复冲洗并干燥,防止原有杂质对水合物成核及生长过程产生干扰;
3) 将表观体积为100 ml的多孔介质颗粒放入塑料容器中,之后放入反应釜并密封,气密性检验之后,开启真空泵将反应釜抽真空,避免残存气体的干扰,通过反应釜上方的进液口加入100 ml表面活性剂溶液;
4) 将反应釜放入温度为274.15 K的恒温水浴箱中,当反应釜温度降至实验温度后,打开进气阀,通过进气系统向反应釜内通入甲烷气体,压力达到6 MPa时自动停止进气(大于该温度下的相平衡压力);
5) 通过数据采集系统实时记录反应釜中的温度压力数值,当反应釜内压力在150 min保持稳定时(波动不超过0.1 MPa),即可认为水合物生成结束,快速拆卸反应釜,水合物在自保护效应下分解较慢,对水合物的原始分布影响较小,取出塑料容器后观察水合物的生成形态和分布位置。
3. 结果与分析
目前在世界范围内所发现的水合物矿藏中,水合物大多赋存于海底或永冻区土壤中的孔隙或岩石缝隙中,只有极少量的水合物是以块状水合物的形式存在 [15],因此,进行多孔介质体系中水合物生成规律的研究对于水合物资源的商业开采有着极为重要的意义。另一方面,水合物良好的储气性能决定了其在工业领域(如天然气的储运,二氧化碳的捕集与封存等。)有也有着非常重要的应用 [8]。而根据现有研究,多孔介质界面的存在可以通过提供成核界面的方法来促进水合物晶核的形成,进而大大促进水合物的生成速率 [16],所以,无论是对于基于水合物法的是工业应用还是水合物资源的商业开采,进行多孔介质体系中水合物的生成研究都显得尤为必要。
3.1. 多孔介质粒径对水合物生成的影响
3.1.1. 多孔介质和纯水中水合物生成情况
图2为氧化铝和二氧化硅颗粒种各粒径条件下水合物生成压降曲线,在实验所用的两种多孔介质中,水合物生成结束后,反应釜内剩余压力均随着颗粒粒径的增大而减小,根据实验数据,对于三种粒径的氧化铝颗粒,随着其粒径的增大,剩余压力分别为5.58,5.49和5.32 MPa,对于二氧化硅颗粒,随着粒径的增大其剩余压力分别为5.74,5.65和5.55 MPa。较小的剩余压力说明有更多地气体用于生成水合物,由于各组实验中SDBS溶液体积均相同,所以上述结果说明多孔介质粒径越大,在其内生成水合物的储气能力越强。对其储气量的计算也证明了上述结论,如表1所示,水合物生成结束后,随着颗粒粒径的增大,两种多孔介质中储存在水合物中的甲烷气体越多,因此,对于本实验采用的粒径尺度内,当水合物在较大粒径的颗粒中生成时,有利于其储气能力的提升。

Figure 2. Pressure drop curve of hydrate formation in porous media and pure water
图2. 多孔介质和纯水中水合物生成压降曲线

Table 1. Experimental data of hydrate formation in porous media and pure water
表1. 多孔介质和纯水中水合物生成实验数据
由于在水合物的生成过程中会消耗气体,因此反应釜中压力的下降速率可以在一定程度上反映出水合物的生成速度。从图中各组实验中的压降曲线可以发现,实验一开始,压力就开始快速下降,并且水合物在很短的时间内生成结束,并且各组实验中压力下降的速率并无明显差异,说明各组实验中水合物生成的速率也都大致相同,图3中的水合物生成速率也同样证明了这一点,在实验进行的前50分钟内,各组实验中水合物的生成速率就维持在一个很高的水平,并且与颗粒的粒径并无太大关系,实验开始150分钟之后,所有实验中水合物的生成速率几乎为零,水合物不再生成。因此,尽管实验中粒径对水合物生成后的剩余压力和水合物整体的储气量影响较大,但是对于水合物生成速率,并无明显的影响。
3.1.2. 多孔介质和SDBS溶液中水合物生成情况
图3为水合物在多孔介质颗粒和SDBS溶液中的生成压降曲线,图3(a)中多孔介质为二氧化硅颗粒,图3(b)中为氧化铝颗粒,较好地符合了上述水合物生成的三个过程。从图中可以看出,对于二氧化硅颗粒,在所采用的三种粒径的多孔介质中,随着粒径的增大,水合物生成结束后反应釜中的剩余压力越小,说明有更多的甲烷气体参与了水合物的生成,水合物生成后的储气量和储气密度也相应更高(如表2所示)。对于氧化铝颗粒也发现了相同的现象,即随着多孔介质粒径的增大,实验结束后反应釜内的剩余压力越小,根据实验数据,在二氧化硅颗粒中,随着三种颗粒粒径的增大,反应釜中剩余压力分别为4.74,4.45,3.95 MPa,氧化铝则分别为4.39,3.94,3.45 MPa。因此,在实验采用的多孔介质和表面活性剂溶液中,可以发现随着颗粒粒径的增大,水合物生成后的储气量和储气能力越强,水合物的生成效果越好。
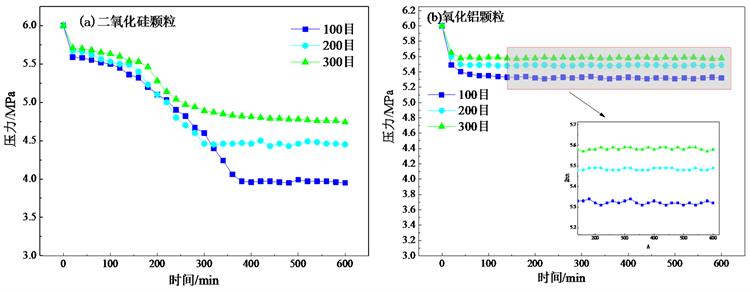
Figure 3. Pressure drop curve of hydrate formation in porous media and pure water
图3. 多孔介质和SDBS溶液中水合物生成压降曲线
根据实验数据,可以发现的另一个现象是,对于相同粒径的二氧化硅和氧化铝颗粒,在两种体系中水合物生成后的剩余压力也有所不同,在氧化铝颗粒中水合物生成后的剩余压力要显著小于二氧化硅颗粒中,这一现象说明,在采用氧化铝颗粒作为多孔介质的体系中,实验过程消耗了更多的气体,即该体系对于气体的储存能力较好。在之前的研究中,Pan等 [17] 采用了毫米级别的氧化铝和二氧化硅颗粒,也发现了上述现象,即氧化铝颗粒体系中水合物生成后气体的剩余压力较小。这可能是由于在氧化铝颗粒中,存在着数量丰富的微孔,该微孔对于气体也有一定的吸附能力,因此对于表面无微孔的二氧化硅颗粒,由氧化铝组成的水合物生成体系对于气体有着更好的吸附能力,进而导致了上述现象。

Table 2. Experimental data of hydrate formation in porous media and SDBS solution
表2. 多孔介质和SDBS溶液中水合物生成实验数据
3.2. 水合物在SDBS溶液和纯水中生成情况对比
根据对水合物生成过程的研究,可以认为比较典型的水合物生成过程主要分为3个阶段,分别为气体溶解期,诱导期和生长期 [18]。在不同的阶段中体系的温度压力将会产生不同的变化,在溶解期,主要为气体通过气液界面向液相中溶解,体系压力会有一定幅度的降低;第二阶段,溶解的气体分子与液相相互作用,逐渐生成小尺寸晶核,当晶核达到一定的数量之后,诱导期结束,水合物开始大量生成 [19]。由于该阶段水合物不断生成和分解,并最终仅有水合物晶核生成,所以温度和压力基本保持不变 [20];最后一个阶段,诱导期形成的稳定晶核不断长大并聚结,宏观反映为体系内水合物大量生成,释放出热量,温度会产生一定程度的波动,并由于此时气体不断被消耗,体系内压力大幅下降,直到水合物生成结束。
根据2.1部分中图2和图3所示的水合物压降曲线,可以看出,由多孔介质和SDBS溶液组成的体系中,水合物生成过程存在着较为明显的诱导期(图3),即在水合物的压降曲线中,压力经过短时间的下降后,在一定时间内保持稳定,之后又快速下降的过程,符合上述水合物生成时所经历的三个阶段,一般认为,水合物生成过程中诱导期的存在及其持续时间的长短存在较大的随机性,并且与生成体系的温度,压力,杂质以及生成介质有一定的关系,诱导期的存在会在一定程度上延长水合物生成所需的时间,进而降低水合物生成的整体速率,因而并不利于水合物的快速生成,因此如何通过控制实验条件,降低水合物诱导期的出现对于水合物的快速生成有着重要的作用,应作为重点进行研究。

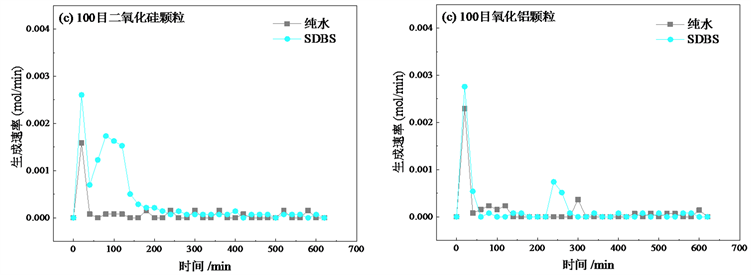
Figure 4. Comparison of hydrate formation rate between pure water and SDBS solution
图4. 纯水和SDBS溶液中水合物生成速率对比
另一方面,通过对比同种多孔介质中水合物在纯水和SDBS溶液中生成后的剩余压力,可以看出在SDBS溶液中,实验结束后反应釜中最终的剩余压力要显著小于纯水中,说明在SDBS溶液中水合物生成过程中有更多的气体参与了水合物的生成,因此水合物生成后的储气密度和储气量相应越大,水合物生成效果更好。图4为水合物在相同粒径的同种多孔介质中,水合物在纯水和SDBS溶液中的生成速率对比。可以发现,对于同种粒径相同的多孔介质颗粒中,水合物在SDBS溶液中的生成速率大于纯水中,同时,水合物生成的持续时间较长,水合物生成速率经过一段时间的波动后,随着水合物生成的结束,其生成速率曲线逐渐趋向于0 mol/min。另外,值得注意的是,虽然纯水体系中水合物生成的持续时间较短,水合物生成整体时间相对于SDBS溶液中较短,但这是由于纯水中水合物生成量较少导致的,因而所需时间较短,并不能说明其中水合物生成较快,其生成速率相对于SDBS溶液中仍较小,图4中水合物生成速率曲线也说明了这一现象。
3.3. 表面活性剂溶液促进水合物生成原因分析
水合物生成时,气体分子会通过气液界面进入液相,在低温和高压条件下与周围邻近的水分子形成水合物晶核,并不断聚集长大成为块状水合物。然而,在纯水条件下,由于气液界面表面张力的存在以及甲烷分子自身的疏水性,在水中的溶解度很小,所以在静态体系中,纯水条件下水合物往往只在气水交界面处生成一层薄膜,并会阻碍气体分子向液相中的传质过程,水合物难以进一步生成,所以,许多研究均发现,水合物在纯水中生成量很少,反应体系难以观察到明显的压降过程,并且生成速率非常缓慢 [21] [22]。

Figure 5. SDBS ionization process of anionic surfactant in solution
图5. 溶液中阴离子表面活性剂SDBS电离过程
而表面活性剂具有双亲性结构,其两侧的亲油性基团和亲水性基团,使其能够显著地降低气液表面张力。在液相中加入表面活性剂后,其分子以亲水基朝向水相,亲油基朝向气相排列 [23] [24]。对于本实验采用的阴离子表面活性剂SDBS,图5展示了其在溶液中的电离过程,当溶于水后,会电离出带正电荷的钠离子和带负电荷的活性基团,此活性基团由于具有双亲性结构,能够显著降低气液界面的表面张力,从而使甲烷分子在水合物生成体系中更易于向液相中溶解。当液相中含有更多的甲烷分子后,在促进水合物成核的同时,也能使得更多的甲烷气体进入水分子笼中,进而增大了生成水合物的储气量和储气密度。因而在前述的实验现象中,对于多孔介质颗粒和纯水组成的体系,水合物生成后反应釜中的剩余压力较大,水合物生成速率、生成量及其储气能力都相对较小;而对于由SDBS溶液所组成的体系中,水合物生成效果则得到了明显的改善,有更多的气体参与了水合物生成,生成速率也有所提高并且生成水合物的量较多。




Figure 6. Hydrate formation in porous media under the conditions of pure water and SDBS solution
图6. 多孔介质中水合物在纯水和SDBS溶液条件下生成现象
图6为粒径100目的氧化铝和二氧化硅颗粒中,水合物分别在纯水和SDBS溶液中的生成现象。如图所示,在多孔介质和纯水体系中,水合物生成量较少,在多孔介质的孔隙中仍有大量的液态水未转变为水合物,水合物仅在气液界面处有生成,生成后阻碍了甲烷气体向反应釜底部液相中的溶解,进而阻碍了水合物的进一步生成。而在多孔介质和SDBS溶液体系中,由于气液界面的表面张力大大降低,甲烷分子易溶于液相中,在气液界面生成水合物阻碍气相向液相中溶解之前,溶液中已溶解了足够量的甲烷分子,因而反应釜底部多孔介质孔隙中,也有大量的水合物生成。因此,上述实验现象说明,表面活性剂的加入,能够较为有效地改善水合物的生成效果,能够在加快水合物生成的同时,增加其储气量和储气密度,促进水合物的生成。
4. 结论
本文通过采用粒径分别为100、200和300目的氧化铝和二氧化硅颗粒作为多孔介质,研究了该条件下水合物分别在纯水和浓度为300 ppm的SDBS溶液中的生成情况,得到了如下结论:
1) 在氧化铝和二氧化硅颗粒中,对于本实验采用的粒径尺度内,水合物在较大粒径的颗粒中生成时,有利于其储气能力的提升,并且生成速率较快。
2) 氧化铝颗粒中,存在着数量丰富的微孔,该微孔对于气体也有一定的吸附能力,因此对于表面无微孔的二氧化硅颗粒,由氧化铝组成的水合物生成体系对于气体有着更好的吸附能力,所以将具有吸附能力的材料作为水合物生成介质可以有效地提高该生成体系的气体储存能力。
3) 表面活性剂SDBS的加入可以降低气液界面的表面张力,使气体分子更易向液相中溶解,促进水合物晶核的生成,进而可以较为显著地改善水合物的生成效果,提高水合物生成速率的同时增加其储气能力。
目前,国内外众多学者的研究成果指出,大粒径条件下水合物生成速率快,原因是当粒径较小时,其孔径越小,产生较强的毛细管力会阻碍气体的扩散并降低液相的活度,而大孔径由于对水分子和气体分子的束缚较小,并且介质表面增大了气–水接触面积,因此能加快水合物生成速率 [25] [26] [27]。在表面活性剂方面,研究指出表面活性剂通过降低液体的表面张力,减小气液传质阻力,能有效促进水合物生成时气体分子进入液相,以改善水合物的生成效果 [13] [28] [29],与文中进行的实验结果及分析相一致。本文进行了静态条件下多孔介质和表面活性剂SDBS的复配体系中水合物的生成研究,由于是在材质为不锈钢的反应釜中生成,并不能在水合物生成过程中进行观测,目前通过拆卸反应釜取出观察的方法存在水合物一定程度上溶解的问题。因此,在接下来的研究中,应采用便于观察的透明反应釜及显微摄像机,以更好地明确水合物在多孔介质孔隙中的生成过程及分布情况。