1. 引言
海马是一种重要的海洋经济鱼类,随着生态环境的污染恶化,它们极易受到过度捕捞和栖息地退化的影响,野生海马的数量不断减少。多数海马物种已被列入《濒危物种红色名录》、《濒危物种国际贸易公约》和《濒危物种名录》 [1] [2]。因为中药需求、宗教仪式以及其他用途,海马市场需求却逐年走高,开展海马的集约化养殖是解决这一供需矛盾的唯一出路。 我国的海马资源主要分布于广东、广西和海南沿海地区,民谚“北方人参,南方海马”,海马是一种重要的海洋生物药源,具有安神镇静、健体强身、活络舒筋、补肾壮阳、消肿止痛、止咳平喘等功效。海马的养殖品种很多,过去传统主要有三斑海马、大海马、刺海马、鲍氏海马、克氏海马、日本海马等 [3] [4] [5] [6]。近年来,更受瞩目的是从美国引进的线纹海马 [7] [8] [9] [10]。
线纹海马(Hippocampus erectus)属硬骨鱼纲(Osteichthyes)、辐鳍亚纲(Actinopterygii)、鲈形总目(Percomorpha)、刺鱼目(Gasterosteiformes)、海龙亚目(Syngnathoidei)、海龙科(Syngnathidae)、海马属(Hippocampus),又名灰海马。最大体长可达27 cm,寿命3~4年,原产地在美洲地区,具有较强的抗病能力,生长速度与其他种类的海马相比也有优势,它可以在5个月之内由刚出生的小海马,长至10 cm左右的成品海马。因此,线纹海马相对国内传统养殖的其它品种海马更加适宜人工养殖,正成为主流的养殖海马品种 [11] [12] [13]。
海马作为一种特殊鱼类,其繁殖方式是雌雄鱼配对,在人工生态调控的适宜环境下自然产卵,由雄性进行孵化。一个海马繁殖场的生产力主要由其能够进行繁殖的海马亲鱼的对数来决定。因此开展关于海马早期雌雄判别的研究对海马的繁育和生产具有重要价值。为此,本研究以线纹海马为研究对象,通过测量不同发育时期血液中激素水平以及卵黄蛋白原含量来尝试在海马早期发育时期判别海马的性别。
2. 材料与方法
2.1. 材料
海马购自威海银泽生物科技有限公司养殖基地,共选取海马100尾,规格分别5~6 cm、7~8 cm、9~10 cm、11~12 cm、13~14 cm的雌雄海马。暂养于山东省青岛农业大学海洋科学与工程学院室内海水循环水养殖系统中,系统包含蛋白分离器、紫外线杀菌灯、控温系统。控制水温26℃~28℃,盐度28~30。系统内置珊瑚石、竹枝供海马攀附。每天投喂冷冻糠虾两次,下午投喂二十分钟后吸底换水一次。每天定时清洗蛋白分离器。
实验前,将海马进行分组,每10尾生长状况相似的为一组,以1 cm为梯度,共分为10组,记录其平均体长和平均体重,如表1所示。

Table 1. Body length and body weight of the Hippocampus erectus
表1. 线纹海马体长体重记录表
2.2. 方法
待检测海马,停食24 h,测定其体重和体长。用0.035% MS-222海水麻醉2分钟后在冰盘上解剖,用解剖剪刀沿泄殖孔向上挑剪,剪刀头向外顶以防划破内脏,剪至下颌直至看到心脏。用解剖刀割去外皮,用镊子取内脏团(主要包括肾、肝胰脏和性腺),放在盛有冰冷生理盐水的烧杯中漂洗,然后用滤纸拭干,用镊子将内脏放在称重纸上,去皮称重。量取内脏团重量九倍的生理盐水,取三分之二倒入研体中,将称重后的组织放入研体中研磨。充分将器官捣碎,研磨成匀浆后将其倒入冷藏管,再用剩余的三分之一生理盐水冲洗残留在研体壁上的碎组织块,一起倒入冷藏管振荡摇匀,使组织充分匀浆化。将配置好的百分之十匀浆用离心机2000 r/min离心15分钟,抽取上清液弃掉沉淀物,上清液即为酶液。酶液分为两部分,一部分马上测定,剩余部分放置于−20℃冰箱中冷藏,保存以备复查。
2.3. 卵黄蛋白原测定
于离心管中加浓度为100 ml/L的TCA 1 ml及0.5 ml血清样品,在零摄氏度过夜。在高速离心机1600 r/min离心10 min,舍弃上清液。在通风橱中按顺序清洗沉淀物,每次清洗后离心,弃掉上清液(乙醇→氯仿:乙醚:乙醇1:2:2→丙酮→乙醚)。加入0.5 ml浓度为5 mol/L的NaOH,将离心管密封后于110℃水解两个小时。将水解后的样品移入比色管中,用移液枪量取0.5 ml浓度为5 mol/L的HCL,加到比色管中中和,再加入2 ml显色液(0.4毫升3 mol/L硫酸、0.4毫升25 g/L钼酸铵、0.4毫升100 g/L抗坏血酸以及0.8 ml蒸馏水)并用蒸馏水定容。在三十七摄氏度中孵育两个小时,稀释十倍后将比色管在分光光度计780 um波长处比色。
2.4. 雌二醇激素测定
将离心好的匀浆留上清液弃掉下面沉淀。E2酶联免疫检测试剂盒(购自南京建成生物工程研究所)从4摄氏度冰箱拿出,放到实验台上在室温下平衡半个小时。将板取出洗涤后甩干,空白孔不加样品,只加显色剂A、B和终止液以调零。用移液枪抽取一百五十微升的标准品稀释液到标准品冻干粉中,用移液枪抽打三十秒作为标准品原液。
从灭菌锅中取出五支干净的离心管,向每管中加入一百五十微升的标准品稀释液,向第一个管中加入一百五十微升原液,摇匀后抽出一百五十微升加入下一管,依次加到第五个管。贴上标签纸,标记浓度400 nmol/L、200 nmol/L、100 nmol/L、50 nmol/L、25 nmol/L。向标准品孔中加入50 ul稀释好的标准品,零孔中加入50 ul标准品/样品稀释液然后加入50 ul生物素抗原工作液。
在样品孔中加入50 ul样品然后再加入生物素抗原工作液50 ul。轻轻摇晃,贴紧封板膜,盖上盖子,在37摄氏度的培养箱中孵育30分钟。将25倍浓缩洗涤液倒进五百毫升大烧杯中定容到五百毫升作为洗涤液使用,小心揭去封板模,甩出液体,再在每孔滴满洗涤液,放置三十秒后甩去,重复五次后轻轻拍干。加入亲和素50 ul到零孔、标准品孔和样品孔中,轻轻摇晃后盖上封板模,再次放在37摄氏度培养箱中孵育三十分钟。
2.5. 睾酮激素测定
睾酮酶联免疫检测试剂盒购自南京建成生物工程研究所,在标准管贴上标签纸,标记浓度120 nmol/L、60 nmol/L、30 nmol/L、15 nmol/L、7.5 nmol/L。其余步骤与雌二醇激素检测方法相同。
3. 结果与分析
3.1. 卵黄蛋白原
如表2、图1、图2所示,随着体长和体重的增加,海马血液中卵黄蛋白原浓度呈下降趋势,说明成熟海马对卵黄蛋白原的吸收利用速度较快,体内血液中卵黄蛋白原含量会略低。雌性海马幼体体内卵黄蛋白原含量相比雄性体内的卵黄蛋白原含量高。

Table 2. Relationship between vitellogenin concentration and sex, body length, body weight
表2. 卵黄蛋白原浓度与性别、体长和体重的关系
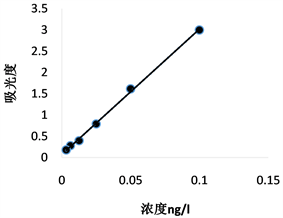
Figure 1. Standard curve of vitellogenin
图1. 卵黄蛋白原的标准曲线

Figure 2. Relationship between vitellogenin concentration and body length
图2. 卵黄蛋白原浓度与体长关系
3.2. 雌二醇激素
根据实验测得数据可知雌二醇E2的浓度与吸光度值的关系是一个二元曲线关系,如图3、图4所示。
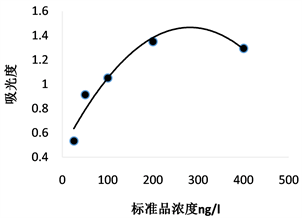
Figure 3. Standard curve of estradiol solution
图3. 雌二醇标准溶液曲线
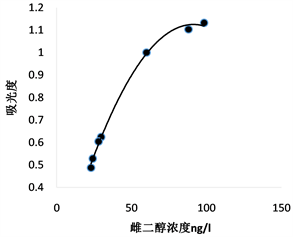
Figure 4. Relationship between estradiol concentration and absorbance value
图4. 雌二醇浓度与吸光度值的关系
根据图5、图6体长、体重与海马雌二醇E2的关系可以看出,在体长9 cm体重5 g前,雌二醇的浓度出现一个增长阶段,在体长9 cm体重5 g后出现一个降低趋势。在体长9 cm体重5 g左右时是数据测量的最佳时间。
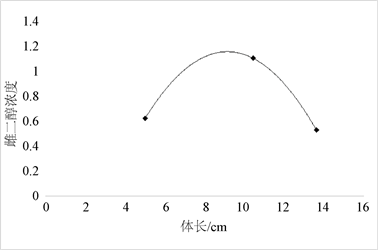
Figure 5. Relationship between estradiol concentration and body length
图5. 雌二醇E2含量与锦鲤体长的关系
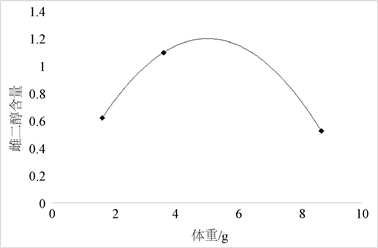
Figure 6. Relationship between estradiol concentration and body weight
图6. 雌二醇E2含量与锦鲤体重的关系
3.3. 睾酮激素
如图7、图8所示,海马睾酮激素的浓度与吸光度值的关系也是一个二元曲线关系。
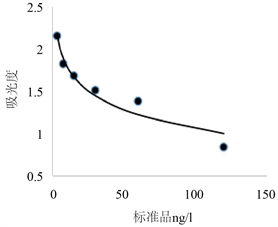
Figure 7. Standard curve of testosterone solution
图7. 睾酮标准溶液
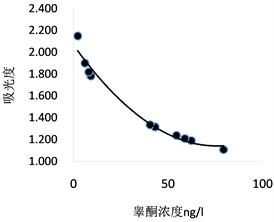
Figure 8. Relationship between testosterone concentration and absorbance value
图8. 睾酮浓度与吸光度
根据图9、图10中的对比,发现同一年龄段雌性海马体内睾酮明显高于雄性海马体内睾酮含量。而且雌性海马体内雌二醇也高于雄性。主要是因为雌二醇刺激海马的发育,而雌性海马生长速度快于雄性,所以雌二醇浓度更高,又因为睾酮是雌二醇的前体物质,所以睾酮的含量,雌性也高于雄性。
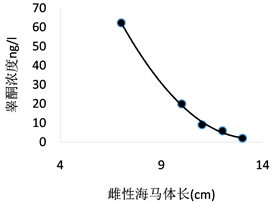
Figure 9. Relationship between testosterone concentration and body length
图9. 睾酮浓度与雌性海马体长的关系
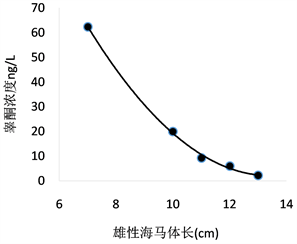
Figure 10. Relationship between testosterone concentration and body weight
图10. 睾酮浓度与雄性海马体长的关系
4. 讨论
4.1. 线纹海马卵黄蛋白原及激素的变化规律
海马卵黄蛋白原的主要来源是依靠外源性的卵黄合成。海马的卵黄蛋白原主要是在肝脏合成,合成后由血液运送至卵巢,由卵巢内的细胞吸收并利用。成熟的雌性海马,对卵黄蛋白原的吸收利用速度较快,体内血液中卵黄蛋白原含量会略低。雌性海马仔鱼卵巢细胞的功能不全,对体内产生的卵黄蛋白原的利用率低,导致体内的卵黄蛋白原含量略高。雄性海马体内血液中也有卵黄蛋白原的存在,卵黄蛋白原是在肝脏细胞中产生的,肝脏细胞在雌二醇存在的情况下,会受到刺激产生卵黄蛋白原,并释放进入血液,但是雄性个体没有可以高度吸收利用卵黄蛋白原的组织器官,血液中就会一直留存一定含量的卵黄蛋白原。
在海马的精巢中,同样产生多种性激素,其中最为主要的性激素为类固醇雄激素(雄酮、雄烯二酮、睾酮以及11-氧睾酮),其中最为活跃的雄性激素为11-氧睾酮,在其他文献中也曾经提到,11-氧睾酮在其它的硬骨鱼类中也是最为活跃的雄激素。当然,在其它品种鱼类中,雄鱼体内也会产生孕激素,海马体内孕激素的含量需要进一步研究证实。
在雄性的精巢中则没有雌性激素的出现,雌激素主要是由雌性体内的卵巢细胞和卵巢内的其他组织细胞产生。
合成雌激素的前体物是雄性激素,因此在雌性个体中还有相当部分的雄性激素。在雌性个体中的雄激素以睾酮的含量为最多,雌性海马体内的睾酮的代谢物与雌性海马的第二性征发育和性行为有关。
性类固醇激素对下丘脑、性腺、垂体的功能及稳定有不可言喻的重要性。在性腺发育的不同阶段,某种性类固醇激素会占有优势。
4.2. 线纹海马的生态习性
海马主要以小型甲壳类、端足类和挠足类以及各种小虾为食,野生海马只吃活食,部分经过人工驯化的种类能够投喂人工冷冻饵料 [7],主要依靠鳃盖和吻的伸张活动吞吸食物,进食时,吻管先接近食物,然后颊部鼓起,口张开,最后吸食食物。海马的摄食量与水质、水温有密切联系。在适温范围内,水温高,则摄食量大,消化快;水温低,则摄食量小,消化慢。水质不良时,食量变小,甚至不吃。在正常条件下,海马每天的摄食量约占体重的百分之十。海马一次性摄食量很大,同时耐饥性也很强,从幼体到成体耐饥时间可长达4~132天 [8]。海马的体色可以随着外界环境的变化而变化,这是因为海马游速较慢,抗敌害能力差,具有保护色能大大提高海马的生存能力。
繁殖期的雌、雄性最明显的特征是体色由黑褐色转变为淡黄色,雌性体色较雄性深而艳丽,背鳍比雄性的要大。欲生产时,雄性的育儿囊明显突起、膨大,生殖孔转变为咖啡色。
线纹海马白天活动性强,晚上活动较少。这是因为海马主要靠视觉捕食,而且这种生物节律也能够有效避免肉食敌害物种的捕食;在上午的时间段里活动更加频繁,幅度也更大,这些可能均与海马的年龄、发育程度有关。虽然海马是白昼型动物,但白天也主要是休息,主要的活动是有关摄食的行为表现(大部分的行为与此有关)。雄性线纹海马通过与雌性日常接触、问候的方式,加强一夫一妻的关系。择偶完成后,才能够更有效地进行交配,互相配合完成整个繁殖过程,繁殖出易于适应环境的后代。雄性线纹海马起主导作用,这是因为前期雌性线纹海马需要消耗远超过雄性线纹海马的能量以提供给配子,生殖投资大于雄性;但不同于其他物种的是,交配结束后,受精卵在雄性体内孵化,此时雄性在繁殖上的投入远远得多于雌性,导致雄性对雌海马也有较高的要求。因此,一旦交配成功,配偶相对固定,综合反应为独特的“一夫一妻”行为。
4.3. 线纹海马早期雌雄判别研究的意义
本文对线纹海马的日节律和繁殖行为作了观察和分析,重点研究了从五厘米到十三厘米的不同规格不同性别的海马激素水平差异。通过分光光度计测出卵黄原蛋白含量,用酶标仪测出睾酮和雌二醇吸光值,根据逻辑斯蒂四参数方程算出浓度,得出雌二醇、睾酮、卵黄原在发育过程中的变化。综上所述,同一年龄段的线纹海马,体内雌二醇和睾酮含量高的为雌性,低的为雄性,以此鉴别幼体线纹海马雌雄。本文进一步总结了其体内激素变化规律,研究了不同阶段海马血浆中性激素(包括雌二醇激素和睾酮、卵黄原蛋白)的变化,从而在其幼年时期尽早区分雌雄。以前对线纹海马的繁殖行为研究较少,不利于线纹海马的人工养殖的扩大生产。
很多野生海马受到来自环境雌激素的影响导致早熟或者雌化,此类雌激素物质可通过食物链的生物放大作用对人类健康造成不良影响,这就需要我们关注其体内激素浓度变化是否异常,及时采取措施。对于养殖型海马通过了解其繁殖期激素水平变化关注其激素浓度指数上升期,给以更全面的保护和照顾;同时可通过性激素水平了解性器官是否衰退,为以后同类的研究中的苗种繁育、增殖养殖和濒危物种保护等奠定基础。
4.4. 线纹海马后续研究及利用价值
本次实验通过测定线纹海马体内卵黄蛋白原浓度、雌二醇浓度和睾酮浓度对线纹海马的性别进行了鉴定。在实验中发现卵黄蛋白原浓度及两种激素浓度随着海马的体长的变化具有一定的线性关系,在后续的试验中可以对雌雄海马体内卵黄蛋白原浓度和两种激素浓度进一步区分,完善其线性关系。最终可以利用该线性关系在线纹海马幼体或胚胎时对其进行雌雄区别养殖。并利用浓度曲线对线纹海马的生长过程进行监测。
海马的经济价值主要有:由于很多海马品种形状独特,种类繁多,色泽亮丽,世界各地的水族馆均有存在,作为一种野生保护动物,海马作为观赏鱼深受人们喜爱。海马具有被制作成装饰品的功能:海马经加工晒干后仍能保持其原有的斑纹,色彩鲜艳美丽,加工工艺简单,经过晒干,可以制成耳环、别针、锁匙扣等装饰品,干海马在有些地方还被作为辟邪物,自古以来,海马就是备受欢迎的收藏装饰品。海马是一种珍贵的海洋中药材:在我国素有“北方人参,南方海马”的美誉。早在《神农本草》中就有记载:海马性温、味甘,具有强身健体、补肾壮阳、消炎镇痛、止咳平喘的药效,尤其对于具有神经系统疾病的患者,更是有显著的疗效。现代医学上已证明海马提取物具有抗衰老、抗癌活性、性激素样等作用,海马的乙醇提取物(即“海马酒”)能使雄鼠前列腺、精囊、提肛肌的重量明显增加,表现为雄激素样作用,因此,海马在中医药上有特殊的需求地位。作为中药用海马,大多产于福建省和广东省,国内外市场需求量很大,据报道,仅中国内地、台湾和香港以及新加坡每年海马销售量就达一千六百万尾,每年的销售额更是达到了两亿美元 [12]。
基金项目
青岛水族技术协同创新中心合作项目(6602418043);青岛市市南区应用基础研究计划项目(2018-4-011-ZH);国家自然科学基金(32073029)
NOTES
*通讯作者。