1. 引言
郁金是常用的大宗药材,被广泛用于临床。据记载,郁金具有清心解郁、行气、活血化瘀、利胆退黄等功效,用于治疗经闭、胸腹胀痛、热病神昏、癫痫发狂、黄疸尿赤等症 [1],其中温州郁金主要分布于浙江温州,为著名的“浙八味”之一 [2],为药材郁金的基原之一。然而,目前因环境的破坏等因素,市面上的郁金品种参差不齐,并且不同的郁金种类在性状、显微、药理药效等方面存在很大差异 [3]。同时,由于2015年版《中国药典》(一部) [4] 中并未收集郁金除总灰分和水分以外的检查,并且在现阶段,我国中药产品中的重金属元素并没有限量控制标准,还需参照其他国家对进口中药的重金属限量标准 [5] [6],因此发掘对其单因素的测定的方法是必要的。
目前,测量中药中重金属的方法有比色法(最主要是砷斑法) [7]、紫外–可见分光光度法、原子荧光光谱法 [8]、高效液相色谱法 [9]、电感耦合等离子原子发射光谱(ICP-AES) [10] [11]、电感耦合等离子体质谱(ICP-MS) [12] 等方法。以电感耦合等离子原子发射光谱法为例,其容易受到基质干扰,虽然目前可通过溶液稀释等方法降低测定时的影响,但无法根除,且测量成本昂贵,对技术操作人员的要求高,检测灵敏度与稳定性都相对较差 [13]。而相对地,原子荧光光谱法作为一种根据待测元素的原子蒸汽在辐射能激发下所产生的原子荧光发射强度进行定量的光学分析方法,能够避开光谱干扰的问题,其操作简单快速、检测成本也较低廉 [14],原子荧光的谱线比较简便,便于分辨,并且原子荧光向各方向辐射,便于制作多通道仪器,适合多元素同时测定,符合中药的整体性概念,因中药发挥多通道、多靶点药理,因此多以多个指标对中药的整体质量进行控制 [15]。原子荧光的校正曲线线性范围宽,且干扰效应相对较少,是一种优良的测量重金属方法。王正等 [16] 通过原子荧光光谱法测定出了贵州不同产地的各种马兰草中砷和汞的含量,测出黔西南安龙药材中的砷含量超标。
为了便于测定样品中的重金属,需要在前期对样品进行预处理,以破坏有机物 [17],便于接下来的试验。现阶段对于中药样品的预处理方法 [18] 主要有干法灰化、湿法消化、微波消化等。干法消解需要马弗炉,前处理的时间较长,其次,长时间的干灼烧过程容易导致检测元素的丢失,另外,其容易因杂质的引入而造成污染 [19];湿法消解中,消解液需要高氯酸,若不使用高氯酸,则需要大量补充消解液,前者容易对造成事故,后者容易造成试剂污染 [20]。目前,微波消化因加热最均匀、消解速度最快、易挥发元素在灼烧过程中的损失最少和对环境影响小而被认可并广泛应用:2013年倪张林 [21] 等利用微波消解和电感耦合等离子体质谱法作为预处理以即测定的搭配方法,测定出了茶籽油中欧给的Pb、Cd、Cr等五种重金属元素的含量,2014年牟锟 [22] 利用微波消解法作为前处理方法,对锌精矿中的锌和镉进行了测定。此外,安建博等 [23] 对干法灰化发和微波消解法进行对比试验,结果表明微波消解法耗时短,适用于形态相对简单的砷的化合物的检测。
原子荧光测定重金属的原理:在一定的酸介质中,重金属与硼氢化钾反应生成氢化物,在相应重金属的空心阴极灯照射下,重金属原子由基态被激发至高能态,而在瞬间又回到基态时,发射出特征波长的荧光,在利用标准曲线法进行测量 [24]。因此,选取影响反应过程的因素负高压、灯电流、载气流量和屏蔽气流量四因素进行单因素筛选,并且对这些试验条件进行优化。
《中国药典》中提出砷的检测方法为原子吸收分光光度法,使用氢化物法进行测定。本试验所使用的方法是在该基础上加以研究和改进的方法,即检测方法采用微波消解–原子荧光光谱法,试剂采用硫脲–抗坏血酸溶液。因此本试验的方法真实可靠。
2. 试验部分
2.1. 仪器与试剂
AFS-8220原子荧光光度计(北京吉天仪器有限公司);SC-2.4-4型号电热板(中国江苏东台市跃进电器厂);WX-4000型微波快速消解系统(上海屹尧仪器科技发展有限公司);ME204E,电子天平(瑞士苏黎世梅特勒–托利多公司)。
100 µg/mL砷标准储备液(国家标准物质研究中心);盐酸、硝酸(优级纯);硫脲、抗坏血酸、氢氧化钾、硼氢化钾(分析纯);试验用水为超纯水。
2.2. 试剂配制
2.2.1. 试验试剂的配制
硫脲,抗坏血酸各取25 g溶于100 ml水中,配制成250 mg/mL的硫脲–抗坏血酸溶液;混合酸(浓硝酸:浓盐酸 = 5:1);配制6 mol/L盐酸(浓盐酸与水的体积比为1:1);浓盐酸与水的体积比例1:20配制5% HCl溶液;配制氢化钾溶液:将7.5 g硼氢化钾溶于0.5% KOH溶液中,用500 mL容量瓶定容。
2.2.2. 标准曲线的配制
As标准溶液(100 μg/mL)。
As标准工作液I (10 μg/mL):移取100 μg/mL As标准工作液1.0 mL,用水定容至10 mL。
As标准工作液II (200 ng/mL):移取10 μg/mL As标准工作液1.0 mL,用水定容至50 mL。
取As标准工作液II 0.00 mL、1.00 mL、2.00 mL、5.00 mL、10.00 mL、15.00 mL分别加入5 mL的硫脲–抗坏血酸溶液并定容于50 mL的容量瓶,溶解后标准溶液浓度为0.00 ng/mL、4.00 ng/mL、8.00 ng/mL、20.00 ng/mL、40.00 ng/mL、60.00 ng/mL。
2.3. 试剂配制样品采集与前处理
2.3.1. 郁金的获取
购于老百姓大药房,经浙工大药学院唐岚副教授鉴定为温郁金和广西郁金。
2.3.2. 样品前处理
1) 微波消解前处理
取1.000 g样品于消化罐中,加入14.0 mL的混合酸,超声20 min后拧紧盖子,放于微波样品制备系统内进行消解(微波功率300 W,消解时间5 min)。消解完毕,冷却至室温,加入硫脲–抗坏血酸溶液5 mL,用5%盐酸少量多次定容于25 mL容量瓶中,待测,做空白。
2) 加热消解前处理
取1.000 g样品于锥形瓶中,加入14.0 mL的混合酸,超声20 min后放置电热板上加热,至溶液澄清。待其冷却至室温,加入硫脲–抗坏血酸溶液5 mL,用5%盐酸少量多次定容于25 mL容量瓶中,待测,做空白。
2.4. 原子荧光仪器条件
光电倍增管负高压300 V;As灯电流70 mA;原子化器高度8 mm;载气流量300 mL/min;屏蔽气流量600 mL/min;载气氩气(99.99%);采用顺序注射程序控制;测量方法:校准曲线法;读数方式:峰面积;读数时间10 s;延迟时间1 s。
3. 结果与讨论
3.1. 标准曲线绘制
取As标准液1 mL,2 mL,5 mL,10 mL,15 mL,25 mL分别加入5 mL的硫脲–抗坏血酸溶液并定容于50 mL的容量瓶,在1.4条件下测定荧光强度。试验表明,砷在4~100 µg/L的浓度下呈良好的线性关系,线性回归方程为:Iƒ = 58.662C + 56.083,r = 0.9998。
3.2. 原子荧光测试的单因素筛选
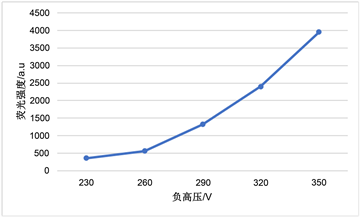
分别考察负高压、载气流量、屏蔽气流量以及灯电流对荧光强度的影响,结果见图1。
 (A)
(A) 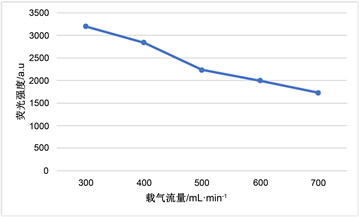 (B)
(B) 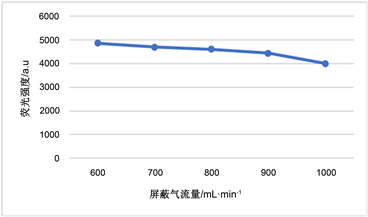 (C)
(C) 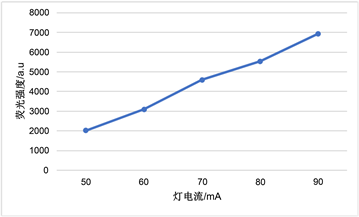 (D)
(D)
Figure 1. Influence of different factors on fluorescence intensity. (A) Negative high pressure; (B) Carrier gas flow; (C) Shielded gas flow; (D) The lamp current
图1. 不同因素对荧光强度的影响。(A) 负高压;(B) 载气流量;(C) 屏蔽气流量;(D) 灯电流
试验表明,荧光信号随负高压的增大而显著升高,但是噪声也逐渐增强,在300 V时,信噪比最大,320 V时信噪比最低;随载气流量逐渐增大,荧光强度反而逐渐减小;荧光强度随屏蔽气流量的增大也逐渐减小,但是减小幅度不大;随着灯电流的逐渐增大,荧光强度逐渐增强,但是灯电流过大,噪声显著增强,荧光强度不稳而且极易降低灯的使用寿命。
3.3. 通过正交分析对原子荧光测试的单因素进行优化
综合以上几点,我们选择以下条件进行正交分析(表1)。

Table 1. Orthogonal test factor level table
表1. 正交试验因素水平表
由表2正交试验可知,负高压影响最大,其次为灯电流强度,最佳选择为A3B3C1D1,即最优条件为:负高压为300 V,灯电流为70 mA,载气流量为300 mL/min,屏蔽气流量为600 mL/min。在优化的条件下平行测定3组试验,荧光强度分别为5926.83 a.u.,5916.42 a.u.,5907.44 a.u.。

Table 2. Orthogonal experimental design and results
表2. 正交试验设计与结果
3.4. 消解方式的选取
3.4.1. 微波消解
取1.000 g温郁金于消化罐中,加入14 mL混合酸,加盖,超声20 min,置微波样品制备系统内进行消解(微波功率300 W,消解时间5 min)。消解完毕后,冷却至室温,加入硫脲–抗坏血酸溶液5 mL,用5%盐酸少量多次定容于25 mL容量瓶中,待测,做空白,平行测三组。
3.4.2. 加热消解
称取1.000 g温郁金于100 mL烧杯中,加入14 mL混合酸,加盖,超声20 min,置电热板上加热消解。
3.4.3. 两种消解法的比较
通过微波消解和加热消解后,比较两种消解方法中砷的含量,结果见表3。

Table 3. Comparison of arsenic content in samples extracted by different digestion methods
表3. 不同消解方法提取样品中砷含量的比较
3.5. 不同郁金中砷含量的测定与比较
分别取适量温郁金与广西郁金,用微波消解法进行消解,然后进行原子荧光测定,其结果见表4。

Table 4. Detection of arsenic content in tulips from different places
表4. 不同产地郁金香砷含量的检测
3.6. 检出限
由3.1线性方程可知,线性关系良好,相关系数r ≥ 0.9992。根据信噪比(S/N) = 3,(S/N) = 10,以噪音的3倍测定检出限,测得检出限(LOD)为1.48 µg/L,定量限(LOQ)为4.93 µg/L。
3.7. 精密度试验
取20 µg/L的砷标液按照试验条件连续进样5次,记录峰面积,计算峰面积层顶结果的相对标准偏差,测得平均RSD为2.36%,结果表明该方法具有良好的精密度和准确度。
3.8. 加标回收率试验
分别精密称取适量温郁金与广西郁金,取浓度为15 mg/L、30 mg/L、60 mg/LSD溶液,25 mg/L、50 mg/L、100 mg/L的SM2溶液和35 mg/L、70 mg/L、140 mg/L SMD溶液按1.4前处理方法,并在1.4色谱条件下进行回收率的测定,记录峰面积并且计算回收率分别加砷对照品进行测定,其结果见表5。
4. 结论
本文利用微波消解–原子荧光光谱法快速有效地测定郁金中的砷含量,可作为检测砷含量的一种可靠方法。试验结果表明,该方法下测定的最优条件为:负高压为300 V,灯电流为70 mA,载气流量为300 mL/min,屏蔽气流量为600 mL/min。此外,不同品种的郁金砷的含量不同,温郁金香砷含量低于广西郁金,这可能与不同土壤里砷含量的高低、使用含砷化肥或农药等有关 [25]。
经过试验发现,微波消解相对于传统加热消解有以下优点:加热快、升温高,消解能力强,大大缩短了溶样的时间;消耗政溶剂少,空白值低;避免了挥发损失和样品的玷污,提高了分析的准确度、精密度和回收率;节省电的消耗,降低分析成本;降低了劳动强度,改善了工作环境。原子荧光光谱法相对别的分析方法具有灵敏度高、气相干扰少、分析速度快、分析费用低等特点。所以利用微波消解–原子荧光光谱法可以快速有效地测定郁金中的砷含量,且有较好的发展前景。
NOTES
*通讯作者。