1. 引言
化工业的快速兴起,导致含有化肥、农药的废水和废渣大量排放,加重了环境中的铜污染。铜污染在环境中难以用生物进行降解,因此当铜污染一旦沿着食物链不断富集,进入人体,造成体内铜含量超标,就会对人体产生不良影响。因此,降低和消除环境中过量的铜成为了必然的趋势。当前,去除废水中过量铜离子的常见方法有吸附法、电解法、离子交换法和膜分离法等 [1] [2] [3] [4] [5],但这些处理方法在操作费用、处理成本和效果等方面均有各自的优势和不足。诸多方法相比,用生物炭吸附重金属铜是一种有效的技术手段,能够减轻甚至消除铜产生的危害。生物炭的材料来源一般为农林废弃物。因此,将生物炭作为新的吸附材料有非常好的应用前景。生物炭具有丰富的孔隙度,比表面积大以及带有许多特殊的官能团,如-OH、-COOH、
以及芳香酸类,因此,生物炭具有非常好的吸附性能和抗分解性能。生物炭由于含有许多以氧化物、碳酸化合物或者氢氧化物形式存在的矿物元素,这些物质有很强的溶解性且溶水后呈现碱性,因此,生物炭也呈现出碱性 [6] [7] [8] [9]。采用不同种类的生物材料制炭,其生成品的孔隙度、比表面积以及表面带电荷量等方面都有较大不同 [10]。此外,热解温度对生物炭性质也有较大影响,通常生物炭的产率随裂解温度升高而降低,而其他的成分,例如灰分、比表面积、孔隙度等却是随温度升高而升高 [11] [12] [13] [14]。
张继义等 [15] 研究在200℃、300℃、400℃、500℃下利用小麦秸秆热解制备生物炭,并分析其对污水中Cu2+的吸附效果。结果表明,当秸秆炭化温度增加时,秸秆内部孔隙增加,提高了生物炭的比表面积,从而增加了对Cu(II)的吸附量。唐行灿等 [16] 利用玉米秸秆在不同温度(200℃、350℃、700℃)下制备生物炭(BC200、BC350、BC700)吸附Cu2+,探讨在不同初始浓度、吸附时间、不同pH条件下对铜的吸附性能。结果表明,随着炭化温度的增加,炭中灰分含量和炭的pH也在增加。这三种生物炭对Cu2+的吸附能力:BC500 > BC700 > BC200;拟合得到的BC200、BC350、BC700的最大吸附量分别为17.1、30.6、27.2 mg/g。蒋艳艳 [17] 研究小麦秸秆炭、花生壳炭、木炭、活性炭4种生物炭在不同浓度、不同吸附时间、不同pH值、不同投加量对水溶液中重金属Cu2+的吸附特征。结果发现小麦秸秆炭、花壳炭和活性炭对Cu2+的吸附在10 h后达到平衡;生物炭用量8 g/L,溶液初始pH为6,小麦秸秆炭、花生壳炭对水中Cu2+的去除率分别为96.12%和92.10%。谢超然等 [18] 研究了在温度298.15 K、pH 3~6条件下,核桃青皮生物炭吸附Cu2+在20 min内即可达到吸附平衡,核桃青皮炭最佳投加量为0.15 g/L,最大吸附量为153.846 mg/g。Gong R. M.、Annadurai G.等国外学者分析出花生壳 [19]、陈皮 [20]、榛子 [21] 等为原材料制备生物炭并对其吸附性能进行了初步的研究。Saito等 [22] 分析得出生物炭径越小,则比表面积越大,吸附效果越好。大多数生物炭呈现碱性,因此溶液的pH值对于生物炭的吸附效果影响较大,刘进阁 [23] 研究结果表明溶液pH越小,生物炭吸附重金属效果就越好,另外,吸附时间对炭吸附量也有较大影响,在短时间内,吸附量呈递增趋势 [24]。
综上所述,利用生物炭作为吸附材料处理含铜废水,所需成本较低,处理装置易于操作,出水水质优良,易于回收再利用等特点,在处理含铜工业废水方面具有现实意义。其次,用于制炭的材料丰富,且多为农业废弃物,因此降低了资源的浪费。在环境问题日益严重的今天,寻找环境友好型的处理废水中铜离子的方法成为了研究的热点,而生物炭正是作为一种绿色无污染的资源,不仅能高效地净化废水中的重金属,而且不会对环境造成污染。本课题旨在将农林废弃物资源化并为生物炭处理废水中Cu2+提供理论依据,也为热带地区重金属污染水体的修复与防治提供技术支持。因此,将生物炭作为新型重金属吸附剂处理废水中的Cu2+具有现实意义。同时椰壳为我国热带地区丰富的农业废弃物,因此将椰壳“变废为宝”合理利用也成为一个难题。椰壳拥有非常丰富的纤维,且学者对于椰壳制成生物炭,并用于吸附重金属的研究较少。为增加对椰壳资源化的处理,本文通过在不同温度下限温热解炭化椰壳制备生物炭,研究其对水中Cu(II)的吸附影响,以便为农业废弃物处理废水中重金属提供理论依据。
2. 材料与方法
2.1. 生物炭制备方法
笔者选用海南来源丰富的农林废弃物椰壳为原材料,将其洗净后烘干,然后敲碎至大小1 cm × 1 cm后置于100 mL坩埚内,用锡箔纸密封置于马弗炉中,采用限氧升温碳化法进行制备:先30 min升温至330℃,恒温60 min,再以每10℃/min速率分别升温至500℃、600℃和700℃,恒温150 min,冷却至室温后取出,分别标记为T500、T600、T700。然后用研钵研磨均匀,再过100目标准检验筛,成品贮存于干燥的样品袋中,待用。
2.2. 试验仪器
电子精密天平(GH-200)、隔膜真空泵(SHZ-D(III))原子吸收光谱仪(PinAAcle 900T)、气浴恒温振荡器(THZ-9213)、酸度计(DELTA320)、马弗炉(JHZ-10-12)、程序控温器(Al-708P)、电热鼓风干燥箱(GZX-9246MBE)。
2.3. 试验方法
2.3.1. 生物炭产率
椰壳生物炭产率的测定:称取部分洗净烘干后的椰壳,放入马弗炉中,进行限氧高温炭化,直到炭化程序结束。当炉内温度降低至常温时,从中取出成品,称取产物的质量。计算不同温度下制备的椰壳炭产率。
炭化产率计算公式为:
(1)
本实验生物炭炭化产率如表1所示。

Table 1. Carbonization yield of coconut shell charcoal
表1. 椰壳生物炭炭化产率
由表1可知,椰壳炭的产率与热解温度有关。随着炭化温度的增加,椰壳炭的产率逐渐降低,同时产率下降的幅度也在逐渐减小。表明生物质材料到炭化后期较难热解,这与其他学者所做的研究结果一致。如罗煜等 [13] 研究报道了芒草热解温度在350℃时,生物炭的产率为47%,而热解温度达到700℃时,生物炭产率则降到了28%。
2.3.2. Cu(II)的测定方法
1) Cu(II)标准曲线的绘制
用原子吸收光谱仪在波长324 nm处,以超纯水为参比,测定浓度为0.00 mg/L、0.10 mg/L、0.20 mg/L、0.50 mg/L、1.00 mg/L、2.00 mg/L铜标准溶液的吸光度,Cu(II)标准曲线的线性关系在0.999以上,可以用来检测,满足分析要求,误差较小。
以Cu(II)浓度为横坐标,吸光度为纵坐标,绘制标准曲线,如图1所示。
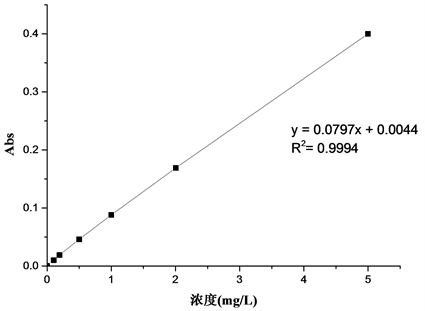
Figure 1. The standard curve of Cu(II)
图1. Cu(II)标准曲线
2) 吸附量计算
吸附量计算公式:
(2)
式中:q为吸附量,mg/g;C0为吸附前溶液中Cu(II)浓度,mg/L;Ct为吸附后溶液中Cu(II)浓度,mg/L;V为溶液体积,L;W为生物炭投加量,g。
2.3.3. 实验设计
本课题选用椰壳为原材料,分别在500℃、600℃和700℃条件下制备生物炭T500、T600和T700。该实验采用单因素实验法,通过静态吸附试验,研究T500、T600和T700在不同的Cu(II)初始浓度、生物炭投加量、溶液初始pH值、吸附时间等四个因素下对水中Cu(II)吸附效果的影响。
2.3.4. 测定方法
1) 不同Cu(II)初始浓度对吸附效果的影响
以0.01 mol/L的NaNO3为背景电解质配制不同Cu(II)初始浓度(10 mg/L、20 mg/L、40 mg/L、45 mg/L、60 mg/L、80 mg/L、100 mg/L、120 mg/L),然后分别称取0.2 g粒径过100目的椰壳生物炭,投入到25 mL不同Cu(II)浓度的溶液中,用0.1 M NaOH、0.1 M HNO3、0.01 M NaOH以及0.01 M HNO3调节溶液pH为4.0 ± 0.1,在30℃下以250 r/min的转速恒温振荡3 h,过滤,测定滤液中Cu(II)浓度,研究不同初始浓度对水中Cu(II)去除效果的影响。
2) 生物炭投加量实验
以0.01 mol/L的NaNO3为背景电解质配制初始浓度为60 mg/L的Cu(II)溶液,然后分别称取不同质量(0.05 g、0.1 g、0.2 g、0.4 g、0.6 g、0.8 g、1.0 g、1.2 g)粒径过100目的椰壳生物炭,投入到25 mL 60 mg/L的Cu(II)溶液中,用0.1 M NaOH、0.1 M HNO3、0.01 M NaOH以及0.01 M HNO3调节pH为4.0 ± 0.1,在30℃下以300 r/min的转速恒温振荡3 h,过滤,测定滤液中Cu(II)的质量浓度,研究不同生物炭投加量对水中Cu(II)去除效果的影响。
3) 初始pH值对吸附效果的影响
以0.01 mol/L的NaNO3为背景电解质配制初始浓度为60 mg/L的Cu(II)溶液,然后分别称取0.2 g的粒径过100目的椰壳生物炭,投入到25 mL 60 mg/L的Cu(II)溶液中,用0.1 M NaOH、0.1 M HNO3、0.01 M NaOH以及0.01 M HNO3调节pH为3、3.5、4、4.5、5、5.5、6,在30℃下以250 r/min的转速恒温振荡3 h,过滤,测定滤液中Cu(II)的质量浓度,研究溶液不同初始pH值对水中Cu(II)去除效果的影响。
4) 吸附时间对吸附效果的影响
以0.01 mol/L的NaNO3为背景电解质配制初始浓度为60 mg/L的Cu(II)溶液,然后分别称取0.2 g的粒径过100目的椰壳生物炭,投入到25 mL 60 mg/L的Cu(II)溶液中,用0.1 M NaOH、0.1 M HNO3、0.01 M NaOH以及0.01 M HNO3调节pH为4.0 ± 0.1,在30℃下以250 r/min的转速恒温振荡0.5 h、1 h、1.5 h、2 h、3 h、5 h、7 h、9 h,过滤,测定滤液中Cu(II)的质量浓度,研究不同吸附时间对水中Cu(II)去除效果的影响。
3. 结果与分析
3.1. 不同Cu(II)初始浓度对三种生物炭吸附水中Cu(II)的影响
T500、T600和T700对水中不同Cu(II)初始浓度吸附量的影响如图2所示。
T500、T600和T700对水中不同Cu(II)初始浓度去除率如图3所示。
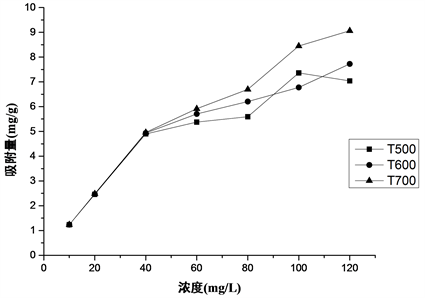
Figure 2. Effect of initial Cu(II) concentration on the adsorption of three biochars to Cu(II)
图2. 不同Cu(II)初始浓度对三种生物炭吸附水中Cu(II)的影响
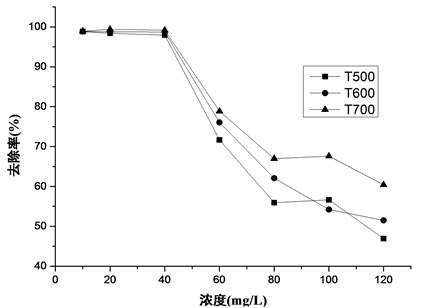
Figure 3. Removal rate of initial Cu(II) concentration of the solution on the adsorption of three biochars to Cu(II)
图3. 三种生物炭对不同初始Cu(II)的去除率
由图2知,生物炭对水中Cu(II)的吸附量与Cu(II)初始浓度密切相关,T500、T600和T700对水中Cu(II)的吸附量整体幅度都是随着溶液初始浓度的增加而增加。由图3可知,随着初始Cu(II)浓度的增加,三种生物炭对水中Cu(II)的去除率则呈现出整体递减的趋势。本试验中投加的椰壳生物炭量一定,所以能提供的吸附位点有限。在一定的浓度范围内,随着溶液中Cu(II)初始浓度不断增加时,吸附量也在逐渐增加,去除率也有小幅度增加然后逐渐递减,但是,当生物炭吸附达到饱和平衡后,就会出现解吸-再吸附现象,吸附量不再增加,去除率则一直在递减。其中,三种生物炭在Cu(II)初始浓度低时都有较大的去除率,对水中Cu(II)的吸附效果较好。其中,T500在初始浓度为100 mg/L时对水中Cu(II)的吸附量达到最大,为7.36 mg/g;T600和T700在初始浓度为120 mg/L时对水中Cu(II)的吸附量达到最大,分别为7.725 mg/g和9.025 mg/g。T500、T600和T700基本均在初始浓度为20 mg/L时达到最大去除率,分别为98.4%,98.7%和98.9%。
3.2. 不同投加量对三种生物炭吸附水中Cu(II)的影响
T500、T600和T700在不同投加量下对水中Cu(II)吸附量的影响如图4所示。

Figure 4. Effect on different doses on the adsorption of three biochars to Cu(II) in water
图4. 不同生物炭投加量对三种生物炭吸附水中Cu(II)的影响
T500、T600和T700在不同投加量下对水中Cu(II)去除率如图5所示。
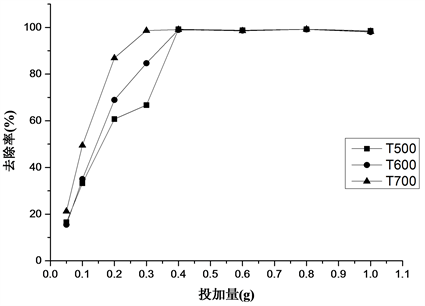
Figure 5. Removal rate of different doses the solution on the adsorption of three biochars to Cu(II) in water
图5. 三种生物炭在不同投加量下对水中Cu(II)的去除率
由图4可知,T500、T600和T700对水中Cu(II)的吸附量均先随着投加量的增加而增加然后呈现递减的趋势。当溶液中投加的生物炭量较少时,生物炭上的吸附位点能全部被Cu(II)占据,因此出现了短暂吸附量增加的现象。当炭量不断增加时,炭的对Cu(II)的吸附量出现整体下降的趋势。这可能与吸附剂的溶解性、结合位点之间的静电感应和排斥作用有关 [25]。由图5可知,随着炭量的增大,溶液中Cu(II)的去除率先快速增长,最终趋于稳定。这主要是由于吸附剂投加量的增加,总官能团数和有效的吸附点位增加,因此,重金属离子的去除率也随之增加 [26] [27]。实验数据表明:当投加量为0.2 g时,T500、T600和T700的吸附量均达到最大,分别为6.073 mg/g、6.896 mg/g和8.689 mg/g。当投加量为0.4时T500、T600和T700对水中Cu(II)的去除率均达到最大,接近于全部吸附。综合考虑三种生物炭投加量对Cu(II)吸附量,可以确定T500、T600和T700的最佳投加量为4 g/L。
3.3. 不同溶液pH值对三种生物炭吸附水中Cu(II)的影响
T500、T600和T700在不同pH值下对水中Cu(II)溶液吸附量的影响如图6所示。

Figure 6. Effect on the pH value of the solution on the adsorption of three biochars to Cu(II)
图6. 不同溶液pH值对三种生物炭吸附水中Cu(II)的影响
T500、T600和T700在不同pH值下对水中Cu(II)去除率的影响如图7所示。

Figure 7. Removal rate of the pH value of the solution on the adsorption of three biochars to Cu(II)
图7. 溶液pH值对三种生物炭对Cu(II)的去除率
由图6、图7可知,弱酸和中性条件下,T500、T600和T700对水中Cu(II)的吸附量和去除率都是随着pH的增加而增加,最终趋于稳定;并且当pH在3~4.5时,生物炭对Cu(II)的吸附比较明显,当pH在4.5~6时,吸附量和去除率存在较小波动。随着pH值的升高,T500、T600和T700表面所带的负电荷和表面有机官能团的酸离解度增加,且pH值的升高更有利于重金属离子水解 [28]。实验数据表明,三种生物炭在pH为3~6时,对水中Cu(II)有良好的去除效果,在其他条件一定时,T700在pH为5时吸附容量已基本达到最大,为6.303 mg/g,去除率达到84%,该吸附反应适应的pH范围较宽,这对于将T700应用于实际操作有现实意义。
3.4. 不同吸附时间对三种生物炭吸附水中Cu(II)的影响
T500、T600和T700在不同吸附时间下对Cu(II)溶液吸附量的影响如图8所示。
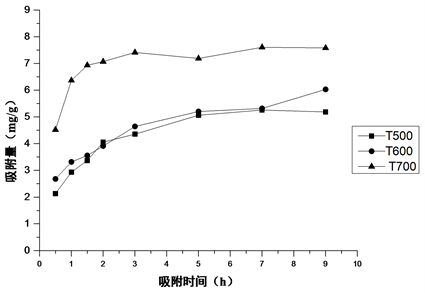
Figure 8. Effect of the adsorption time on the adsorption of three biochars to Cu(II)
图8. 不同吸附时间对三种生物炭吸附水中Cu(II)的影响
由图8可知,T500、T600和T700对水中Cu(II)的吸附量都是随着吸附时间的增加先增加然后逐渐趋于稳定。其中,在最初的0.5~3 h之间,三种生物炭对水中Cu(II)的吸附速率较快,在吸附1 h后,吸附效率已达近一半的量,吸附量增幅较大;在3 h后,三种生物炭的吸附过程基本到达稳定。由于在吸附开始时生物炭上吸附位点较多,不存在竞争反应,因此吸附量是逐渐增大。但由于吸附位点有限,随着吸附时间的增加,吸附位点不断被占据而逐渐饱和,吸附量则不再增加,从而达到吸附平衡 [29]。实验数据表明,在达到平衡的3~9 h内,在同一吸附时间下,Cu(II)的吸附量大小顺序为T700 > T600 > T500。综合考虑,在其他条件相同下,T700在吸附时间为3 h,对水中Cu(II)的吸附效果最好。
4. 结论
本实验以海南省来源广泛的椰壳作为原材料,分别在500℃、600℃和700℃条件下制备生物炭T500、T600和T700。研究三种温度制备的椰壳生物炭在不同初始浓度、生物炭投加量、溶液初始pH值以及吸附时间等因素对水中Cu(II)的吸附特征。研究结论如下:
1) 三种温度下制备的椰壳生物炭对水中Cu(II)都具有较好的吸附效果,在相同条件下,三种生物炭的吸附能力:T700 > T600 > T500。
2) 在水中Cu(II)初始浓度为60 mg/L,投加量为0.2 g,pH为4,吸附时间为3 h时,T700的最大吸附量达到8.6833 mg/g。
NOTES
*通讯作者。