1. 引言
在目前工业社会快速发展的状态下,同时也产生了一些污染气体,其中一些代表性的挥发性物质例如甲醛、乙醛、苯、甲苯、苯乙烯等对人类的危害巨大。由于光催化可以有效降解有机污染物,因此有人提出用光催化来降解这些残留物。现如今,至少将近三分之二的半导体光催化剂都是禁带宽度为n型的半导体材料,在目前活性比较高的三种半导体材料中,CdS和ZnO在自然条件下的腐蚀现象对环境造成了极大的危害。因此在各种光催化剂中,TiO2在紫外光下表现出良好的降解速率,且TiO2具有较高光催化活性、亲水性、成本低,因此在近来研究中广受欢迎。
本文先论述了TiO2催化有机污染物的降解机理,而后综述了近年来TiO2在不同掺杂方式下的改性,并分析了不同掺杂情况下TiO2的催化性能,而后着重介绍了TiO2负载方面的研究进展,最终文章结尾给出了TiO2催化降解方面的研究方向。
2. 二氧化钛催化有机污染物降解机理
TiO2光催化剂是一种半导体,由价带、导带和禁带组成。TiO2光催化剂带隙为3.2 eV,当吸收的光子能量要大于等于该数值时,将会发生电子跃迁,VB上的电子就会激发至CD上,同时VB上形成带正电的空穴h+。此外电子具有还原性,电子由禁带过渡到价带上,与氧气生成具有强氧化能力的自由基
,而VB上的带正电的空穴h+与H2O以及O2生成羟基
。二者能够显现出较强的氧化能力。图1为二氧化钛光催化剂机理。
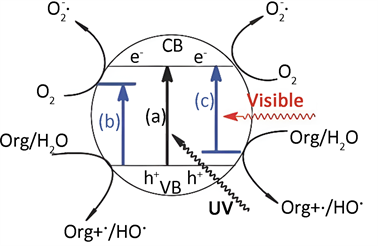
Figure 1. Principle of TiO2 photocatalytic degradation of organic pollutants [1]
图1. TiO2光催化降解有机污染物原理 [1]
TiO2表面催化反应方程 [2] 如下
在此基础下,可将有机污染物降解为无污染性化合物释放出去,比如CO2、H2O等。此外,由于产生的高活性空穴h+和光生电子易复合,不利于反应的进行,而其易复合的原因取决于电子结构、反应条件、敏化剂种类等多种因素 [3],这里采用对光催化剂进行光敏化 [4],进一步提高二氧化钛的催化活性 [5]。光敏化后TiO2与纳米TiO2反应机理见图2。
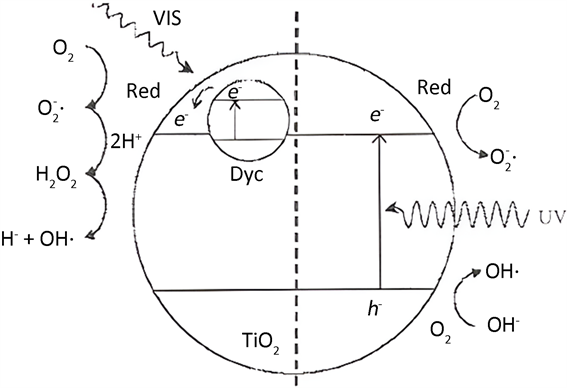
Figure 2. Schematic diagram of photocatalysis principle of nano TiO2 (right) and photosensitized (left)
图2. 纳米TiO2(右)和光敏化后(左)光催化原理示意图
在此基础下,纳米TiO2光催化剂可以有效的净化室内空气,去除有机污染物。
3. 二氧化钛的改性进展
3.1. 非金属掺杂
非金属掺杂就是指将部分非金属元素例如C、N、F等引入TiO2的内部结构中,替代部分氧原子的位置。这样做的目的有两个,一是提高了二氧化钛的导电性,由于非金属元素的加入,客观上促进了由吸收太阳光辐射的能量而产生的光生电子向二氧化钛表面的迁移。二是非金属元素取代了氧的位置形成了部分氧空位,由于这些氧空位的存在,改变了催化剂吸收光谱的范围,与金属掺杂一样,形成了更窄的能带间隙,提高了在可见光区域的活性。
赵豫洁 [6] 在非金属元素N掺杂下,制备了纳米TiO2光催化剂。探究了不同氮源下可见光响应型纳米TiO2的催化活性。在可见光金卤灯的照射下,以硝酸铵(NH4NO3)为掺杂源,在45 min后对RB水溶液的降解率达到了90%,以氯化铵(NH4Cl)为原料,对罗丹明B的降解率在60 min后达到了90%,以硫脲(N2H4CS)为原料,90 min后,降解率达到为94%,优于紫外光照射下的催化性能,并且比纯纳米TiO2高出43%。Chen [7] 等采用液相沉积法,在以Ar/O2/N2为反应气的基础上,制备了N掺杂的TiO2光催化剂。结果表明:三种气体在不同比例下,二氧化钛的晶体存在类型将会呈现出不一样的比例,N的掺杂量越多,催化活性越高,同时在含量较少的紫外光区域也有较高的催化活性,且为未掺杂的光催化剂薄膜催化效率的1.5倍。
李晓苇 [8] 等人制备出了硼氟共掺杂 [9] 的具有催化性能的TiO2透明乳液。在模拟太阳光照射下,以对酸性红3R染料溶液降解为参考标准,该催化剂对其降解率可达98%。秦莲 [10] 等人制备了氮掺杂黑色TiO2光催化剂。实验结果表明:当尿素:黑色花状TiO2 = 2:1时,该催化剂对甲基橙溶液的催化降解效果最好。彭晓叶 [11] 制备了硫掺杂型的S/TiO2光催化剂,在25%乙醇水清洗下,催化剂的回收率以及对MC-LR降解率最高。此外该催化剂对0.1 μg∙mL−1的MC-LR降解率达到100%。陈晓 [12] 制备了N掺杂C/TiO2纳米材料。结果表明:PPY-2对Cr(W)降解率是P25的2.43倍,PPY-3对MB的降解率是P25的2.02倍。
3.2. 金属掺杂
金属掺杂原理是将金属离子例如三价铁,二价锰等引入二氧化钛晶体内部,取代部分钛离子的位置,从而影响二氧化钛的空间内部结构,掺杂一定量的金属离子一定程度上将会缩短价带与禁带的宽度,从而提高可见光的响应度。
刘明 [13] 等人采用溶胶–凝胶法,在金属铜掺杂下,制备出纳米二氧化钛颗粒,对其的表征进行分析,探究了金属掺杂对该复合型催化剂的影响。Cu的掺杂抑制了纳米TiO2相变,并且催化剂光吸收度逐渐提高;此外在温度的影响下,该复合材料在可见光区域有了响应。林卫丽 [14] 过用溶胶–凝胶法,采用多种金属元素(比如铁、钴、镧、铈、铬等金属元素)共同掺杂的形式,制备了金属离子共掺纳米TiO2型催化剂。在光降解过程中,发现多金属掺杂更能提升TiO2的光催化活性。此外,Fe/Zn比例为5:1的情况下共掺杂的效果优于Co/La。
唐丽娜 [15] 等人采用光沉积法,加入了金属铁或铜,制备了二氧化钛光催化剂。当掺杂金属量为1%、银:铜 = 1:1的时,在2 h内,该催化剂对硝酸氮的降解率达到了48.1%,总氮去除率达到34.2%。陈云 [16] 将Co2+、Ni2+、Cu2+、Zn2+、Fe3+、Sn4+等金属离子分别掺杂到TiO2中,制备了摩尔分数为1%的金属离子掺杂M-TiO2材料。实验结果发现Sn-TiO2材料的光催化活性最优,对甲基橙与紫丁香醇的降解率分别是未掺杂TiO2的2倍、6.3倍,其他金属离子无明显提高催化剂的催化活性。
3.3. 贵金属沉积
贵金属纳米粒子,如银、铂、钯和金等,当有光照射其表面时,两种物质之间相互作用,发生等离子体共振效应,因此将其引入催化领域中。贵金属粒子可作为光敏剂来提高TiO2的光催化效率,其一,贵金属具有电子储存特性,且在二氧化钛内部均匀分散,一定程度上促进了电子空穴对的分离。其二,贵金属可以吸收可见光、近红外光,而不单单像二氧化钛仅仅吸收单一光源。
3.3.1. 铂掺杂二氧化钛光催化剂
黄佳木 [17] 等人采用溶胶–凝胶法,通过两种贵金属共同沉积,制备了铂/铬/纳米二氧化钛薄膜复合型催化剂,实验结果表明:在一定时间内,该复合型催化剂在最佳比例Cr:TiO2 = 0.4%;Pt:TiO2 = 0.03%时,对亚甲基蓝的降解率达到95%左右,其催化活性要远高于纯二氧化钛以及单金属掺杂的状况。Sescu Amalia Maria [18] 等人采用等体积浸渍法(IWI)合成了不同贵金属掺杂(Au和Pd)的二氧化钛样品。结果表明,IWI法制备的样品具有较高的光催化活性,且TiO2-Pd/IWI法对2,4-二硝基苯酚(2,4-DNP)的去除率高于TiO2-Au/IWI法。
3.3.2. 银掺杂二氧化钛光催化剂
众多贵金属中,银的成本比较低,而且易制备被认为是良好的贵金属掺杂目标。TEKIN等 [19] 通过光催化分解耐光橙G,结果表明贵金属Ag提高了TiO2对耐光橙G降解率。
喻灵敏等人 [20] 采用浸渍法,在分别掺杂各种贵金属(包括Pt、Pd、Ru、Rh、Au、Ag)的条件下,研究了紫外光下二氧化钛光催化剂的催化性能。实验表明:在Pt和高Ag量的掺杂下,二氧化钛对溴酸盐(
)的降解率相比较纯二氧化钛分别提高了4.6倍和2.9倍。
3.4. 异质结构
二氧化钛禁带宽度较宽一直是其作为催化剂无法忽视的缺点,因此我们可以采用构建异质结的方法解决此问题,我们可以假想一种模型,比如,可以找到一种易激发光生电子的材料(常用半导体带隙能如图3)与二氧化钛复合,那么在太阳光辐射下,此材料上产生的电子转移到二氧化钛表面,在两种材料之间形成一个内部电场,以此来促进电子与正电空穴的分离,具体反应机理见图4。此外我们可以通过找到一种禁带间隙较窄以及在可见光区域有较强的响应度的半导体材料,用它来和二氧化钛进行复合。
丁鹏等人 [23] 采用沉淀法,构建了TiO2-Bi2O3纳米粒子,实验以二甲苯为降解对象,反应180 min后,对二甲苯降解率达到84.0%。李澈 [24] 采用溶剂热法成功构建出花状TiO2单体以及纳米花状β-Bi2O3/TiO2异质结复合型二氧化钛光催化剂,以降解罗丹明B为标准。结果表明:Bi2O3/TiO2异质结复合型催化剂对罗丹明B的降解率由原来的降解率61.2%提升至99.6%,由此可以看出,异质结的成功构建,极大的提升了TiO2的光催化活性。
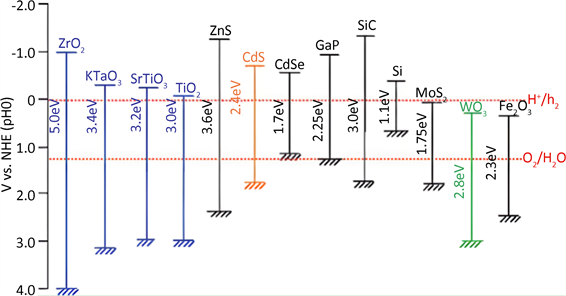
Figure 3. Common semiconductor band gap energy [21]
图3. 常用半导体带隙能 [21]
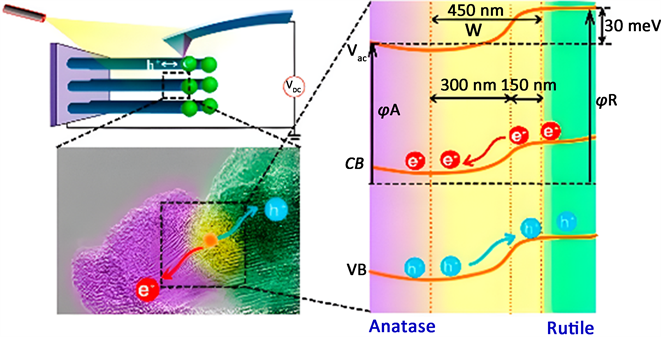
Figure 4. Photogenerated electron and hole transfer direction at the interface of TiO2 heterogeneous junction [22]
图4. TiO2异相结界面上光生电子和空穴转移方向 [22]
Jiang [25] 等人制备出一种新型的TCNQ二氧化钛复合型光催化剂,极大的提高了对苯酚的降解率。Chen Wu Jhang [26] 等人制备Ag/TiO2/ZnO异质结构复合型光催化剂,4 h内对亚甲基蓝的降解率可达83%,比未掺杂时催化剂降解率提高了14%。仓金顺 [27] 等人制备了g-C3N4-TiO2纳米复合材料,在最优比TiO2:尿素 = 1:3的情况下对甲基蓝的降解率达到了98%,且长时间使用下,未出现明显的性能衰退现象。
4. 二氧化钛的负载
在实际应用过程中,TiO2在循环利用以及高效回收方面目前依旧是一个很大的问题,TiO2综合活性影响其应用范围。近来研究中,已经开发出多种二氧化钛负载的材料,以此来改善二氧化钛的活性,增强催化效果。一种是悬浮体系,就是将二氧化钛粉碎,在溶液中与催化物直接充分混合。另一种就是寻找到一种可负载材料,将二氧化钛吸附在其表面,吸附性材料将被降解目标吸附到TiO2表面,增大接触表面积处的降解物浓度,加快反应速度。
4.1. 以硅藻土为载体
王娟等 [28] 采用溶胶–凝胶–低温烧结法将硫掺杂到TiO2上,并且吸附在硅藻土,通过分析在不同比例S/硅藻土的比例下,光催化剂对苯酚的降解率的影响。结果表明,在质量浓度为2.0 g/L,以氙灯为辐照光源,催化剂用量为5 mg/L时,Ti02-xSx/硅藻土负载型光催化剂降解苯酚的效率最高。孙怀虎 [29] 等以废弃硅藻土为目标,对废弃硅藻土进行表面改性,再将二氧化钛负载其表面。在改性硅藻土与二氧化钛的光催化降解协同作用,对甲醛的降解率高达95.59%。
4.2. 以纳米纤维为载体
上海师范大学刘灵娜 [30] 以浸渍法制备复合型催化剂,以纳米纤维为载体,在光照5小时后,纯TiO2对甲醛的降解率达到了55%左右,而聚丙烯腈/TiO2催化剂复合催化剂对甲醛的降解效率为74%。其次此实验使用粘结剂来改性纳米纤维/TiO2催化剂,通过加入壳聚糖,以此来解决其结合不牢固的问题。结果表明:在粘结剂在3%左右时,甲醛降解率最好。而改性后的纳米纤维/二氧化钛复合材料比原先的催化效果更好。
4.3. 以玻璃珠为载体
赵静 [31] 在玻璃珠上负载TiO2,制备了负载型TiO2光催化剂。负载型TiO2小于未负载的催化剂的催化活性,但是它实现了易分离、循环利用等特性,并且达到了透光性好,均一的效果。
4.4. 以蛋白土为载体
李曙光等 [32] 采用四氯化钛,载体蛋白土作为钛源,制备负载型催化剂,当负载量在20%时,对罗丹明B的降解率最高,且对TiO2的负载量较大,但二氧化钛无法进入蛋白质孔隙,因此还有待提高。但相比较与其他载体而言,蛋白土作为载体还是有明显的优势的。
5. 结语与展望
综上所述,近年来,以TiO2为催化剂的研究快速发展,但由于TiO2的能带间隙宽,在可见光区域无响应以及光生载流子与空穴易复合问题阻碍了TiO2催化降解的步伐。因此对TiO2进行改性,减小禁带间隙尤为重要。无论是通过非金属与金属掺杂还是贵金属沉积,在一定程度上都是在改变催化剂的能带间隙,增强其吸收光的范围,活化能量降低,也就是可以在较低的能量辐射的情况下,依旧可以有大量的光生电子跃迁,从而促进正向反应的顺利进行,使跃迁的电子以及产生的羟基都得到较高的利用率。
为此对今后二氧化钛催化降解有机污染物的研究给出三个方向:
1) 相比较于单元素掺杂,多元混合掺杂更具有优越性,可采用多金属元素或者金属元素与非金属元素共掺杂的形式。此外,贵金属掺杂能够促进电子空穴对的分离,显著降低了电子–空穴的复合速率,从而促进氧化还原反应进程,TiO2掺杂能级示意图见图5。因此,采用贵金属与非金属共掺,即能拓宽光谱响应宽度,又能防止内部电子–空穴的复合。

Figure 5. Schematic diagram of TiO2 doping energy levels [33]
图5. TiO2掺杂能级示意图 [33]
2) 构建异质结,加入新型半导体材料,与二氧化钛之间形成间接联系,目的是为了解决二氧化钛对可见光区域无活性同时改变二氧化钛能带间隙的问题。构建一个复合模型,找到一种半导体材料且在可见光区域有较高的活性与二氧化钛形成复合材料,形成内部电场,并且利于半导体材料表面的电子转移到二氧化钛表面,以此来弥补二氧化钛仅对紫外光区域响应的缺点。
3) 寻找新型负载材料,将二氧化钛负载其表面,以此改变二氧化钛的内部结构,比如基于多孔陶瓷 [34]、磁性复合材料 [35] 等。鉴于目前硅藻土虽然依旧有良好的优势,但其改善程度还没有达到理想的高度,因此寻找新型复合材料,或者更改负载材料的形状来进一步提高二氧化钛的循环利用率。