1. 引言
TAVR自问世以来,取得快速发展,目前已成为高龄高危主动脉瓣疾病患者的一线治疗手段 [1] [2]。尤其对于心功能差、存在多种合并症或存在外科手术禁忌等问题无法行开胸手术的患者来说,更可能是唯一的解决办法。作为一项诞生不久的新技术而言,适应症不断拓宽的同时,并发症也是无法避免的问题,其中影响预后最常见的即PVL,多项研究结果表明,TAVR术后PVL的发生率为50%~85%,绝大数为轻度PVL,中重度PVL发生率则高达9%~21% [3] [4],而中度以上的反流普遍将对患者长期生存产生严重的影响,需要积极治疗。在Kahlert等的研究中,约21%的PVL患者群体,即使使用了球囊后扩张和“瓣中瓣”等干预措施,PVL仍是晚期死亡率的重要预测因素 [5]。本文通过分享一例用多个封堵器封堵严重复杂PVL的病例为研究介入治疗PVL提供一定的参考。
2. 病例介绍
患者男性,74岁,主诉因“全身乏力4月余”于2022年8月4日入院。患者诊断主动脉瓣重度狭窄伴关闭不全20年,间断出现双下肢水肿,2年前因“突发胸痛6小时”至我院急诊内科就诊,完善心电图及心肌酶化验,诊断为急性ST段抬高型心肌梗死,急诊行冠脉造影+血栓抽吸术,手术顺利,术后行经胸超声心动图(TTE)结果显示:主动脉瓣重度狭窄伴关闭不全[主动脉瓣显著增厚,钙化,右冠瓣与左冠瓣交界处粘连、融合,开放受限,收缩期峰值流速4.2 m/s,峰值跨瓣压差71 mmHg (1 mmHg = 0.133 kPa),关闭欠佳,舒张期见中度反流],左心室射血分数(LVEF) 25%,后转入心外科行手术治疗,入院诊断:急性ST段抬高型心肌梗死,主动脉瓣狭窄(重度)伴关闭不全(中度),持续性心房颤动,2型糖尿病,纽约心脏病协会(NYHA)心功能IV级。2020年2月14日行经导管主动脉瓣置换术(TAVR),术中置入VenusA-Valve L29人工瓣膜一枚,释放完毕后行主动脉造影见由于瓣环钙化严重,导致瓣膜释放后位置偏深,瓣周反流较重,决定应用“瓣中瓣”技术再次置入一枚VenusA-Valve L29人工瓣膜,释放后造影显示瓣膜形态不良,中–重度瓣周漏,使用NUMED 25 mm球囊反复多次进行后扩张,扩张后见瓣膜形态好转,瓣周漏好转。术中经食道超声心动图(TEE)示:主动脉瓣瓣口收缩期峰值流速2.6 m/s,峰值压差27 mmHg,舒张期左室流出道内探及源于主动脉瓣周右后方的中–重度反流,瓣口见轻度过瓣反流,LVEF 30%。术后患者恢复良好出院。后患者因心力衰竭于2022年5月5日再次住院治疗,复查TTE示:主动脉瓣位人工瓣,瓣口开放正常,收缩期峰值流速2.5 m/s,最大跨瓣压差24 mmHg,多普勒指数速度(DVI) 0.3,舒张期轻度过瓣口反流,人工瓣环外侧见重度瓣周漏反流,心肌梗死后改变,左室壁节段性运动异常,LVEF 29%,后经保守治疗症状明显改善,于2022年6月20日出院。
2022年8月4日患者因“急性心力衰竭”再次入院,既往有糖尿病、冠心病、心房颤动病史,手术史如前所述,个人史、家族史无特殊。入院体格检查:体温36.3℃,脉搏82次/min,血压120/62 mmHg;心率82次/min,家属搀扶下步入病房,颜面部潮红,颈部未闻及血管杂音,双肺呼吸音清,双下肺少许湿性啰音,心律绝对不齐,主动脉瓣第一、二听诊区可闻及III/6级舒张期隆隆样杂音,向胸骨传导;腹部饱满,腹软无压痛,查体无阳性体征;双下肢指凹性水肿。
十二通道心电图结果示:异位心律,心房颤动,室性早搏,完全性左束支传导阻滞。TTE示:主动脉瓣位人工生物瓣,收缩期峰值流速2.5 m/s,最大跨瓣压差24 mmHg,DVI 0.44,舒张期轻见微过瓣口反流,于人工瓣环外侧见重度瓣周反流,LVEF 29%,左心室舒张期内径7.3 cm,陈旧性心肌梗死改变,左室壁节段性运动异常,二尖瓣轻–中度反流,三尖瓣轻–中度反流,左心功能重度减低,肺动脉轻–中度高压,全心扩大,升主动脉扩张,心房纤颤。主动脉CTA影像显示主动脉根部植入两枚Venus-A瓣膜,外瓣膜支架最深处为13 mm,内侧瓣架植入深度约2 mm,瓣环平面支架呈椭圆形,支架外侧可见严重团块状钙化斑块,CTA及3D剖视图可见三处漏口位于左冠窦,最宽处近8 mm (图1)。患者术前诊断为急性心力衰竭,心脏瓣膜置换术后瓣周漏(重度),冠状动脉粥样硬化性心脏病,心房颤动,心功能IV级(NYHA分级),主动脉瓣生物瓣置换状态,2型糖尿病,陈旧性心肌梗死,完全性左束支传导阻滞。
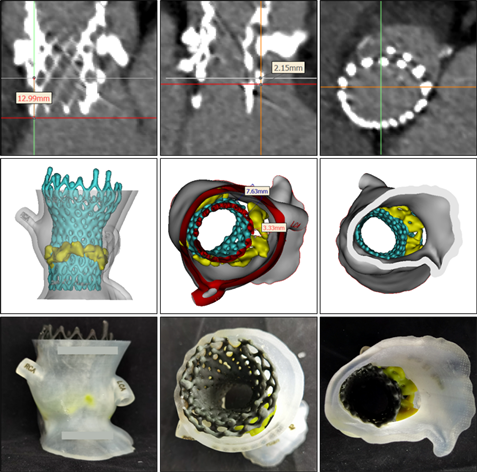
Figure 1. Preoperative CTA and 3D section view (the deepest part of the external valve scaffold was 13 mm, the implantation depth of the medial valve scaffold was about 2 mm, and the three leakage openings were located in the left coronary sinus, and the widest part was nearly 8 mm)
图1. 术前CTA及3D剖视图(外瓣膜支架最深处为13 mm,内侧瓣架植入深度约2 mm,三处漏口位于左冠窦,最宽处近8 mm)
手术术前讨论患者情况,TAVR“瓣中瓣”术后重度瓣周漏,心功能较差。TTE及CTA结果示人工支架瓣膜位置良好,功能良好,瓣周漏位置孤立,考虑与既往钙化位置相关,可考虑介入瓣周漏封堵治疗。次选方案可考虑外科开胸主动脉瓣置换或心脏移植。开胸手术术中可探查解剖主动脉根部,取出支架瓣膜更换外科人工瓣膜,必要时考虑行带主动脉瓣人工血管替换手术,以解决主动脉瓣瓣环严重钙化带来的瓣周漏问题,但患者基础状况差,开胸手术风险极高,心脏移植更需要合适的心脏供体配型,综合考虑决定为其行介入封堵治疗。术前加用3D打印技术建立起患者主动脉瓣处瓣膜及瓣周模型,并模拟多枚封堵器置入术后状态(图2)。于2022年8月6日在全麻下行经导管主动脉瓣瓣周漏封堵术。
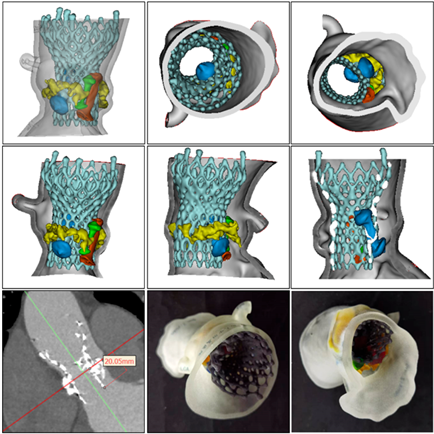
Figure 2. 3D sectional view and printed model (perivalvular leakage is well occluded and there is no risk of coronary obstruction)
图2. 3D剖视图及打印模型(可见瓣周漏封堵良好且无冠脉阻塞风险)
手术过程(图3):全身麻醉后穿刺右侧股动脉置入6Fr血管鞘,肝素化(1 mg/kg),经鞘管送6Fr猪尾导管行升主动脉造影,造影显示主动脉瓣人工瓣膜瓣周漏,程度达到极重度,更换Fusmart 6Fr可调弯导管,由超滑导丝引导至左冠窦处造影探及左冠窦侧PVL1处,并经术中TTE证实;结合术前CTA及3D模型模拟评估(图4),在S曲线中确定左冠切线位投照角度,并在此角度下经数字减影血管造影(Digital Subtraction Angiography, DSA)引导,由直头超滑导丝引导导管穿过PVL口至左心室,随后更换提前塑形后的超硬导丝(Amplatz Super Stiff, Boston Scientific)建立轨道。沿导丝使用5Fr封堵器介入输送装置(上海形状记忆合金材料有限公司)输送ADOII08封堵器(上海形状记忆合金材料有限公司)至左心室,于左心室内释放左伞盘,回撤输送鞘至PVL口处,于主动脉侧释放右伞盘,透视下见封堵器形态良好,位置理想,腰征明显,完成第1枚6 mm ADOII释放。术中TTE提示瓣周反流较前明显改善,程度接近中–重度。
继续在第1枚封堵器旁造影,探查到1处左冠脉窦侧较明显PVL,结合术前CTA及3D模拟评估,沿上述同样方法再次置换鞘管后置入第2枚封堵器,仍选择6 mm ADOII。封堵器释放后位置良好。TTE提示2枚封堵器位置良好,瓣周反流较前减少,程度已达到中–重度。遂在已植入封堵器旁再次造影探
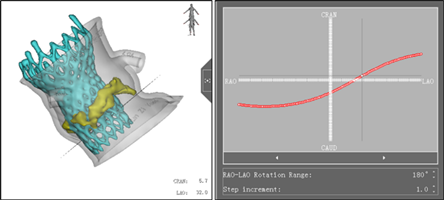
Figure 4. Preoperative CTA evaluation (in S-curve, the Angle of the left crown tangent was determined as LAO32 CRA6)
图4. 术前CTA评估(在S曲线中确定左冠切线位投照角度为LAO32 CRA6)
查,发现仍有一处较明显PVL。因已释放两枚封堵器,瓣周空间有限,再次交换鞘管困难,遂更换0.035 mm × 260 cm超滑导丝穿过该PVL处,并穿刺左侧股动脉置入6Fr血管鞘,经鞘管送6Fr造影导管,置入20号圈套器(上海形状记忆合金材料有限公司),使用圈套器抓捕超滑导丝(LOOP法)建立轨道,引导输送鞘管通过PVL,释放第三枚封堵器,仍选用6 mm ADOII,释放后再次行升主动脉造影,见主动脉瓣PVL处造影剂量较前明显减少,再次行术中TTE显示患者PVL程度达到轻中度水平,考虑已为患者解决主要问题,根据术前CTA及3D模拟评估PVL位置及大小,其他细小PVL口封堵成功可能性极小,决定结束手术。患者恢复顺利,出院前复查TTE:主动脉瓣位人工生物瓣功能正常,收缩期峰值流速3.0 m/s,最大跨瓣压差35 mmHg,DVI 0.5,LVEF 31%,左心室舒张期内径7.0 cm,中度PVL,左室壁节段性运动异常,二尖瓣轻-中度反流,三尖瓣轻-中度反流,左心功能减低,右心功能减低(轻度),全心扩大,升主动脉扩张。
术前与术后TTE对比见图5。
 (a)
(a) 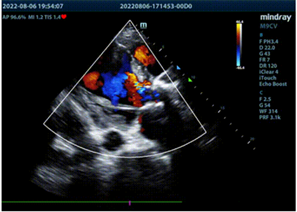 (b)
(b)
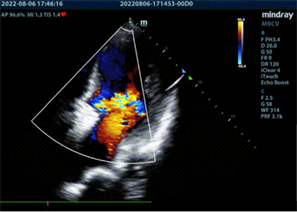
Figure 5. Comparison of TEE before and after surgery. (a): Severe perivalvular regurgitation in apical view; (b): Mild to moderate perivalvular regurgitation in short-axis view, the width of the regurgitation bundle was about 0.2 cm
图5. 手术前后TEE对比。(a):心尖切面显示人工瓣周重度反流;(b):短轴切面显示瓣周舒张期轻中度反流,反流束宽约0.2 cm
3. 讨论
造成TAVR术后PVL的原因主要有主动脉瓣及瓣环严重钙化,导致人工瓣膜支架与主动脉壁贴合差或瓣膜形态不良、人工瓣膜置入深度过深或过浅、选择的人工瓣膜尺寸对于患者本身的瓣环过大或过小等多种原因。当前已有多项研究表明主动脉瓣钙化积分是PVL的独立危险因素 [6] [7] [8]。并且在合并主动脉瓣二叶瓣畸形(Bicuspid Aortic Valve, BAV)的患者中,中度以上PVL的发生率为6%~10.4% [9] [10]。此外,不同类型的人工瓣膜也会影响PVL的发生,球囊扩张式瓣膜由于瓣膜展开的形态相对于自膨式瓣膜来说更可控,所以贴合性也更强,而新一代自膨式瓣膜的裙边设计也能在一定程度上减少PVL的发生 [4] [11] [12]。
绝大多数PVL患者由于仅为轻度PVL,没有明显的临床症状,但是仍有少数患者瓣周反流程度较高,有研究显示术后中度以上的反流普遍将对患者长期生存产生严重的影响甚至出现急性心力衰竭等严重后果,需要积极治疗 [5] [13],TAVR术后严重PVL是近期和远期死亡的独立危险因素。严重PVL患者TAVR术后1年死亡风险是中度以下PVL患者的2~4倍 [14]。二次外科修复或二次换瓣目前仍然是治疗PVL的标准治疗方式,但是二次开胸手术往往因为技术难度大,风险高,手术死亡率高,故而很多患者不愿选择二次手术。根据当前医疗技术的发展,除了外科手术,我们应对TAVR术后PVL的方法还有球囊后扩张、瓣中瓣置入、经导管PVL封堵等措施 [15]。球囊后扩张术是大多数TAVR术中因瓣膜形态不良导致PVL的处理方法,对于瓣膜置入过深或过浅以及选择的人工瓣膜尺寸对于患者本身的瓣环过大或过小的情况,则通常采取“瓣中瓣”的方式来改善瓣周反流。而对于上述两种方法都无法解决尤其是因主动脉瓣根部严重钙化造成人工瓣膜支架与瓣环之前留有腔隙或隧道导致的PVL,我们可以优先考虑介入封堵。目前对于TAVR术后PVL的介入封堵治疗的研究数量有限,国内外报道多为个案报道或小样本研究。Waterbury等人 [16] 的单中心研究回顾性纳入TAVR术后重度PVL患者行介入封堵治疗18例,术中有44%的患者使用PVL专用封堵器AVP2,56%的患者使用AVP4,手术技术成功率为78% (PVL降至中度及以下)。Feldman等人 [17] 为研究经4-5Fr造影导管使用小型号封堵器AVP4封堵PVL的可行性,回顾性的分析了TAVR术后行介入封堵PVL的患者6例,6例患者术中均成功释放封堵器,其中1例患者更是置入了2枚AVP2。6名患者平均随访时间为5个月(1~11个月),5例患者术后瓣周反流程度由中度以上减少至中度以下,只有1例患者PVL术后严重程度无明显减少,并且该患者在1个月后死亡,而剩余5名存活的患者则仍然没有心力衰竭的表现 [18]。国内近期也有1例对TAVR术后PVL尝试封堵的报道,但由于患者本身心脏大血管复杂的解剖结构及较大的输送鞘导致出现输送鞘嵌顿现象,术中曾试图通过提拉技术拔出嵌顿的输送鞘,但最终导致瓣膜脱出而不得不中转外科手术 [19]。
本文报道的是1例采用多枚封堵器封堵Type1型严重钙化的带嵴二叶瓣TAVR“瓣中瓣”术后重度PVL并且取得良好效果的病例,证明了除了外科修复或再次换瓣以外,介入封堵对于主动脉瓣置换术后严重PVL治疗的可能性。在TAVR术后PVL的评估环节,传统的评估方法主要是主动脉CTA和TTE,但这两种方式都存在一定的局限性:主动脉CTA受体位及造影剂的影响,有时对于PVL和瓣中过瓣反流的区分有一定难度。TTE则存在测量指标无法明确量化从而导致评估不够准确的问题 [15] [20]。在本例患者测量过程中除了将二者的结果相结合外,还采用3D打印技术模拟打印出了患者主动脉瓣瓣环及前期置入的人工瓣膜的情况。故而大大提高了对PVL位置形态测量、跨瓣优选投照角度确定和反流量大小测量的准确性,并且为3枚封堵器的材质、型号及放置位置的选择提供了参考。本例患者因支架瓣膜及固有钙化团块坚硬,封堵器宜选用材质柔软塑形良好的不覆膜封堵器,如血管塞或ADOII等,考虑较硬质先心封堵器术后残余分流较少,效果更佳,故选择ADOII封堵器。且封堵器若穿过瓣架进行封堵时,需考虑瓣架内生物瓣叶与瓣架的相对位置以及有无冠脉阻塞风险,以确定释放位置,防止封堵器盘片影响生物瓣叶启闭,或损伤人工瓣叶,3D打印技术在避免此类并发症方面有较大优势。打印的主动脉根部模型可以准确且直观地展现解剖结构,可以更准确地选择匹配的人工瓣膜和封堵器。并且将3D打印模型用于手术预演,熟悉解剖结构,缩短实际手术操作时间,尤其对危重和解剖结构特殊患者意义较大 [21]。此外,多种测量方法对于术中轨道的建立也有很大帮助,比如长支架自膨瓣的主动脉内“花冠”结构可能影响PVL通过时导管导丝位置的判断,通过多次模拟试验尝试后发现导丝从未贴壁的支架一侧进入主动脉窦位置可提高手术的技术成功率。
4. 结论
PVL是TAVR常见并发症之一,对术后患者的预后有着显著影响。对于存在严重PVL问题的患者来说,介入封堵治疗不失为一种有效的替代方式,尤其是对于无法耐受外科手术的患者而言。但因多数患者解剖结构复杂,手术难度大,且目前研究多为小样本临床案例,其安全性和有效性仍需更大规模的研究数据来进一步明确。
利益冲突声明
所有作者均声明不存在利益冲突。
NOTES
*第一作者。
#通讯作者Email: Jianglei1126@sina.com