摘要: 氨氮废水对人体和环境有极大的危害,排放前需要降解到一定的浓度。本文采用撞击流技术使氨氮废水和氧化剂臭氧在亚微米级湿式状态下相向碰撞而发生氧化反应,研究降解氨氮的效果。通过测量不同臭氧流量、不同反应时间、不同氨氮初始浓度下的降解率,发现臭氧流量越大、反应时间越长、初始浓度越高,降解率越高。撞击流的作用使氨氮废水和臭氧气流的混合物处在亚微米级的颗粒状态下发生更充分的接触和反应。当臭氧流量为4 L/min、反应时间为60分钟、氨氮初始浓度为60 mg/L时,氨氮降解率为16.52%。
Abstract:
Ammonia nitrogen wastewater is very harmful to human body and environment, and needs to be degraded to a certain concentration before discharge. In this paper, the effect of ammonia nitrogen degradation by ozone was studied by the impinging stream technology, which was used to make ammonia nitrogen wastewater and oxidant ozone collide with each other in a submicron wet state to produce oxidation reaction. By measuring the degradation rate under different ozone flow rate, different reaction time and different initial concentration of ammonia nitrogen, it was found that the greater the ozone flow rate, the longer the reaction time and the higher the initial concentration, the higher the degradation rate. The impinging stream made the mixture of ammonia nitrogen wastewater and ozone gas contact and react in the submicron particle state, which became more fully. When the ozone flow rate was set at 4 L/min, the reaction time was 60 minutes, and the initial concentration of ammonia nitrogen was 60 mg/L, the ammonia nitrogen degradation rate was 16.52%.
1. 引言
氨氮的来源可分为自然因素和人为因素两种。自然因素来源是指自然界的有机物质缓慢分解一定数量的氨,对人体一般不会构成危害,是因其量较分散和浓度低。人为因素来源主要来源于人工固氮制造的氨,其次是在工业加工生产中产生有氨氮的污水,例如炼油、钢铁工业、化肥、肉类加工和饲料加工生产等 [1]。人为因素的氮排放量因分布较集中和浓度高,容易污染环境和危害人体健康 [2] [3]:它会消耗水体溶氧量,使水体中的溶解氧降低,严重时会造成水体黑臭;它会污染饮用水,导致饮用水有异味甚至完全不能饮用;它会加速水体富营养化;它会腐蚀、堵塞管道和用水设备等。氨氮在水体中以NH3分子和
离子两种形式存在,酸性时主要以
存在,碱性时主要以NH3存在 [4]。处理氨氮废水的方法很多,如生物法、化学法、物理法、高级氧化技术法等。高级氧化包括光电氧化、臭氧氧化和光催化氧化等。单一技术处理的结果往往有不足之处,因此出现复合两种技术的研究,例如臭氧协同光催化技术,光电协同光催化技术,光电联合微生物技术。后者可以避免单独使用生物膜技术时的不可控因素,能使出水达到国家排放标准,但是能耗高,容易产生新的污染产物,用电化学技术处理 [5] 实际废水时会使部分污染物发生化学反应,反而使处理变得复杂。撞击流(Impinging Stream,简称IS)的概念最初是在1961年被苏联科学家Elperin [6] 提出,是指两股气–液两相流同轴高速相向流动撞击,在撞击面形成高度湍动,加强相间的传热传质,增强微混合以及相间传递等过程,提高两相接触面和反应效率 [7],在处理污染物方面应该具有很大的优势。本文采用高级氧化技术,利用亚微米级反应器(即撞击流反应器)将废水和氧化剂臭氧的混合物变成亚微米级状态,使其在湿式状态下进行相撞快速反应,实现降解氨氮目的。
2. 实验部分
2.1. 试剂和仪器
实验试剂主要有氯化铵NH4Cl (分析纯)。实验仪器主要包括自制的撞击流装置(1 m长,管径25 cm)、多参数水质分析仪(5B-3B型,兰州连华环保科技有限公司)、臭氧发生器(YX-802,天长市云霄电子科技有限公司)、无油空气压缩机(OTS-550,台州市奥突斯工贸有限公司)、氟塑料泵(25FSB-10L,上海氟鑫泵阀有限公司)、防腐玻璃转子气体流量计(LZB-10WB/4WB,兴化市祥锦流量仪表厂)、分析天平(T-214,北京赛多利斯仪器系统有限公司)等。
2.2. 实验方法
用氯化铵模拟氨氮废水,配制浓度为10~60 mg/L。方法是:准确称取经100℃烘干过的氯化铵(3.819 g)溶于水中,移入1000 mL容量瓶中用无氨水稀释至标线,然后上下振荡,摇匀。此溶液每毫升含1 mg氨氮,即1000 mg/L氨标准溶液以备用。在实验时根据需要再配制所需浓度。
具体实验装置连接图如图1所示。从污水桶(以液位到1/3为准)到撞击流反应管全部容量约5升,因此每次实验配制氨氮废水的体积是5升,所需的氨标准溶液体积根据浓度确定。实验中为了比较撞击流的效果,先把200 mL氨氮废水倒进烧杯,再直接通臭氧,使其和氨氮废水反应,测氨氮前后的浓度,求降解率。然后将同样浓度的5 L氨氮废水倒进污水桶,经撞击流反应管与臭氧反应,经过一定的时间,取样测量废水的氨氮浓度,求降解率。根据测得的氨氮浓度计算氨氮降解率,氨氮降解率公式如式(1)所示:
(1)

Figure 1. Schematic diagram of experimental connection ① sewage tank, ② fluoroplastic pump, ③ liquid flow control valve, ④ discharge valve, ⑤ impinging stream reactor, ⑥ ozone flow control valve, ⑦ ozone generator, ⑧ jet, ⑨ air flow control valve, ⑩ oil-free air compressor
图1. 实验连接示意图。① 污水桶、② 氟塑料水泵、③ 液体流量调节阀、④ 排污阀、⑤ 撞击流反应器、⑥ 臭氧流量调节阀、⑦ 臭氧发生器、⑧ 射流器、⑨ 空气流量调节阀、⑩ 无油空气压缩机
对不同的臭氧流量和不同的氨氮初始浓度在不同的反应时间下测量氨氮浓度的变化,根据式(1),比较各种情况下的降解率。
2.3. 实验结果和分析
2.3.1. 不同臭氧流量对氨氮降解率的实验结果
保持氨氮废水浓度为30 mg/L和反应时间为60分钟,通过调整图1的⑥臭氧流量调节阀,改变臭氧的流量来测试不同臭氧流量对氨氮降解率的影响,流量分别选择为1 L/min、2 L/min、3 L/min、4 L/min,先让其在烧杯中与氨氮废水进行充分反应,每间隔10分钟停止反应,取样测定每一时刻的氨氮浓度并记录数据,待反应60分钟后结束实验。然后改为在撞击流反应器中反应,步骤与烧杯的实验一样。实验结果如图2~5所示,从图结果发现撞击流反应的效果均比烧杯反应效果好,相同反应时间下,随着臭氧流量的增加,两者的降解率均有提高,撞击流的值与烧杯的值的差距也增加。臭氧氧化过程通常认为主要有两个氧化途径,当pH < 4时以直接氧化为主,当pH > 4时以间接氧化为主。前者有选择性,后者无选择性,主要是利用臭氧在水中的分解产物之一,即具有强氧化性的羟基∙OH对物质的氧化,反应迅速,与废水反应后主要生成氮气N2和硝酸根离子
。在烧杯反应中,臭氧在氨氮废水中停留时间较短,传质不充分进而产生较少的∙OH,臭氧氧化氨氮的反应速率慢,降解效果较差,一般不超过10% [8]。相对而言,臭氧在撞击流反应器中与氨氮废水充分接触能够形成较多的∙OH,大大提高臭氧的分解率,使反应更迅速,所以在反应时间相同的情况下在撞击流反应器中降解效果更好。撞击流效果比直接反应的烧杯效果好,因此后面实验只测量撞击流反应下的数据。
2.3.2. 不同的反应时间对对氨氮降解率的实验结果
保持氨氮废水浓度为40 mg/L和臭氧流量为4 L/min,经撞击流反应器,测不同的反应时间下氨氮浓度的变化,比较降解率随着时间的变化。实验结果如图6所示。反应时间越久,氨氮降解率越高,但从提高的速率来看,一开始提高得快,10分钟比5分钟提高约2个百分点,这是因为氨氮初始浓度大,可与臭氧充分接触反应;然后开始提高得慢,从10分钟到25分钟之间每增加5分钟提高的百分点不到1,是因氨氮浓度下降导致的;反应半小时后,发现提高速度变快,从30分钟到60分钟之间每增加5分钟提高的百分点从1升到1.7,由于氨氮废水反应前是弱酸性的,而∙OH自由基的生成速度因在酸性溶液中会受到抑制,当反应半小时后氨氮被降解部分后使得 值升高,酸性减弱,从而臭氧流量不变的情况下会产生更多的∙OH自由基,进而促进反应的进行;反应1小时到2小时之间的1个小时,降解率只提高1.8个百分点,因氨氮浓度下降,氨氮被降解的速度开始变得很缓慢,降解率趋于稳定。
2.3.3. 不同的氨氮初始浓度对氨氮降解率的实验结果
保持臭氧流量为4 L/min和反应时间为60分钟,通过配制不同的氨氮初始浓度,分别为:10 mg/L、20 mg/L、30 mg/L、40 mg/L、50 mg/L、60 mg/L,测量氨氮的降解率随初始浓度的变化,实验结果如图7所示。初始浓度越大,降解率越高,但随着浓度增加,降解率的提高速率变小。在撞击流作用下,初始浓度越大的氨氮溶液与臭氧气流发生接触反应得越充分,因此降解率越高;浓度越低,反应得越不够充分,因此降解得较少。值得注意的是,对于更高浓度的氨氮废水,要降到排放标准 [9],则需要更多的反应时间。
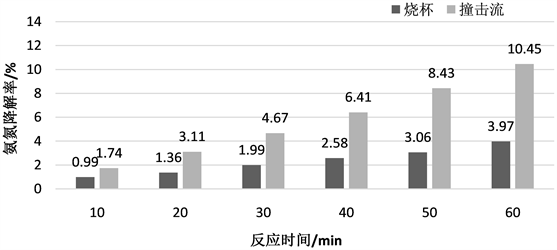
Figure 2. Relation between the degradation rate and reaction time in case of ozone flow at 1 L/min
图2. 臭氧流量1 L/min下降解率与反应时间关系

Figure 3. Relation between the degradation rate and reaction time in case of ozone flow at 2 L/min
图3. 臭氧流量2 L/min下降解率与反应时间关系
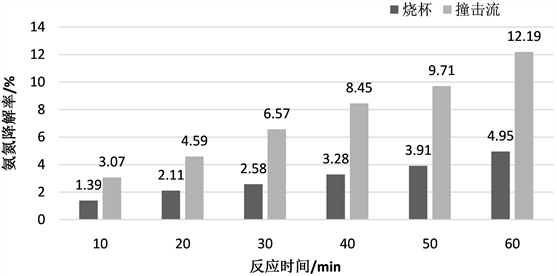
Figure 4. Relation between the degradation rate and reaction time in case of ozone flow at 3 L/min
图4. 臭氧流量3 L/min下降解率与反应时间关系
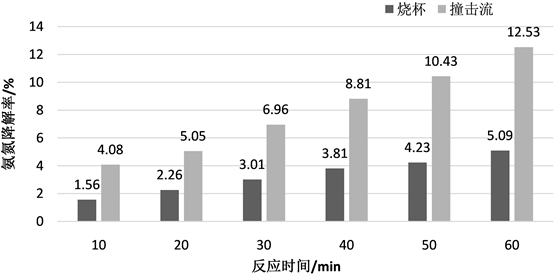
Figure 5. Relation between the degradation rate and reaction time in case of ozone flow at 4 L/min
图5. 臭氧流量4 L/min下降解率与反应时间关系
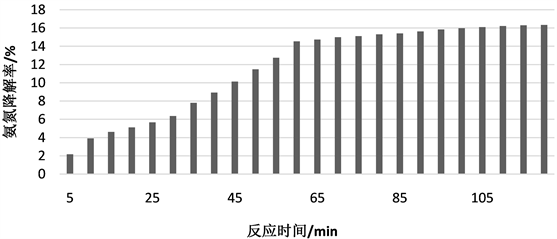
Figure 6. Effect of different reaction time on degradation rate of ammonia nitrogen under impinging stream
图6. 撞击流下不同反应时间对氨氮降解率的影响

Figure 7. Effect of different original concentration on degradation rate of ammonia nitrogen under impinging stream
图7. 撞击流下氨氮不同初始浓度对降解率的影响
3. 结论
本实验研究了烧杯和撞击流反应器下臭氧对氨氮模拟废水的降解效果,发现撞击流效果比烧杯效果好。通过测量不同臭氧流量、不同反应时间、不同氨氮初始浓度下的降解率,发现臭氧流量越大、反应时间越长、初始浓度越高,降解率越高,臭氧流量在4 L/min、反应时间60 min、初始浓度为60 mg/L时,降解率最高,为16.52%,超过了臭氧单独氧化氨氮的降解率的最高极限值10% [8]。撞击流技术使得氨氮废水和臭氧气流的混合物处在亚微米级的颗粒状态下发生更充分的接触和反应,对臭氧直接降解氨氮起到促进作用,对氨氮废水的处理能够提供有一定价值的参考作用。如果再联用其他技术,例如添加光照或催化剂等,会得到更高的降解率,便能确定较高效的氨氮废水处理工艺。
基金项目
佛山科学技术学院实验室开放创新基金一般项目“亚微米级湿式氧化处理氨氮废水研究”。
NOTES
*第一作者。
#通讯作者。