1. 引言
随着现代科学与医疗技术的不断发展,医学图像已成为临床诊断中不可或缺的材料之一。相关医护人员通过使用现代高性能成像医疗仪器,对患者相关部位进行扫描,来获取该部位的生理结构信息以及与诊断密切相关的病变信息 [1]。当前,使用较多的成像技术有电子计算机断层扫描(Computed Tomography, CT)、核磁共振成像(Magnetic Resonance Imaging, MRI)、超声波成像(Ultrasound, US)以及X射线等。
近年来,由于超声检查是一种便捷、可靠、及时的诊断技术,相比于计算机断层扫描、核磁共振、X射线,超声检查已成为健康人群或者亚健康人群的初步筛查的首选,已被广泛用于临床诊断。与此同时,相关的医务人员也可避免因工作带来的射线损伤。超声检查在临床的应用包括对复杂临床图像的诊断与治疗,例如血液动力学不稳 [2]、急性呼吸衰竭 [3] 或心脏骤停 [4] 等。
床旁肺部超声(Lung Ultrasonography, LUS)是一种超声诊断肺部疾病技术。关于肺脏超声的首次描述可以追溯到上世纪60年代 [5],关于肺超声的基本体征在30年前得到了系统的描述 [6] [7] [8] [9]。但是由于肺泡内充满气体,超声波遇到气体时会发生全反射,因此超声技术在肺部检查时一直得不到广泛应用,几年来随着技术的发展,这一技术瓶颈逐渐被打破,过去需要依赖胸部X射线、CT检查的多种疾病,现在均可借助超声检查做出明确诊断,且具有更高的特异性、准确性。且超声本身的无放射性,床旁肺部超声技术近十多年来得到飞速发展与广泛应用。
近几年,机器学习技术得到迅速发展,其中的深度学习更是已成为热门研究领域,在图像处理、自然语言处理、机器翻译等方向已取得了很多成果。在医学方面,计算机辅助诊断也已经成为研究热点,其主要特点是提高人为诊断的工作效率与准确率。尽管基于机器学习的计算机辅助诊断技术实现了医学影像的分类,但这些医学影像需要人工提取特征再发送给分类器。而深度学习可以通过卷积神经网络自动提取特征,避免了人工提取特征这一过程,大幅度提升了工作效率。
本文实验先对医院采集的新生儿肺部超声图像进行预处理,再对Vision Transformer进行微调并将预处理的数据集输入至网络中,实现对新生儿肺部超声图像进行自动分类,分类结果为两组,为病情类(阳性)与健康类(阴性),可辅助医生诊断新生儿是否需要治疗。本文第二部分主要是对实验相关工作进行阐述,包括采样过程、数据集来源等。本文第三部分阐述模型结构;第四部分描述实验具体内容与步骤;第五部分为总结,其中包括实验的结果,不足点以及对未来的展望。
2. 关于数据集
本文实验选取了2020年在上海市第一妇婴保健院出生的30名新生儿,日龄0~3天,胎龄27~40周。本次实验通过上海市第一妇婴保健院认可,且获得受试者监护人书面同意。
新生儿肺部疾病主要有:新生儿呼吸窘迫综合征(neonatal respiratory distress syndrome, NRDS)、新生儿暂时性呼吸增快症(transient tachypnea of the newborn, TTN)、胎粪吸入综合征(meconium aspiration syndrome, MAS)。NRDS是指由于各种原因引起肺泡表面活性物质(pulmonary surfactant, PS)原发或继发行缺乏,出现肺不张,导致新生儿出身不久后出现以进行性呼吸困难、青紫和呼吸衰竭为主要临床表现的严重肺部疾病,该病情主要见于早产儿。TTN又称新生儿湿肺(wet lung of the newborn),主要高危因素有:剖宫产分娩、出生体重大、母亲糖尿病等,患儿主要表现症状为呼吸困难,患儿出生时大作正常或有窒息史,数小时(2~5 h)后出现呼吸困难,轻者表现为呼吸增快,重者表现为严重呼吸窘迫、吐沫、反应差。MAS是因胎儿在宫内或产时吸入被胎粪污染的羊水而导致新生儿出生后出现以呼吸窘迫为主要临床表现的综合征,主要表现为在出生数小时内出现呼吸困难,且患儿皮肤、指甲、脐带等部位严重黄染。该病情常见于足月儿或过期产儿。总之,当新生儿在出生几小时内出现呼吸困难时,需要及时对其进行肺部超声检查。
医生使用的超声诊断仪是GE LOGIC P5,相应的探头为高频线阵探头 ,频率为10 MHz~12 MHz。新生儿处于安静状态下,取仰卧位与侧卧位,以腋前线、腋后线为基准,将左右双肺各分为前、侧、后3个区域,并将每个区域分为上下两部分,总共12个区域。并根据从上而下,先右后左,从前到后的顺序依次一次扫查各个区域且储存规划范的图像。
对于新生儿肺部超声图像,主要观察指标有胸膜线、A线与B线 [10]。胸膜线:胸膜与肺表面的界面回声所形成的回声反射,在正常情况下,胸膜线光滑且厚度不超过0.5 mm,当胸膜线变粗糙、增厚或消失等,为异常。A线:是胸膜下一系列间距相等且与胸膜线平行的线性高回声。B线:是起源于胸膜线的线性高回声,且垂直于胸膜线并呈放射状向肺野深部发散。
正常情况下,新生儿肺组织在超声下呈黑色低回声,胸膜线呈现高回声,光滑且清晰可见;A线与胸膜线等间距平行排列,呈现清晰、光滑且规则的线性高回声,随着肺野深度增加回声强度逐渐降低;同时没有B线或者仅有少数几条B线。如图1中(a)图所示。当新生儿有明显呼吸困难时,显示的超声图像往往是胸膜线及A线模糊或消失,B线清晰可见,如图1(b)~(d)所示,其中,(b)图为患有NDRS的新生儿肺部超声图,(c)图为患有TTN的新生儿肺部超声图像,(d)图为患有MAS的新生儿肺部超声图像。下图2为超声下NRDS的恢复过程,该新生儿在出生体重仅1980 g,因会呼吸困难出生3 h后入院,此时肺部超声图像显示为图A,胸膜线异常且A线消失,经过一定的治疗之后,患儿情况有所好转,肺部超声图像为图C,胸膜线恢复正常,部分A线出现。
3. 模型结构
Transformer在自然语言处理(Natural Language Processing, NLP)领域已取得了较大的成功。Vison Transformer (ViT)就是将Transformer在NLP领域的思想与架构运用至图像分类任务上。Alexey等人 [11] 利用ViT网络先将一张图片分成多个小块的patches,再进行分类操作。本文没有将输入图像划分成若干个小块,而是使通过使用卷积以及一些其他处理,再输入至Transformer网络,用于对新生儿肺部超声图像进行分类。模型结构如图3所示。
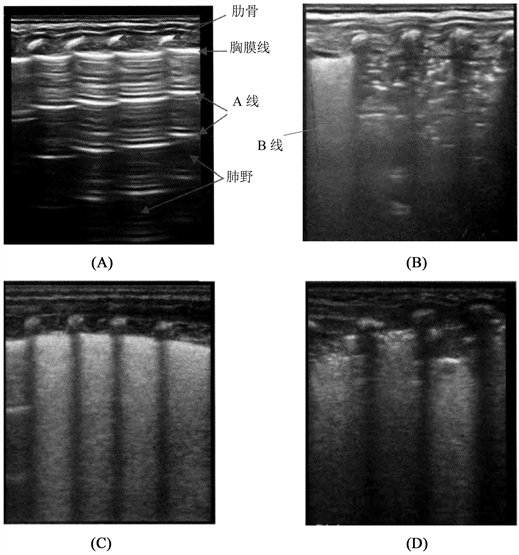
Figure 1. The images of neonatal lung ultrasound
图1. 新生儿肺脏超声声像图表现
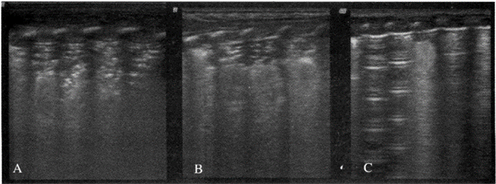
Figure 2. The recovery process of NRDS under ultrasound
图2. 超声下NDRS恢复过程
本实验模型输入的图像的数据格式为[224, 224, 3]的三维矩阵,但是Transformer模型要求输入的是二维矩阵[num_token, token_dim]。首先使用卷积核大小为16 × 16,步距为16,卷积核个数为768的卷积将图像的数据格式从[224, 224, 3]变为[14, 14, 768],接着进行展平处理,把图像的宽与高两个维度展平,得到的数据格式为[196, 768],便能得到Transformer所需要的二维矩阵。同时,在第一维度拼接一个长度为768的分类向量class token,其数据格式为[1, 768]。由于所有的token相互之间都在做信息交互,因此分类向量classtoken可以从另外的196个token中学习到有用的信息,最后只需根据classtoken的输出做出最后的分类判断便能得到最终分类结果,拼接后得到的矩阵大小为[197, 768],即得到197个token,每个token向量维度为768。为了保持输入图像的空间位置信息,需要添加位置编码向量,此模型参考Devlin等人 [12] 的类标记,使用标准的可学习1D位置编码,其数据格式也为[197, 768],其中分类向量classtoken的位置编码为0。
在Transformer Encoder中,堆叠Encoder Block 12次。主要由Layer Norm、Multi-Head Attention、MLP Block组成。其结构图如图4所示。Layer Norm用于对输入的数据归一化,可提升训练的稳定性。Multi-Head Attention (多头注意力机制) [13] 是基于自注意力机制(Self-Attention),Self-Attention是注意力机制中的一特例。Self-Attention公式如下式(1),式(2)所示:
(1)
(2)
式(1)中,输入矩阵
通过矩阵乘法线性映射到注意力空间矩阵
(查询矩阵),
(键矩阵),
(值矩阵),
、
、
为可学习的超参数矩阵。式(2)中
表示键的维度,
表示缩放因子,用来防止
与
的乘积过大。最终得到基于查询和键的相似度与值得加权和。
Multi-Head Attention是将
、
、
映射到不相同得子空间上,每个子空间独立进行Self-Attention计算,最后将子空间的各个输出拼接在一起,最终得到多头注意力机制的结果。公式如下式(3)、式(4)所示。
(3)
(4)
式中
、
、
是可学习的超参数矩阵,
是为了将多头注意力进一步融合,保证输入输出mtlti-head attention的向量长度保持不变,用一个输入输出大小全为768的全连接层实现。
MLP Block由全连接层、GELU激活函数、Dropout组成。其结构如图5所示,其中输入至第一个全连接层后,二维矩阵中token_dim的值变成原来的4倍,即矩阵[197, 3072],经过第二个全连接层之后,数据格式还原为原来的[197, 768]。其公式为式(5)、式(6)。
(5)
(6)
式中MSA表示多头注意力操作,
表示Layer Norm,
表示MLPBlock层对应的操作,
是多头注意力的结果,
表示每次Transformer Block的输出。
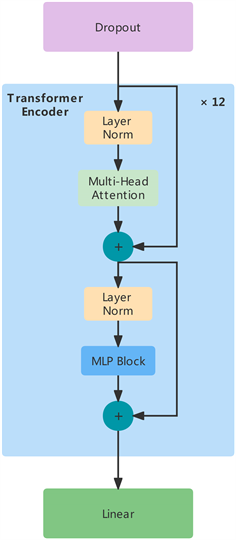
Figure 4. The structure of the Transformer Encoder
图4. Transformer Encoder结构图
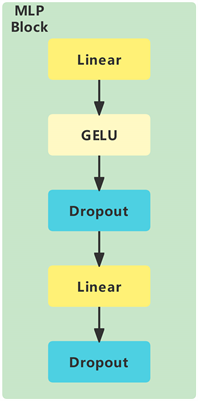
Figure 5. The structure of MLP Block
图5. MLP Block结构图
对于Transformer Encoder输出的数据,取位置编码维度中索引为0的分类向量classtoken,输入至全连接层,实现对新生儿肺部超声图像的分类,最终得到诊断结果。公式如下式(7)所示。
(7)
式中
即为分类向量class token所对应的输出。
4. 实验步骤
4.1. 数据预处理
在超声诊断仪采集到的图像存在诸多与模型训练无关的干扰信息,因此需要在不丢失图像关键信息的基础上对原始图像进行手动降维。原始图像大小为816 × 614像素,保留原始图像中的信息,使用Matlab中的imcrop函数,将图像的剪切成500 × 500,再通过imresize函数,将图像等比例缩小至224 × 224像素。原始图像如图6所示,预处理后图像如图7所示。

Figure 6. The original image captured by ultrasonography
图6. 超声诊断仪采集的原始图像

Figure 7. The image after pre-processing
图7. 数据预处理后的图像
4.2. 模型训练
本次实验数据集总共600张新生儿肺部超声图,包括300张正常的超声图像和300张有病的超声图像。在300张正常超声图像中,270张图用作训练与验证,30张图用作测试集;300张有病的超声图像中,270张图用作训练与验证,剩余30张图用作测试集。同时,在540张用于训练的图像中,按8:2的比例划分训练集与验证集。在完成数据集的预处理之后,基于Pytorch环境,使用的显卡是NVIDIA GTX 3090。学习率设置为0.01,每次输入模型100张数据集、即BATCH_SIZE设为100,STEP设为600,使用VIT网络在IamgeNet-21K上预训练的权重,对模型进行训练。本文共进行了5次实验,5次实验独立进行,每次实验前重新随机划分训练集与测试集。
4.3. 评价指标
为了验证模型对新生儿肺部超声图像的分类效果,采取四种不相同的指标对模型进行评估 [14] [15] [16]:正确率(Accuracy, Acc)、精确度(Pression, Pre)、敏感性(Sensitivity, Sen)、特异性(Specificity, Spe)。Acc公式如下式子(8)所示,是指正确识别数据集的数目在数据集总数的占比;Pre公式如下式子(9)所示,是指正确识别阳性数据集数目在所有被认定为阳性数据集的占比。Sen公式如下式子(10)所示,是指在所有阳性数据集中被正确判别出来的比率;Spe公式如下式子(11)所示,是指在所有阴性数据集中被正确识别出来的比率。
(8)
(9)
(10)
(11)
其中,TP (True Positive)是指将阳性样本正确分类的个数;TN (True Negative)是指将阴性样本正确分类的个数;FP (False Positive)是指将阴性样本错误分类的个数,FN (False Negative)是指将阳性样本错误分类的个数。其混淆矩阵图如图8所示。
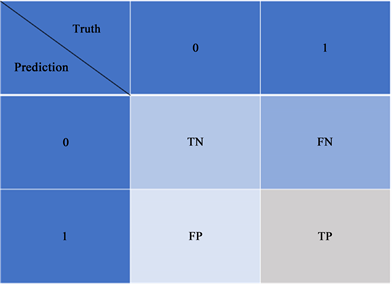
Figure 8. The confusion matrix of indicators
图8. 评估指标的混淆矩阵
另外,受试者工作特征曲线(Receiver Operating Characteristic Cruve, ROC)反映着敏感性与特异性连续变量的综合指标,在一定程度上可以显示出分类器的分类效果;AUC表示ROC曲线下的面积,可以更加直观地反映出分类效果。
4.4. 实验结果
在这5次的模型训练中,训练集的平均准确率acc为0.935,平均损失函数loss为0.210,验证集的平均准确率为0.893,平均loss为0.279。对于测试集,每组有60张图片,其结果如下表1所示。Acc、Pre、Sen、Spc四类模型评估指标如下表2所示。同时,在表3中,我们还对本次实验提出的模型与目前一些主流分类模型做比较,有残差网络ResNet,基于逐点分组卷积的轻量级神经网络ShuffleNet以及基于深度可分离卷积的轻量级神经网络MobileNet-V2,来验证本次模型的实验效果。

Table 1. The results of five experiments
表1. 5次实验测试集测试结果

Table 2. The four different indexes of five experiments
表2. 5次实验评估指标

Table 3. Comparison with other classification models
表3. 与其他模型对比
从表2中可以看出,经过5次实验,平均准确率Acc已达到了95.68%,敏感性Sen、精确度Pre、特异性Spc均达90%以上。表3中,选取了其他几个模型效果最好时的评估指标值,可以看出,效果都不如本文的模型。
根据实验结果,绘制出ROC曲线,如图9所示。从图中可以看出,平均AUC达到了99.53%,说明该模型对新生儿肺部超声图像的分类效果较好。
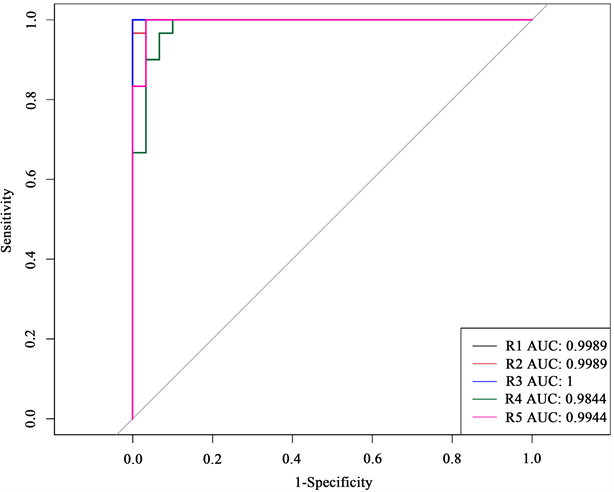
Figure 9. ROC curve of five experiments
图9. 五次实验的ROC曲线
5. 总结
实验结果表明,相对于传统的诊断方法,本文提出的一种卷积与ViT相结合的模型可以实现对新生儿肺部超声图像的特征提取及分类,并且分类效果较好。本文分类模型能够辅助医生诊断新生儿是否需要进一步的诊断,提高主治医师的工作效率,减轻工作负担,同时能够减轻新生儿父母的心理负担。但还存在着一些不足之处,本次实验数据集的样本较少,实验的结果容易出现过拟合。同时,需要对模型结构进一步优化与完善。实验结果如何与医生的临床诊断相结合,也需要不断地探索与研究。
基金项目
国家自然科学基金81101116。
NOTES
*第一作者。
#通讯作者。