摘要: 目的:探讨优替德隆治疗晚期乳腺恶性肿瘤病人的临床疗效。方法:选取2021年5月至2022年12月就诊于新疆医科大学附属肿瘤医院晚期乳腺癌患者。其中生存分析采用Kaplan-Meier法和Log rank检验,多因素采用Cox回归模型分析。结果:1) 28例患者,5例为部分缓解,16例为疾病稳定,7例为疾病进展,无1例患者达到完全缓解,客观缓解率17.9% (5/28),疾病控制率75% (21/28)。2) 在接受优替德隆的晚期乳腺癌病人中,mPFS为3个月,最高PFS为10个月,中位OS未达到,平均OS为13.4个月。3) 三阴性、Lunminal型、HER-2过表达型乳腺癌的中位PFS分别为4、3和2个月,优替德隆治疗三组患者的疗效无差别(p > 0.05)。结论:优替德隆治疗各种分子亚型的晚期乳腺癌的疗效无差别。优替德隆对于多线化疗失败后的晚期乳腺肿瘤患者具有较好的治疗效果,其具有较好的临床应用价值。
Abstract:
Objective: To explore the clinical efficacy of Utidelone in the treatment of advanced breast cancer patients. Methods: The patients with advanced breast cancer who visited Xinjiang Medical Univer-sity Cancer Hospital from May 2021 to December 2022 were selected. Survival analysis was con-ducted using Kaplan Meier method and Log rank test, while multivariate analysis was conducted using Cox regression model. Result: 1) Of the 28 patients, 5 showed partial response, 16 showed stable disease, 7 showed disease progression, and no patient achieved complete response. The ob-jective response rate was 17.9% (5/28), and the disease control rate was 75% (21/28). 2) Among patients with advanced breast cancer who received Utidelone, the mPFS was 3 months, the highest PFS was 10 months, and the median OS was not achieved, with an average OS of 13.4 months. 3) The median PFS of triple negative, Lunminal, HER-2 overexpression breast cancer was 4, 3, and 2 months, respectively. There was no difference in the efficacy of the three groups of patients treated with Utidelone (p > 0.05). Conclusion: There is no difference in the efficacy of Utidelone in the treatment of various molecular subtypes of advanced breast cancer. Utidelone has a good therapeu-tic effect in patients with advanced breast tumours after failure of multiple lines of chemotherapy, and its clinical application is of good value.
1. 引言
世界卫生组织国际癌症研究机构(International Agency for Research on Cancer, IARC)发布了2020年全球最新癌症数据,女性乳腺癌现已超过肺癌,成为2020年全球癌症发病首位,它是全球癌症死亡的第五大原因 [1] 。针对晚期复发的乳腺癌,紫杉类药物是乳腺癌化疗的基础用药。然而紫杉醇广泛应用于临床导致肿瘤细胞对P-糖蛋白表达型多药耐药性的出现(MDR)使紫杉醇的治疗和应用受到一定程度的限制 [2] 。
优替德隆(Utidelone, UTD1)是由生物合成的埃博霉素基因簇的遗传操作产生的埃博霉素衍生物。优替德隆主要的作用机制与紫杉类药物类似,优替德隆在G2/M阻滞后通过激活caspase-3和PARP诱导细胞凋亡,其效果优于紫杉醇 [3] 。优替德隆具有更高的亲和性,且具有更好的抗癌活性,而针对其靶基因的变化和抗药性机理,优替德隆则不会受到干扰 [4] 。优替德隆的临床研究应用尚且不足,因此探讨优替德隆治疗晚期乳腺癌的疗效。
2. 资料与方法
2.1. 临床资料
选举2021年5月至2022年12月就诊于新疆医科大学附属肿瘤医院的28例晚期乳腺癌患者。入组标准:① 经组织学或细胞学证实为乳腺癌的患者,且为不可切除的转移性疾病者。② 患者年龄在18~75周岁的男性或女性。③ 之前所有的化疗或放疗相关的毒性反应都已缓解,达到1级或更低的严重程度,但稳定的≤2级脱发、色素沉着除外。④ 东部合作肿瘤学组(ECOG)表现状态为0~2分。⑤ 预期寿命在3个月以上。⑥ 入组前一周血常规检查大体正常(以每个研究中心化验室正常情况为准)。白细胞计数(WBC) ≥ 3.5 × 109/L;中性粒细胞计数(ANC) ≥ 1.5 × 109/L;血小板计数(PLT) ≥ 100 × 109/L;血红蛋白(HB) ≥ 90 g/L。病人可以通过输血或者促红细胞生成素的治疗来满足此标准。⑦ 入组前1周之内肝肾功能检查基本正常。总胆红素(TBIL) ≤ 1.5 × 正常值上限(ULN);谷丙转氨酶(SGPT/ALT) ≤ 2.5 × ULN (肝转移患者≤5 × ULN);谷草转氨酶(SGOT/AST) ≤ 2.5 × ULN (肝转移患者≤5 × ULN);肌酐清除率(Ccr) ≥ 60 ml/min。排除标准:① 排除临床资料不全的病人;② 排除已被确诊为双原发性癌症的病人;③ 排除预期生存期不超过3个月患者;④ 排除优替德隆药物过敏的病人;⑤ 排除患有不易控制的精神病患者。
2.2. 治疗方法
患者给予优替德隆治疗,优替德隆使用方法为50 mg d1-d5,21 d为1周期。优替德隆治疗:其中接受优替德隆单药治疗1例,优替德隆联合替吉奥治疗7例、卡培他滨治疗6例、安罗替尼治疗3例、阿帕替尼及卡培他滨治疗1例、多柔比星及卡培他滨治疗1例、安罗替尼及卡培他滨治疗2例、安罗替尼及替吉奥治疗2例、卡瑞丽珠单抗及替吉奥治疗1例、吡咯替尼 + 卡培他滨2例、吡咯替尼 + 安罗替尼2例。在基线和之后每2周收集血液样本。每2周期治疗后进行复查评估,患者评估包括体格检查,血液检测生及化检测评估其病情治疗相关不良反应,计算机断层扫描或磁共振成像评估原发灶及转移灶,以及肿瘤标志物评估治疗疗效,直至病情进展或患者不可耐受的不良反应。
2.3. 观察指标
2.3.1. 临床疗效评判标准
本研究观察患者无进展生存期(progression-free survival, PFS):定义为从接受优替德隆治疗开始至首次出现PD或患者死亡的时间;完全缓解(complete response, CR):所有靶病灶及非靶病灶消失;部分缓解(partial response, PR):靶病灶最大单径之和减少>30%且非靶病灶未进展;疾病稳定(stable disease, SD):肿瘤最大单径之和减少≤30%或增加≤20%;疾病进展(progressive disease, PD):肿瘤最大单径之和增加>20%或者出现新病灶;客观缓解率(objective response rate, ORR) = (CR+PR)/总例数 × 100%;疾病控制率(disease control rate, DCR) = (CR+PR+SD)/总例数 × 100%。
2.3.2. 患者随访
患者的随访是从接受优替德隆开始,通过查阅病人的门诊复查、入院病例或打电话询问等方法,并且做到认真完整记录随访的结果。本研究随访初始时间是:第一次应用优替德隆治疗的时间;随访结束时间是:确定该患者在接受优替德隆过程中出现疾病进展或死亡,不可接受的毒性或应患者或研究者的要求停止治疗,允许减少剂量以控制毒性作用。随访的电话内容包括:治疗效果、治疗后复查结果、疾病进展时间、药物不良反应。若患者死亡或失访,随访时间则从初次服药之日起至最后一次随访时间。失访定义为通过电话及门诊随访均联系不到患者及家属,三次以上视为失访。
2.4. 统计学方法
采用SPSS 26.0软件进行统计学分析。定性资料采用例数(%)表示,计数资料采用卡方检验或Fisher’s精确检验;PFS采用Kaplan-Meier法和Log rank检验进行评估,影响因素采用Cox比例风险回归模型,双侧检验水准α = 0.05。
3. 结果
3.1. 治疗疗效
在本研究中,全组患者优替德隆治疗周期为2~8个,中位治疗周期为3个。28例患者中,PR 6例,SD 15例,PD 7例,ORR为21.4%,DCR为75%。
1) 不同分子亚型乳腺恶性肿瘤患者的疗效:HER-2过表达乳腺恶性肿瘤患者5例,其中PR患者0例,SD患者2例,PD患者3例,ORR为0%;DCR为40.0%;Luminal型乳腺恶性肿瘤患者9例,PR患者2例,SD患者5例,PD患者2例,ORR为22.22%,DCR为77.8%;三阴性乳腺恶性肿瘤患者14例,PR患者4例,SD患者9例,PD患者1例,ORR为28.6%,DCR为92.9%。不同分子亚型的乳腺癌患者在治疗疗效上没有统计学上的显著差异(p = 0.223,表1)。
2) 不同治疗线数乳腺恶性肿瘤患者的疗效:优替德隆为治疗小于等于三线的肿瘤患者11例,PR患者3例,SD患者8例,PD患者0例,ORR为27.3%;DCR为100%;治疗大于等于四线的肿瘤患者17例,PR患者3例,SD患者8例,PD患者6例,ORR为17.6%;DCR为64.7%;优替德隆不同治疗线数的乳腺癌患者在治疗疗效上没有统计学上的显著差异(p = 0.172,表1)。
3) 不同年龄治疗乳腺恶性肿瘤患者的疗效:<50岁肿瘤患者15例,PR患者4例,SD患者8例,PD患者3例,ORR为26.7%;DCR为80.0%;≥50岁的肿瘤患者13例,PR患者2例,SD患者8例,PD患者3例,ORR为15.4%;DCR为76.9%;不同年龄段的乳腺癌患者的结果没有统计学上的显著差异(p = 0.878,表1)。

Table 1. Evaluation of the efficacy of UTD1 in the treatment of 28 patients with advanced breast cancer
表1. 优替德隆治疗28例晚期乳腺癌患者疗效评价
3.2. 生存情况
全组患者中位PFS为3个月(图1),PFS最长为10个月,中位OS未达到,平均OS为13.4个月402天[95%CI 10.76~16.13],约为13.4个月(图2)。三阴性、Lunminal型、HER-2过表达型乳腺癌的中位PFS分别为4、3和2个月(p = 0.789;表2,图3)。


Table 2. Analysis of factors influencing the prognosis of patients with advanced breast cancer
表2. 晚期乳腺癌患者预后的影响因素分析
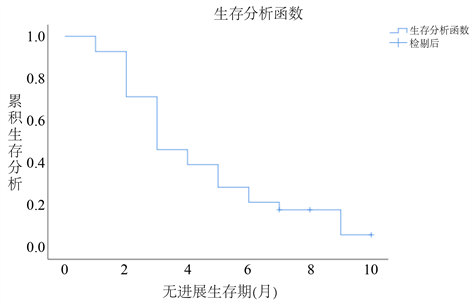
Figure 1. PFS curve of 28 patients with advanced breast cancer treated with UTD1
图1. 28例晚期乳腺癌病人应用优替德隆治疗的无进展生存曲线
4. 讨论
基于BG01-1323L(NCT 02253459) [5] 一项多中心、随机、开放标签的Ⅲ期临床研究,表明优替德隆在乳腺恶性肿瘤治疗中能兼顾其疗效及安全性的优势。优替德隆联合卡培他滨与卡培他滨单独治疗相比,根据2020年公布的最新数据显示,联合治疗组相对单药治疗组PFS延长[HR = 0.47, 95%CI (0.37, 0.59),p < 0.00011],中位PFS分别为8.4个月[95%CI (7.89, 9.49)]和4.1个月[95%CI (3.09, 5.09)];OS也获得延长[HR = 0.75, 95%CI (0.59, 0.94), p = 0.0142],中位OS分别为19.8个月[95%CI (17.02, 21.59)]和16.0个月[95%CI (14.26, 18.53)];ORR分别为45.6%和23.7% (p < 0.001) [6] 。
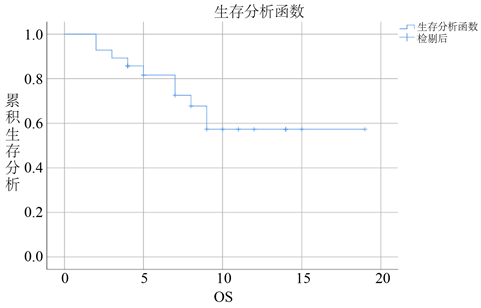
Figure 2. Overall survival curve of 28 patients with advanced breast cancer treated with UTD1
图2. 28例晚期乳腺癌病人应用优替德隆治疗的总体生存曲线
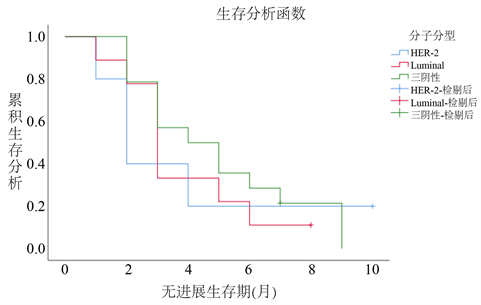
Figure 3. PFS curves of 28 patients with different molecular subtypes of advanced breast cancer treated with UTD1
图3. 28例不同分子亚型晚期乳腺癌病人应用优替德隆治疗的无进展生存曲线
但在中国应用优替德隆治疗乳腺癌的经验仍然较少,因此我们收集了28例患者进行分析,研究结果显示,≤3线与≥4线的患者其中ORR分别为27.3%与17.6%,结果显示更早阶段选择优替德隆治疗有更优的趋势。六线以上使用优替德隆患者占比28.6% (8/28),ORR及DCR分别25%与75%,提示对多线化疗失败的晚期患者,优替德隆仍有较好的疗效。优替德隆在治疗不同分子亚型的乳腺癌患者的临床疗效并无差异(p = 0.223;表1),此外,本研究ORR略低于文献报道数据,这可能与本研究是单中心研究,因此样本数少于之前的试验,而且患者基线情况比较复杂相关。
在本研究中,28例患者中位PFS为3个月,PFS最长为10个月,中位OS未达到,平均OS为13.4个月402天[95%CI 10.76~16.13]。其中三阴性、Lunminal型、HER-2过表达型乳腺癌的中位PFS分别为4、3和2个月,由于样本量较少,随访时间较短,中位PFS并无统计学意义(p = 0.789;表2)。采用Kaplan-Meier生存曲线进行分析,采用log-rank检验比较组间差异,单因素分析结果显示,Ki67%指数和疗效评价与患者预后有关(p < 0.05;表2),其年龄、分子亚型以及治疗线中位PFS并无统计学意义。Cox多因素回归分析结果表明,影响患者预后的独立影响因素是疗效评价(p < 0.05;表3)。

Table 3. Results of Cox multiple regression analysis of factors influencing prognosis in advanced breast cancer
表3. 晚期乳腺癌预后影响因素的Cox多因素回归分析结果
5. 本研究局限性
这项研究也有一些不足之处。第一,研究的患者数量较少,存在一定的偏倚;第二,由于大多数的患者都有长期的综合性的治疗经历,难以实行同期同质对照组。第三,该研究未考察药物组合对患者存活时间的影响,不能正确评价药物组合的效果,后期应设置优替德隆与不同化疗方案、靶向治疗和免疫治疗相结合的研究,以便更好地指导临床实践。
6. 总结
综上所述,本研究结果表明,优替德隆在治疗晚期乳腺癌方面仍有临床疗效,并有良好的生存获益,优替德隆治疗各种分子亚型的晚期乳腺癌的疗效无差别。优替德隆对于多线化疗失败后的晚期乳腺肿瘤患者具有明显的治疗效果。
声明
该病例报道已获得病人的知情同意。
NOTES
*通讯作者。