1. 引言
炭疽病是由炭疽芽孢杆菌引起的一种人畜共患的急性传染病,由于其高传染性、高致病率、高死亡率,严重威胁着人类生存以及畜牧业的健康发展 [1] [2] 。炭疽杆菌芽孢对环境具有极强耐受性,能在高温、紫外线照射、冷冻、干燥和化学消毒等恶劣环境中存活,即使炭疽杆菌被杀死,其芽孢仍然可以在合适的条件下发芽 [3] [4] 。人体一般可通过进食、呼吸道或皮肤接触感染疾病,当吸入孢子数量超过104个,24~48 h内不采取医药治疗,可以导致死亡 [5] 。因此,实现对炭疽杆菌芽孢及其浓度的简便、快速以及准确检测对于维护公共安全具有重要意义。2,6-吡啶二羧酸(DPA)是炭疽杆菌芽孢中的主要组分,其质量占据芽孢干重的5%~15%。目前DPA已被确认为鉴定炭疽病和识别炭疽杆菌的唯一生物标志物,通过检测DPA可以对炭疽杆菌芽孢浓度进行评估 [6] [7] 。
目前已发展了多种方法用于DPA的检测,例如表面增强拉曼光谱、高效液相色谱法和液质联用法,但这类检测仪器体积较大、检测周期较长、仪器造价昂贵,且无法满足现场快速检测需求 [8] [9] [10] 。后来逐渐发展的电化学检测、免疫分析法和荧光分析技术具有操作简单、灵敏度高和检测准确等优点 [11] 。而荧光传感检测技术以其检测快速、简便、可视化等特点为原位灵敏选择性检测DPA提供了理论基础。因此,建立可实现灵敏选择性检测DPA的荧光检测方法具有重要意义。然而,荧光探针的光稳定性以及复杂构建过程将极大限制其推广应用。基于镧系发光的光学探针由于具有长荧光寿命、较大的Stokes位移、光稳定性以及高发射光纯度等特点在传感分析、生物成像以及光电器件等领域广泛应用,因而建立基于镧系元素发光的新型荧光探针将极大的解决上述问题 [12] [13] 。其中,相比于单发射探针,比率荧光探针可以通过自校准减小或排除背景荧光、仪器误差以及外界环境因素造成的干扰,进而实现对目标物的灵敏和准确检测。此外,双发射峰的相对变化可以引起探针显著地荧光颜色改变,有利于实现对目标物的裸眼可视化以及原位检测,显著提高样品检测效率,并降低检测成本 [14] [15] [16] 。
本论文工作拟构建基于磷酸根(Pi)调控的鲁米诺(Luminol)-Tb荧光配合物(Luminol-Tb-Pi)用于炭疽杆菌生物标志物(2,6-吡啶二羧酸,DPA)的快速、灵敏以及可视化检测。如方案1所示,以Luminol为有机配体,Tb3+为金属中心体,在Pi的调控下,DPA的加入可以使Tb3+特征荧光显著增强,同时引起Luminol荧光淬灭。DPA通过与Tb3+配位结合,向Tb3+进行能量转移敏化其发光;Pi通过缩小DPA与Tb3+之间的距离,增强DPA的敏化作用;此外,Pi通过与Tb3+的配位还可以减少水分子对Tb3+的荧光淬灭作用,进一步增强Tb3+荧光。由于DPA与Tb3+的竞争性结合,使Luminol与Tb3+的配位作用减弱,部分Luminol释放成游离态,其聚集诱导的荧光增强状态破坏,导致其荧光淬灭。因此,基于Tb3+特征荧光增强和Luminol荧光淬灭的双信号变化,可实现对DPA的比率检测,且具有很好的特异性和抗干扰性。此外,随着DPA浓度的增加,该传感体系荧光逐渐由蓝色变为绿色,可实现对DPA的可视化检测。
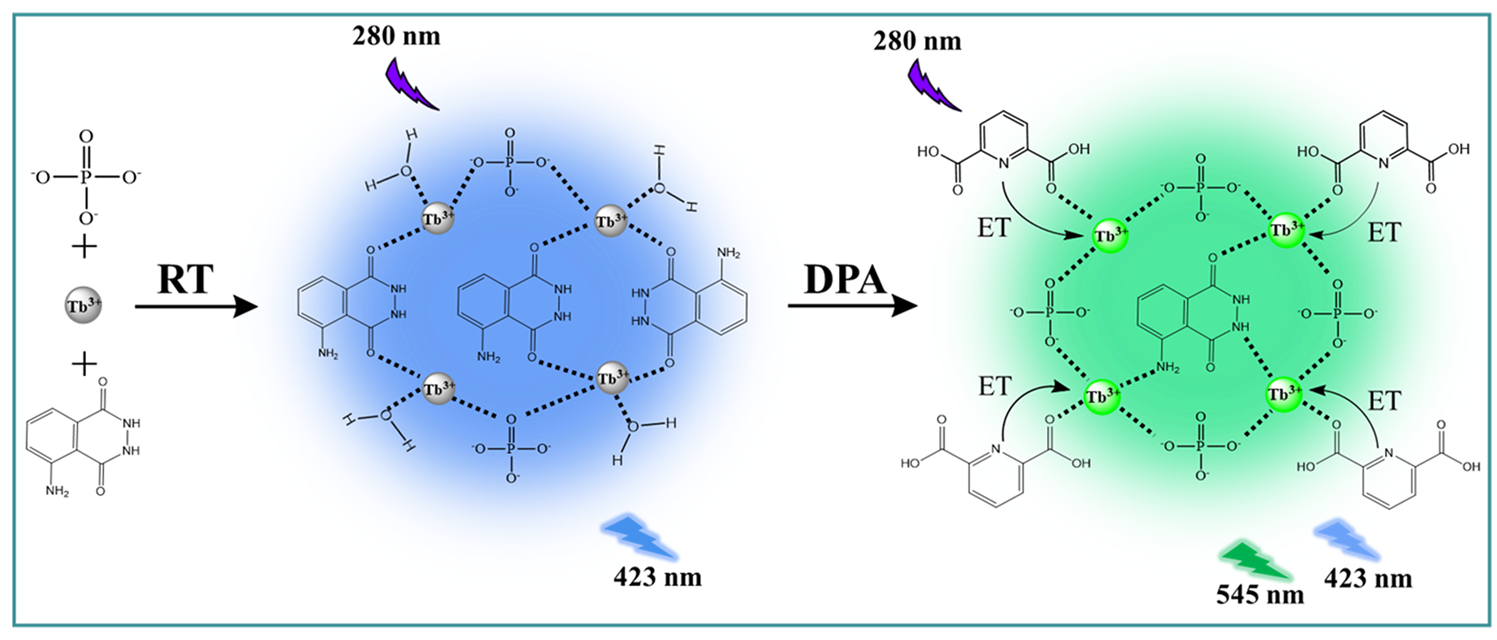
Scheme 1. Schematic illustration of the strategy for the detection of DPA based on Pi modulated Luminol-Tb fluorescent probe
方案1. 基于Pi调控的Luminol-Tb荧光探针用于DPA检测
2. 实验部分
2.1. 实验试剂与仪器
实验中使用的所有试剂至少是分析纯度。鲁米诺(Luminol)、六水合硝酸铽(Tb(NO3)3∙6H2O)、2,6-吡啶二羧酸(DPA),和磷酸钠(Na3PO4)购自上海阿拉丁化学有限公司。L-亮氨酸(L-leucine)、L-谷氨酸(L-glutamic acid)、L-半胱氨酸(L-cysteine)、D-丙氨酸(D-alanine)、鸟苷一磷酸(GMP)、腺苷一磷酸(AMP)、牛血清白蛋白(BSA)、葡萄糖(glucose)、柠檬酸(citric acid)、尿酸(uric acid)、烟酸(nicotinic acid)、土霉素(oxytetracycline)、氢氧化钠和三羟甲基氨基甲烷(Tris)购自国药集团化学试剂有限公司。其他的无机金属盐类药品均为分析纯,购自国药集团化学试剂有限公司。实验中使用的去离子水(18.25 MΩ∙cm)由UPK/UPT净水系统制备。
样品的荧光光谱由F-7000荧光光谱仪(日立,日本)进行测定,激发光源为氙灯,激发和发射狭缝均为5 nm,激发波长为280 nm,光电倍增管电压为400 V。所有pH测量均在FE28标准pH计(Mettler Toledo, Switzerland)上进行。
2.2. 荧光传感构建及对DPA的检测
在5.0 mL的比色管中,依次加入一定量的如下溶液:500 μL的Tris-HCl缓冲溶液(1.0 mol∙L−1, pH = 7.5)、160 μL的Luminol溶液(1.0 mol∙L−1)、30 μL的Tb3+溶液(5 mol∙L−1)和100 μL的Pi溶液(10.0 mol∙L−1),构筑Luminol-Tb-Pi配合物荧光探针。
向探针中DPA标准溶液(0.2~45 μM)或预处理样品,最后用去离子水定容至10.0 mL。样品混合均匀后在室温下放置20 min,最后使用荧光光谱仪在激发波长为280 nm,激发狭缝和发射狭缝为5 nm条件下,依次测定各样品在300~600 nm内的荧光光谱。以545与423 nm处的荧光强度值作为DPA浓度的函数,用于DPA的定量分析。在选择性试验中,用其他可能的干扰物质代替DPA,采用相同的测定方法进行分析检测,探究该荧光探针对DPA的选择性,并探究可能共存物质对DPA检测的干扰性。
2.3. 实际采集与测定
水样采集:水样分别采自当地自来水和湖水。
水样预处理:取采集水样25 mL于50 mL烧杯中,静置2 h后,取上清液。将上清液用0.22 μm滤头过滤,然后稀释100倍备用。
水样测定:向预处理水样中加入一定浓度的DPA (5、10、40 μM),然后将加标样品加入荧光探针中,采用与上述定量分析相同的测定过程,分析样品中DPA含量。
3. 实验结果与讨论
3.1. 荧光探针的构建及对DPA的检测机制

Figure 1. Fluorescence spectra of different systems. Luminol: 50 μM; Tb3+: 50 μM; Pi: 50 μM; DPA: 20 μM; Tris-HCl buffer: 10 mM (pH = 7.5); λex = 280 nm
图1. 不同配合体系的荧光光谱图,Luminol:50 μM;Tb3+:50 μM;Pi:50 μM;DPA:20 μM;Tris-HCl buffer:10 mM (pH = 7.5);λex = 280 nm
如图1所示,在激发波长为280 nm条件下,测定了Luminol-Tb-Pi体系加入DPA前后的荧光光谱变化。在加入DPA之前,Luminol-Tb-Pi体系中只有Luminol的特征荧光;加入DPA后,在489、545和584 nm波长处出现三个荧光峰,分别源于Tb3+的跃迁(5D4→7FJ (J = 6、5、4),表明DPA作为天线配体向Tb3+进行了能量转移,敏化其发光 [17] ;此外,加入DPA后,Luminol荧光出现轻微淬灭。这是由于DPA与Tb3+的竞争性结合,使Luminol与Tb3+的配位作用减弱,部分Luminol释放成游离态,其聚集诱导的荧光增强状态破坏,导致其荧光淬灭 [18] [19] 。
此外,为了说明Pi调控增强的荧光响应,在激发波长为280 nm条件下,同时测定了Luminol-Tb体系加入DPA前后的荧光光谱变化。结果表明,相对于Luminol-Tb体系,Pi调控的Luminol-Tb体系对DPA具有更显著的荧光响应,这是由于Pi的加入使配合物体系配位作用增强,有效缩小DPA与Tb3+之间的距离,增强了DPA的敏化作用 [20] ;此外,Pi通过与Tb3+的配位还可以减少水分子对Tb3+的荧光淬灭作用,进一步增强Tb3+荧光 [21] 。因此,基于Luminol-Tb-Pi探针体系中Luminol和Tb3+的双荧光信号响应,可实现对DPA的比率荧光检测。
3.2. 荧光探针构建及传感条件优化
为构建对DPA具有灵敏性响应的Luminol-Tb-Pi荧光探针,对探针体系中Luminol和Pi的浓度、溶液pH以及该探针对DPA的响应时间等实验条件进行了优化。
3.2.1. Luminol浓度的优化
当Tb3+浓度一定时(50 μM),对Luminol-Tb-Pi体系中Luminol的浓度进行了优化,结果如图2所示。结果表明,当Luminol浓度较低时,虽然DPA对Tb3+荧光的敏化效率较高,但是Luminol荧光信号较弱,易导致实验误差较大,并且体系的荧光颜色变化不明显。随着Luminol浓度的增加,DPA对Tb3+荧光的敏化效率也逐渐降低,因此,综合考虑到探针体系荧光强度和荧光可视化,选择Luminol浓度为50.0 μM用于构建Luminol-Tb-Pi配合物探针。
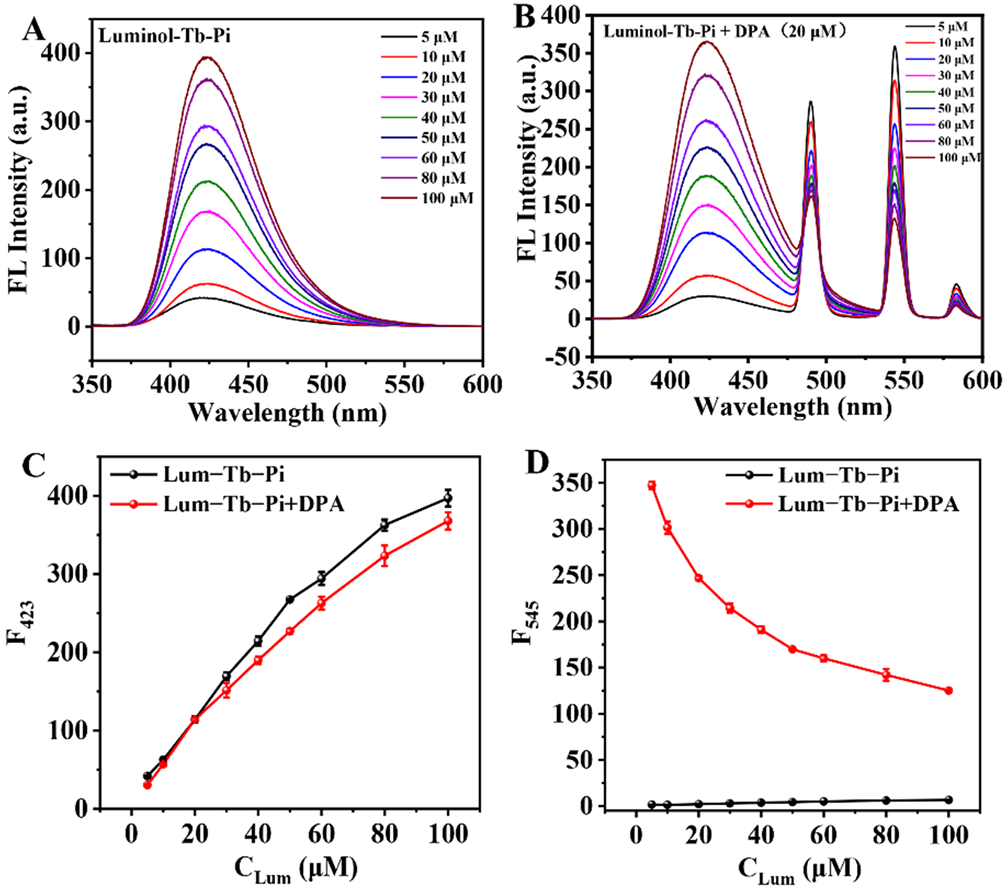
Figure 2. Effect of Luminol concentration (CLum) on fluorescence spectra of Luminol-Tb3+-Pi complex system before (A) and after (B) addition of DPA. Effect of CLum on fluorescence intensity at 423 nm (C) and 545 nm (D) of Luminol-Tb-Pi complex system before and after adding DPA. Pi: 50.0 µM; Tb3+: 50.0 µM; DPA: 20.0 µM; Tris-HCl buffer: 10 mM (pH = 7.5); λex = 280nm
图2. Luminol浓度(CLum)对Luminol-Tb3+-Pi配合物体系加入DPA之前(A)和之后(B)荧光光谱的影响;CLum对Luminol-Tb-Pi配合物体系加入DPA前后在423 nm (C)和545 nm (D)波长处荧光强度的影响;Pi:50 µM;Tb3+:50 µM;DPA:20 µM;Tris-HCl buffer:10 mM (pH = 7.5);λex = 280 nm
3.2.2. Pi浓度的优化
Pi浓度可显著Luminol-Tb-Pi配位物体系对DPA的荧光响应结果,因此本工作探究了在不同的Pi浓度条件下该荧光探针对DPA的响应结果。如图3(A)、图3(B)所示,在加入DPA前后,Pi浓度对Luminol荧光没有明显影响;而在DPA加入后,Pi浓度可显著影响Tb3+特征荧光强度。Pi浓度对Luminol-Tb-Pi体系在423和545 nm波长处荧光强度的影响结果如图3(C)、图3(D)所示。结果表明,随着Pi浓度的增大,DPA对Tb3+的荧光敏化作用逐渐增强,并且当Pi浓度大于50 µM时,DPA对Tb3+的敏化作用趋于稳定,即随着Pi浓度的继续增大,Tb3+特征荧光未出现明显的荧光增强。这是由于随着Pi浓度的增大,Pi与Tb3+的更多配位有效减少了水分子对Tb3+荧光的淬灭作用。因此,选择50 µM的Pi用于构建Luminol-Tb-Pi配合物探针。
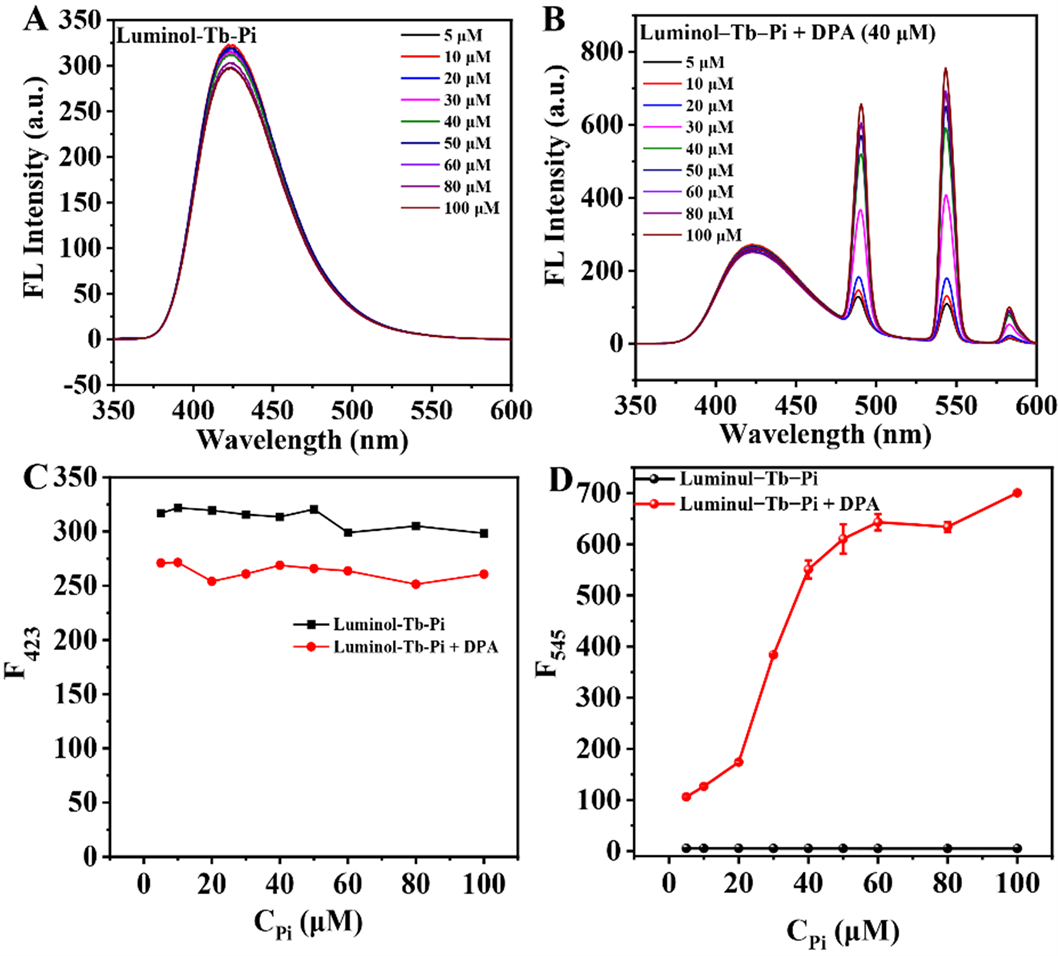
Figure 3. Effect of Pi concentration on fluorescence spectra of Luminol-Tb-Pi complex system before (A) and after (B) addition of DPA. Effect of Pi concentration on fluorescence intensity of Luminol-Tb-Pi complex system at 423 (C) and 545 nm (D) before and after the addition of DPA. Luminol: 50 µM; Tb3+: 50 µM; DPA: 50 µM; Tris-HCl buffer: 10 mM (pH = 7.5); λex = 280 nm
图3. Pi浓度对Luminol-Tb-Pi配合物体系加入DPA之前(A)和之后(B)荧光光谱的影响;Pi浓度对Luminol-Tb-Pi配合物体系加入DPA前后在423 nm (C)和545 nm (D)波长处处荧光强度的影响;Luminol:50 µM;Tb3+:50 µM;DPA:50 µM;Tris-HCl buffer:10 mM (pH = 7.5);λex = 280 nm
3.2.3. pH优化
对于含有酸性或碱性基团的荧光体系,溶液pH值的变化对体系荧光的影响显著。因此,此工作探究了不同pH值(6.0~10.0)对Luminol-Tb-Pi荧光强度的影响。如图4(A)所示,pH对Luminol的荧光强度具有显著明显影响,而在DPA前后,Luminol荧光并未出现明显变化。有趣的是,pH对Tb3+的荧光强度没有显著影响,而向探针体系加入DPA后,Tb3+的荧光强度随着pH值的增大而增强(图4(B))。这是由于在酸性条件下,
易发生水解产生
和
,导致其与Tb3+的配合作用较弱,不能有效增强DPA向Tb3+的能量转移,并且不能有效减少水分子对Tb3+的荧光淬灭作用;而在碱性条件下,
与Tb3+的强烈配位结合通过减少分子间距有效增强了DPA对Tb3+的敏化作用,并有效排除了水分子的淬灭作用。因此,综合考虑溶液pH的影响以及实际样品的酸碱性,选择pH7.5用于Luminol-Tb-Pi探针对DPA的检测分析。
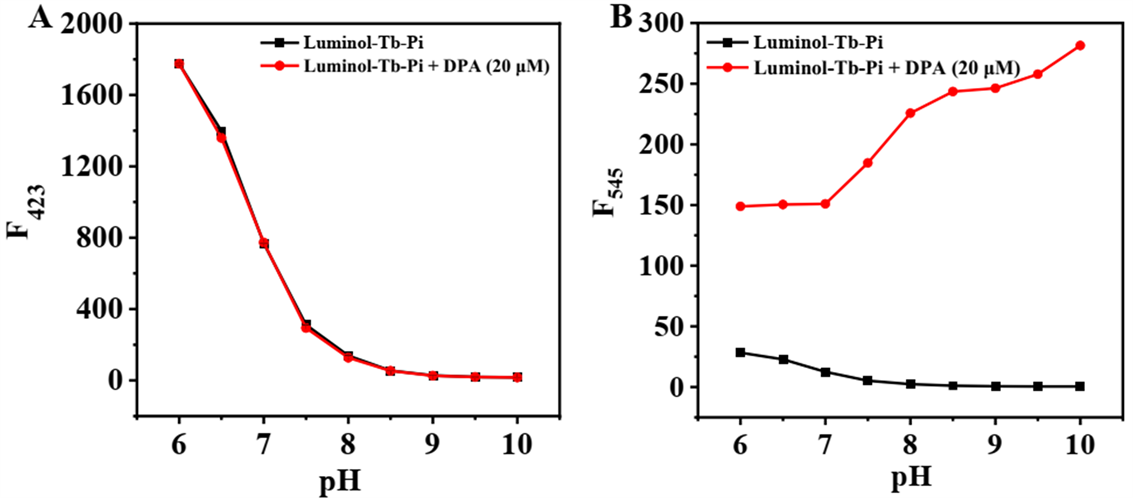
Figure 4. (A) Effect of pH on the fluorescence intensity of Luminol at 423 nm in Luminol-Tb-Pi complex system before and after addition of DPA. (B) Effect of pH on the fluorescence intensity of Luminol at 545 nm in Luminol-Tb-Pi complex system before and after addition of DPA. Luminol: 50 µM; Tb3+: 50 µM; DPA: 20 µM; Pi: 50 µM; λex = 280 nm
图4. (A) pH对Luminol-Tb-Pi配合物体系中Luminol在423 nm处的荧光强度的影响;(B) pH对Luminol-Tb-Pi配合物体系中Tb3+在545 nm处的荧光强度的影响;Luminol:50.0 µM;Tb3+:50.0 µM;DPA:20.0 µM;Pi:50.0 µM;λex = 280 nm
3.2.4. 响应时间优化
荧光稳定性和响应时间也是评估荧光传感性能的重要参数,因此,探究了加入一定量DPA后,Luminol-Tb-Pi探针体系的荧光强度随时间的变化情况,如图5所示。结果表明,Luminol-Tb-Pi体系在2 min内即可实现对DPA的完全响应,并其荧光强度在60 min内保持稳定,因此选择2 min作为DPA检测的响应时间。
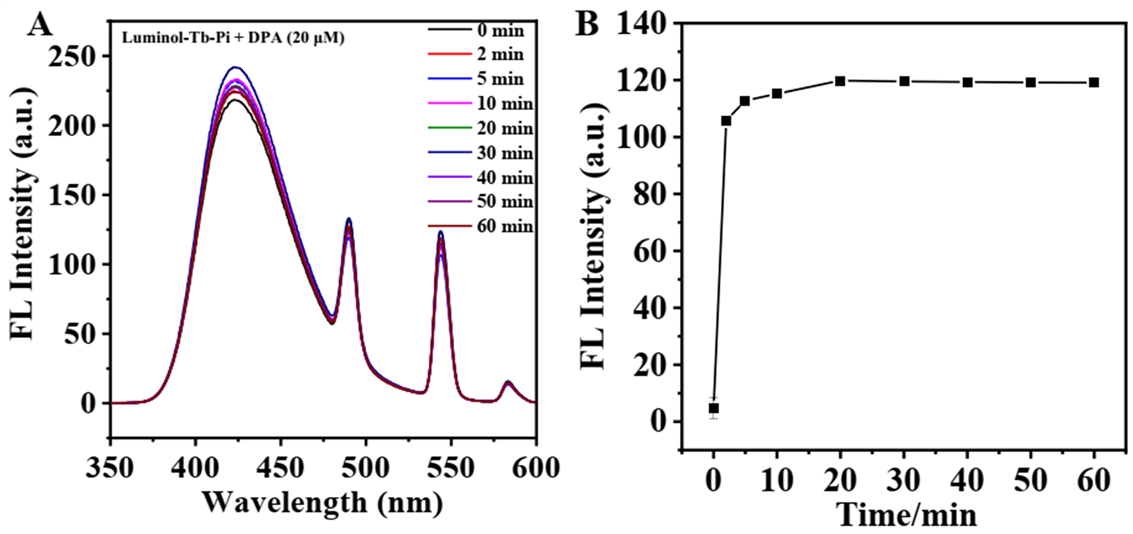
Figure 5. (A) Fluorescence spectra of the Luminol-Tb-Pi system at different times after the addition of DPA; (B) Fluorescence intensity of the Luminol-Tb-Pi complex system at different times after the addition of DPA; Luminol: 50 µM; Tb3+: 50 µM; DPA: 20 µM; Pi. 50.0 µM; Tris-HCl buffer: 10 mM (pH = 7.5); λex = 280 nm
图5. (A) Luminol-Tb-Pi配合物体系加入DPA之后在不同时间点的荧光光谱图;(B) Luminol-Tb-Pi配合物体系加入DPA后在不同时间点的荧光强度变化;Luminol:50 µM;Tb3+:50 µM ;DPA:20 µM;Pi:50 µM;Tris-HCl buffer:10 mM (pH = 7.5);λex = 280 nm
3.3. 荧光探针对DPA的定量分析
在上述优化条件下,我们探究了Luminol-Tb-Pi荧光探针对DPA的检测性能。如图6(A)所示,随着探针体系中DPA浓度的逐渐增加(0.2~45 μM),Tb3+的特征荧光逐渐增强,而体系中Luminol的荧光逐渐减弱。并且DPA在0.2~45 µM的浓度范围内,通过绘制剂量效应曲线发现探针的荧光强度比值F545/F423和DPA浓度之间存在良好的线性关系,线性回归方程式为y = 0.04893x − 0.21202,R2 = 0.9891 (图6(B))。此外,基于LOD = 3σ/k (σ是指11个空白样品信号值的标准偏差,k是线性回归方程式的斜率,即0.04893),计算得到该荧光探针对DPA的检测限为0.051 μM,该方法的LOD远低于炭疽杆菌孢子对人类的传染剂量(60 μM),表明该传感方法对DPA的灵敏检测性能。
此外,我们对比考察了不存在Pi调控的Luminol-Tb配合物体系对DPA响应性能,结果如图6(C),图6(D)所示。与Luminol-Tb-Pi荧光探针相比,Luminol-Tb配合物体系对DPA的响应相对较弱,即DPA对Tb3+的特征荧光敏化作用明显较弱,并且荧光强度比值F545/F423和DPA浓度之间线性关系较差,该对比结果说明基于Pi调控的Luminol-Tb-Pi探针对DPA具有更高的检测灵敏性。
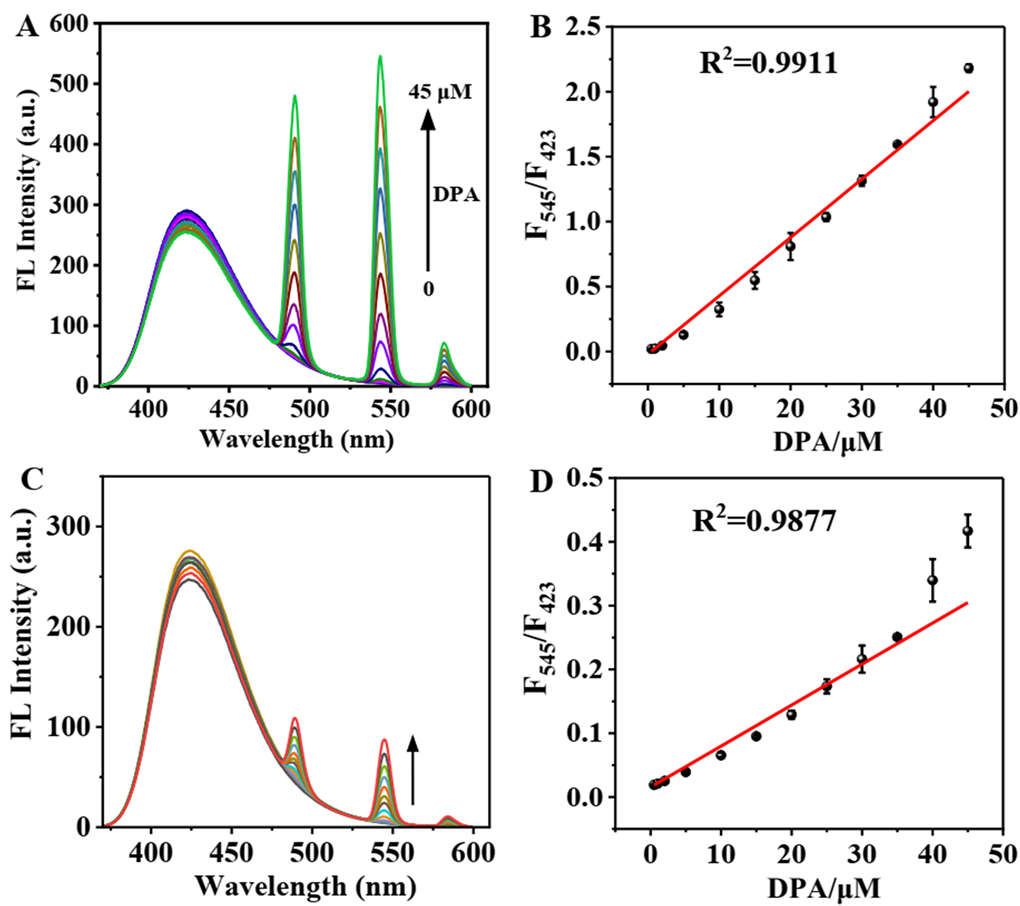
Figure 6. Fluorescence spectra of the Luminol-Tb-Pi complex system after addition of different concentrations of DPA (A) and the linear relationship between F545/F423 and CDPA (B); Fluorescence spectra of the Luminol-Tb complex system after addition of different concentrations of DPA (C) and the linear relationship between F545/F423 and CDPA (D)
图6. Luminol-Tb-Pi配合物体系在加入不同浓度DPA后的荧光光谱图 (A)以及该探针体系中F545/F423与DPA浓度之间的线性关系 (B);Luminol-Tb配合物体系在加入不同浓度DPA后的荧光光谱图 (C)以及该探针体系中F545/F423与DPA浓度之间的线性关系 (D)
3.4. 荧光探针对DPA的选择性分析
为了评估该荧光探针对DPA检测的实际应用潜力,考察了Luminol-Tb-Pi体系对DPA检测的特异性,如图7所示。只有DPA使探针体系的荧光强度比值F545/F423迅速增大,而在加入其他有机化合物(L-亮氨酸(L-leucine)、L-谷氨酸(L-glutamic acid)、L-半胱氨酸(L-cysteine)、D-丙氨酸(D-alanine)、鸟苷一磷酸(GMP)、腺苷一磷酸(AMP)、牛血清白蛋白(BSA)、葡萄糖(glucose)、柠檬酸(citric acid)、尿酸(uric acid)、烟酸(nicotinic acid)、土霉素(oxytetracycline))或者多种无机离子(K+、Na+、Ca2+、Mg2+、Ba2+、Fe3+、Fe2+、Cu2+、Cr3+、
、
、
、
、
、
、
)后,荧光强度比值未出现明显变化,说明该荧光探针对DPA检测具有良好的选择性。
此外,抗干扰是评价荧光探针应用性能的重要条件之一,在多种可能共存干扰物存在条件下,考察了该荧光探针对Luminol-Tb-Pi探针的抗干扰性。结果表明,有机物质几乎不会干扰DPA的测定,其它可能共存的常见离子也几乎都不干扰测定。对于细菌孢子等生物有机体,这些金属离子在有机体中的浓度非常低,因此对DPA检测的干扰可以忽略不计。以上结果表明该荧光探针对DPA的测定具有较好的选择性,在实际样品检测中具有一定的应用潜力。
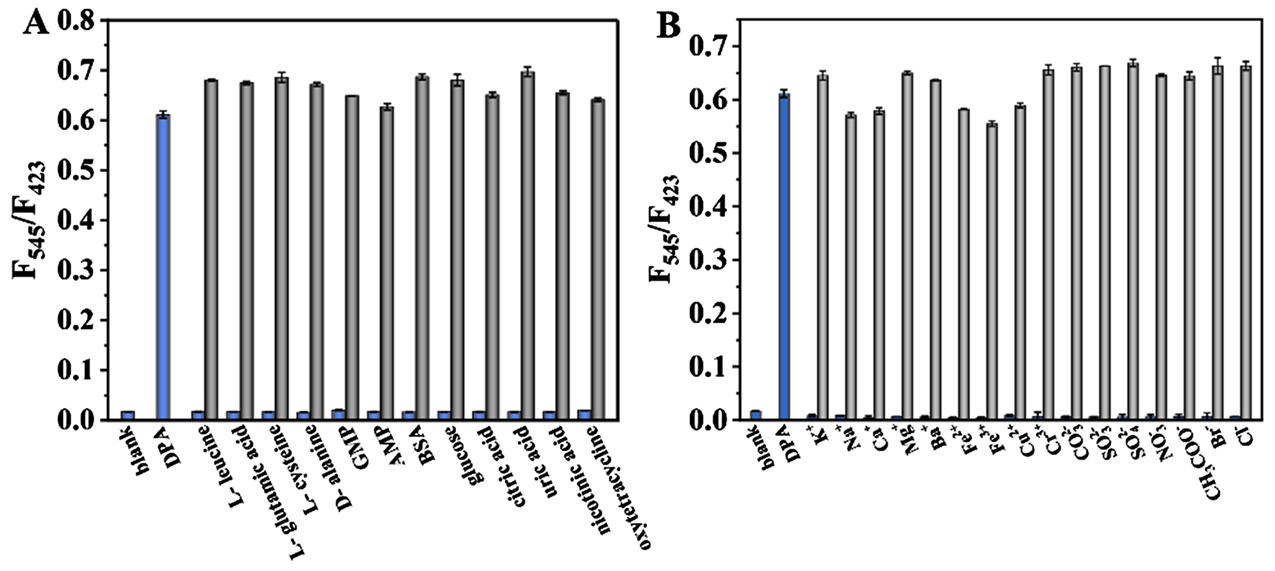
Figure 7. The selectivity and anti-interference of Luminol-Tb-Pi fluorescent probe for DPA detection. The concentration of DPA and all inorganic ions and organic molecules is 20 µM, λex = 280 nm
图7. Luminol-Tb-Pi探针体系对DPA的选择性与抗干扰性检测,DPA:20 µM;有机化合物和无机离子均为20 µM;λex = 280 nm
3.5. 样品中DPA的测定

Table 1. Detection of DPA in real samples
表1. 实际样品中DPA的检测
为进一步考察所提方法的实用性,通过标准加入法考察了该方法对样品中DPA的回收率情况,测定结果如表1所示。荧光探针对样品中DPA的检测回收率在90.98%~108.35%之间,标准偏差值不超过0.5%,说明本方法可用于对样品中DPA的可靠检测。因此,本工作开发的荧光探针在评估环境样品中炭疽杆菌浓度方面具有一定的应用前景。
4. 结论
本工作构建了一种可用于灵敏选择性检测炭疽杆菌生物标志物DPA的稀土配合物荧光探针(luminol-Tb-Pi)。该探针以luminol为有机配体,Tb3+为中心离子,在Pi的调控下,DPA的加入可以使Tb3+特征荧光显著增强,同时引起luminol荧光淬灭。因此,基于DPA敏化的Tb3+特征荧光增强和luminol荧光淬灭的双信号变化,实现了对0~45 μM DPA的定量检测,且该探针可实现对DPA的高特异性和抗干扰性检测。此外,基于DPA引起的探针体系荧光颜色变化可实现对DPA的可视化检测。本工作开发的荧光传感方法操作简单、成本低,在检测炭疽生物标志物方面具有良好的应用潜力。
基金项目
本项目由国家自然科学基金(No. 22106076)和江苏省大学生创新创业训练计划项目(No. 202310304102Y)支持。
NOTES
*通讯作者。