摘要: 为明晰活性炭对天然气中气态单质汞的吸附效果,从气流流量、初始汞蒸汽浓度、吸附温度和吸附动力学等入手,研究了载硫活性炭对汞的吸附性能。结果表明气流流量对AC
S吸附汞的影响较小,且提高初始汞蒸汽浓度,可以促进AC
S对Hg的吸附和单位吸附容量。吸附温度升高可以促进AC
S对汞的吸附率,AC
S吸附汞的最佳温度介于60℃~80℃之间。采用准二级动力学过程对AC
S吸附汞过程进行了拟合,相关系数R
2为0.995,表明AC
S吸附汞过程遵循Langmuir吸附等温方程。
Abstract:
In order to investigate the adsorption effect of activated carbon on gaseous elemental mercury in natural gas, the adsorption performance of sulfur-loaded activated carbon on mercury was studied based on the flow rate, initial concentration of mercury vapor, adsorption temperature and adsorption kinetics. The results showed that flow rate has little effect on Hg adsorption by ACS, and increasing the initial concentration of mercury vapor can promote the adsorption and unit adsorption capacity of Hg by ACS. The increase of adsorption temperature can promote the adsorption rate of mercury by ACS, and the optimal temperature of mercury adsorption by ACS is between 60˚C~80˚C. The quasi-second-order kinetic process was used to fit the mercury adsorption process of ACS, and the correlation coefficient R2 was 0.995, indicating that the mercury adsorption process of ACS followed the Langmuir adsorption isothermal equation.
1. 引言
天然气是地质体内烃类气体和非烃类气体的总称,包括C1~C5烃类气体和N2、CO2、H2、H2S、He和Ar等。天然气还含有众多的微量元素,这些元素主要由生物有机体在形成天然气阶段所带入呈纳米级微粒游离于天然气中,研究报道有50余种 [1] [2] [3] 。有些微量元素在天然气运输储藏中存在许多不安全因素,当它们沉降附着或渗透在管道输送和下游燃气工业所使用的各种高温设备、元件和材料表面时,会导致金属高温腐蚀、材料衰老和管道堵塞等危害,缩短设备使用寿命,甚至进一步引发安全事故 [4] [5] [6] 。特别是天然气中的Hg及其化合物具有高毒性和腐蚀性,能与金属发生汞齐反应使管道金属脆裂,在天然气加工的系列过程中,Hg也可使催化剂中毒 [7] 。天然气中的Hg主要以单质汞形态存在,单质Hg的高挥发性且难溶性的特点致使天然气中Hg的控制依然面临较大的挑战。目前,一般认为吸附是控制天然气Hg污染最为可行的方法。改性活性炭吸附天然气脱Hg已被证实是切实有效的,且表现出了较好的脱汞性能 [8] [9] [10] 。
本文活性炭为购买的载硫活性炭,模拟脱除天然气中单质Hg的性能。研究了活性炭对汞的吸附特性及规律,考察了气体流量、吸附温度、汞蒸汽浓度对天然气中汞脱除的影响效果,为天然气脱Hg及安全使用提供基础数据。
2. 实验部分
商业载硫活性炭记为ACS。对ACS过筛,40~50目粒径范围内ACS作为脱汞吸附剂。吸附装置主要由模拟天然气(主要成分为CH4)、汞渗透管(QWG-6-6)、温控系统、吸附管(HBDYG)、尾气净化装置等组成。实验开始前,用高纯度氮气置换装置中空气10 min,汞蒸气由置于U型石英管内的汞渗透管产生,并通入模拟天然气,整个吸附装置采用保温材料保持恒温,模拟天然气和汞蒸气混合后通过吸附管,尾气经尾气吸收液后排入大气。吸附管直径为20 mm,长为100 mm,ACS均匀铺放于内,实验所用ACS量均为50 mg。尾气吸收液为酸性高锰酸钾溶液。
ACS的脱汞性能用吸附效率η和单位吸附量表示q表示。
(1)
(2)
式中,Cout为出口汞浓度,μg/m3;Cin为入口汞浓度μg/m3;q为单位质量活性炭汞吸附量,μg/g;Q为模拟气体体积流量,m3/min;t为吸附时间,min;m为活性炭质量,g。
3. 结果与讨论
3.1. 气流流量对汞吸附的影响
图1为不同气流流量下对吸附效率的影响,实验共设置了4组不同的气流流量,分别为1 L/min、1.5 L/min、2 L/min、2.5 L/min,吸附管温度保持常温,初始汞蒸汽浓度设置为19.72 μg/m3。图1中可以看出,ACS用量为50 mg的条件下,当气流流量从1 L/min提高到2.5 L/min时,其初始吸附汞效率从88.1%下降至79.5%,表明气流流量对ACS吸附汞的性能有一定程度影响。有研究认为 [11] ,气流流量增加,意味着单位时间内反应物分子数的减少,也进一步降低了反应分子之间的碰撞机率,从而导致ACS吸附汞效率的降低。而且图1也可以发现随着吸附时间的增加,ACS对气态单质汞的吸附效率也会降低,例如,在1 L/min的气流流量下,在吸附时间为90 min内,其吸附效率从88.1%下降到了80.2%。从总体上看,ACS对单质汞的吸附效率随气流流量增加而降低的幅度不大,此现象可能与ACS吸附过程的内扩散有关 [11] 。
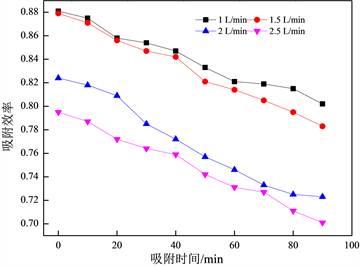
Figure 1. Effect of gas flow on mercury adsorption by ACS
图1. 气体流量对ACS吸附汞的影响
3.2. Hg浓度对ACS吸附效率的影响
图2为不同初始单质汞蒸汽浓度对ACS吸附汞效率的影响,前期研究表明我国天然气中的汞含量在0~50 μg/m3,因此本实验设置了3组汞蒸气初始浓度,分别为:19.72、27.35和48.64 μg/m3。吸附管温度为常温,气体流量为1 L/min。从图2可以看出,在吸附初始阶段,随着汞蒸汽的初始浓度增加,ACS对汞的吸附效率逐步增加,但在吸附时间达到40 min以后,ACS对汞的吸附效率明显下降。而且随着吸附管入口汞蒸汽浓度越高,其下降的程度越明显。这可能是因为高浓度的汞蒸汽为汞分子向ACS内部活性点位扩散提供了驱动力,从而提高了ACS对汞的吸附效率。但随着吸附进一步的进行,汞分子对活性点位的覆盖,致使ACS对汞的吸附效率会随反应进行而明显下降。

Figure 2. Effect of Hg concentration on mercury adsorption by ACS
图2. Hg浓度对ACS吸附汞的影响
3.3. 温度对ACS吸附效率的影响
图3为不同吸附管温度对ACS吸附Hg效率的影响,初始汞蒸汽浓度为19.72 μg/m3,流量为1 L/min,吸附管温度分别设为室温,40℃,60℃,80℃。从图3可以看出,随吸附管温度由室温升高至80℃,ACS吸附Hg效率呈上升趋势,当吸附温度由室温升至80℃时,初始吸附效率由87.9%增加至93.2%。但随吸附时间的延长,ACS吸附Hg效率呈下降趋势,特别是在80℃时,当吸附时间超过30 min后,其吸附效率明显下降。同时,本研究也表明在室温下,ACS对汞也具有较高的吸附效果,有研究表明 [11] 这与硫和汞反应所需的吉布斯自由能以及具有化学吸附活化能的分子数相关。温度升高,促进了吸附区域内的分子活化,进而产生大量具有化学吸附活化能的分子。同时,分子运动速率加快,硫与汞分子有效碰撞增多,吸附反应速率提高。
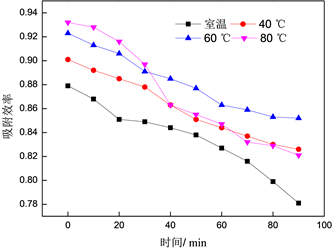
Figure 3. Effect of temperature on adsorption efficiency of Hg by ACS
图3. 温度对ACS吸附Hg效率的影响
3.4. ACS吸附动力学
吸附动力学用于描述ACS对Hg的吸附反应快慢,Hg在时刻t的吸附量可由式(3)计算:
(3)
式中,Qe为t时刻下Hg的吸附量,mg/g;Ci为Hg的初始浓度,μg/m3;Ce为t时刻下Hg的浓度,μg/m3;V为气体流量,L/min;M为ACS用量,mg。
本实验中,采用准二级动力学模型对Hg在ACS的吸附数据进行了拟合。准二级动力学模型是基于Langmuir吸附等温方程,以化学吸附为主 [12] ,准二级动力学方程如式(4)所示 [13] :
(4)
式中,Qt为t时刻下Hg的吸附量,mg/g;Qe为平衡吸附量,mg/g;k1为准二级动力学吸附常数,g/(mg·min)。
表1给出了ACS吸附汞的准二级动力学拟合结果。从表1可以看出,准二级动力学对ACS吸附汞过程拟合性好,Qe为0.437 mg/g,吸附常数k1为1.54 × 10−6,相关系数R2为0.995。说明化学吸附是整个汞吸附过程的控制步骤 [14] 。同时也表明ACS吸附汞过程遵循Langmuir吸附等温方程。

Table 1. Quasi-second-order kinetic model fitting results
表1. 准二级动力学模型拟合结果
4. 结论
本文对ACS吸附气态单质汞进行了详细的研究,分别考察了初始汞蒸气浓度、吸附温度、气体流量和吸附发动力学。实验得出以下结论:
(1) 结果发现气流流量对ACS吸附汞的影响较小,且初始汞蒸汽浓度越高,可以促进ACS对Hg的吸附和单位吸附容量。
(2) 吸附温度升高可以提高吸附区域内的分子的活化,提高ACS对汞的吸附率,且实验得出,ACS吸附汞的最佳温度介于60℃~80℃之间。
(3) 采用准二级动力学过程对ACS吸附汞过程进行了拟合,拟合相关系数R2为0.995。说明化学吸附是整个汞吸附过程的控制步骤。同时也表明ACS吸附汞过程遵循Langmuir吸附等温方程。
基金项目
达州市科技计划项目,项目编号:20ZDYF0015。
NOTES
*通讯作者。