1. 引言
大蝎子草为荨麻科蝎子草属大蝎子草Girardinia diversifolia (Link) Friis.的新鲜或干燥的全草或根部,又名红禾麻、老虎禾麻。其味苦、辛,性凉,有毒,有祛风解表、利气消痰、清热解毒等的功效。用于治疗伤风咳嗽、胸闷痰多等,外用治疮毒 [1] [2] [3] 。目前对大蝎子草的研究尚且较少,多集中于大蝎子草的化学成分与药理作用方向,有待挖掘。前人调查发现,大蝎子草在贵州部分少数民族用药中被当作红禾麻使用 [4] ,但2003版《贵州省中药材、民族药材质量标准》中红禾麻的基源为荨麻科植物珠芽艾麻 [5] ,直至2022年大蝎子草才被确定为红禾麻的另一基源 [6] 。现代研究发现,大蝎子草具有多种活性成分,例如东莨菪内酯、对羟基肉桂酸、黄酮、三萜、多糖等 [4] [7] [8] [9] 。具有很好的抗炎镇痛作用 [10] ,常用于治疗风湿性关节炎、骨关节炎等 [11] 。
标准汤剂是一种中药制剂,是以中医理论和临床应用为前提,现代提取方法、标准化工艺、单味饮片为关键因素,标化临床用药准确性和剂量统一性为目的所产生的汤剂 [12] ,对药物的使用及研究具有规范性作用。因此,为促进民族药物资源的开发应用探讨大蝎子草标准汤剂对大鼠骨关节炎的药理作用及机制,本研究以SD大鼠为实验对象,建立由木瓜蛋白酶和L-半胱氨酸混合溶液诱导的骨关节炎模型,为揭示大蝎子草标准汤剂抗炎镇痛、保护骨关节的机制提供一定的理论依据,以期为大蝎子草标准汤剂的后续研究和临床用药提供参考。
2. 材料
2.1. 实验主要试药
塞来昔布胶囊(批号DR7993,辉瑞制药有限公司);木瓜蛋白酶(批号716M022,索莱宝科技有限公司);L-半胱氨酸(批号820N0219,索莱宝科技有限公司);苏木素–伊红染液(货号C200301,C200403,珠海贝索生物技术有限公司);大鼠肿瘤坏死因子(TNF)-α、白细胞介素(IL)-1β ELISA测定试剂盒(欣博盛生物科技有限公司,批号分别为R221014-007b,R221014-102b);50 × TAE (北京索莱宝科技有限公司,批号20220920);超纯PNA提取试剂盒(Ultrapure RNA Kit) (康为世纪公司,货号CW0581M);绿色荧光核酸染料(10,000×) (北京索莱宝科技有限公司,货号G8140);HiScript II One Step qRT-PCR SYBR Green Kit (Vazyme公司,货号Q221-01)。
大蝎子草药材由国药集团同济堂(贵州)制药有限公司提供,经贵州中医药大学魏升华教授鉴定为荨麻科蝎子草属大蝎子草Girardinia diversifolia (Link) Friis的干燥全草。
2.2. 实验动物
SPF级雄性SD大鼠60只,体质量180~220 g,购自于长沙市天勤生物技术有限公司,许可证号:Scxk (湘)2019-0014。适应性喂养一周。
2.3. 实验主要仪器
RE-2000B型旋转蒸发仪(上海亚荣生化仪器厂);转轮式切片机(徕卡-2016,德国);正置荧光显微镜(DM500,德国徕卡);成像系统(德国徕卡);涡旋混合器(XW-80A,江苏其林贝尔);自动酶标仪(EL10A,BIOBASE);实时荧光定量(qRT-PCR)仪(QuantStudio 1, Applied Biosystems));低温离心机(C2500,湖南湘仪实验仪器厂);凝胶成像仪(4600SF,上海天能科技有限公司),电子天平(PPT-A + 100,美国康州HZ电子科技有限公司)。
3. 方法
3.1. 试剂的制备
3.1.1 不同剂量大蝎子草标准汤剂样品的制备
大蝎子草标准汤剂制备方法:参照《中药配方颗粒质量控制与标准制定技术要求》制备标准汤剂,采用水煎煮法进行制备,以纯水为提取溶剂,提前浸泡0.5 h。取适量饮片,一煎料液比为1:16,武火煮沸,文火煎煮40 min,过滤;二煎料液比为1:14,武火煮沸,文火煎煮30 min,过滤,合并2次滤液,减压浓缩至0.98~1.10 g/mL,即得。
称取3批适量大蝎子草药材,按“大蝎子草标准汤剂制备方法”分别制备浓度为0.28 g/mL、0.56 g/mL、1.12 g/mL的浓缩液,作为低、中、高剂量的大蝎子草标准汤剂样品溶液备用。
3.1.2. 阳性样品的制备
纯水溶解塞来昔布胶囊制得,即得阳性样品。
3.1.3. 试剂的制备
6%木瓜蛋白酶和0.09 mol/L L-半胱氨酸的混合溶液:以生理盐水为溶剂溶解0.6 g木瓜蛋白酶和54 mg L-半胱氨酸,定容至10 mL,即得。
3.2. 造模、分组及给药
采用膝关节腔注射6%木瓜蛋白酶和0.09 mol/L L-半胱氨酸的混合溶液的方法建立OA大鼠模型。将大鼠随机分为空白组、模型组、阳性组、大蝎子草标准汤剂低、中、高剂量组,每组10只。于造模的第1、3、7天给大鼠单侧关节腔内注射0.2 mL的6%木瓜蛋白酶和0.09 mol/L L-半胱氨酸混合溶液(空白组除外,空白组注射等剂量的生理盐水),于造模第14天,观察造模情况,并开始给药治疗,持续4周。阳性组每天灌胃18 mg/kg剂量的塞来昔布胶囊溶液,大蝎子草标准汤剂低、中、高剂量组则每天分别灌胃1.25、2.5、5.0 g生药/kg的标准汤剂,空白组、模型组则每天灌胃等量纯水。
3.3. OA样品收集与处理
各组大鼠给药结束禁食24 h,称重后麻醉,腹主动脉取血致死。称量每只大鼠的胸腺和脾脏脏并计算脏器指数(即为目的脏器重量占机体体重的百分比);4%多聚甲醛固定部分大鼠的膝关节(距其关节5 mm处剪断,生理盐水冲洗,滤纸吸干),另一部分打开关节腔,剥离滑膜组织,剥离后的组织与滑膜−80℃冻存,备用。
3.4. 指标检测
3.4.1. 一般情况观察
记录实验期间大鼠的每周体重变化。观察记录大鼠的一般情况,如毛发、精神状态、行为、膝关节肿胀程度情况等。
3.4.2. 各脏器指数
称量每只大鼠的胸腺和脾脏重量并计算脏器指数(即为目的脏器重量占机体体重的百分比)。
3.4.3. HE染色观察大鼠膝关节病理改变
4%多聚甲醛固定部分大鼠的膝关节(距其关节0.5 cm处剪断,生理盐水冲洗,滤纸吸干),经脱水、包埋、切片、染色、封片后制得大鼠膝关节组织HE染色切片,观察膝关节组织形态变化。
3.4.4. 大鼠滑膜组织中炎症因子水平检测
取出各组大鼠滑膜组织,采用ELISA法检测滑膜组织中TNF-α、IL-1β水平,根据ELISA试剂盒检测说明书进行检测。
3.4.5. 大鼠膝关节软骨组织OA相关基因的表达检测
取出各组大鼠膝关节软骨组织,采用qRT-PCR法检测Sox-9、MMP13、Colx mRNA表达水平。按照TRIzon说明书进行操作,使用TRIzon Reagent试剂提取总RNA;反转录成cDNA,以cDNA模板;β-actin为内参基因,20 uL的PCR反应体系,反应条件:55℃逆转录5 min,95℃预变性5 min,循环反应:95℃、10 s和60℃、30 s,40个循环,溶解曲线:default。反应结束后,根据扩增曲线、溶解曲线,2−ΔΔCT法计算Sox-9、MMP13、Colx、β-actin mRNA表达。所有引物均由生工生物工程(上海)股份有限公司设计合成,具体序列见表1。

Table 1. Primer sequences and product sizes used for PCR
表1. PCR所用引物序列及产物大小
3.5. 统计学处理
采用SPSS 26.0软件分析处理数据。计量资料均以(
)表示,ANOVA法分析、LSD检验方差齐性的数据;Welch法分析、Tamhanes法检验方差不齐的数据。P < 0.05表示差异具有统计学意义。
4. 结果
4.1. 一般情况观察
为了解苗药大蝎子草标准汤剂对OA大鼠骨关节炎的影响,对大鼠的一般情况进行研究。造模后,与空白组相比,其余各组大鼠皮毛较暗淡,精神状态较差,进食减少,体重减轻或增长缓慢,行动力差,活动量较少,膝关节红肿较严重。经给药干预后,与模型组相比,各给药组大鼠精神状态随着治疗逐渐变好,皮毛变顺滑,精神状态均有所好转,饮食逐步增加,活动量增加,膝关节红肿程度逐步减轻。随着给药时间体重逐渐增加,其中大蝎子草标准汤剂低剂量组体重增长最显著,结果见表2。

Table 2. Changes in body weight of rats in each group (
, n = 6)
表2. 各组大鼠体重变化情况(
, n = 6)
注:与空白组相比,*P < 0.05,**P < 0.01;与模型组相比,#P < 0.05。
4.2. 大蝎子草标准汤剂对OA大鼠免疫器官脏器指数的影响
为了解苗药大蝎子草标准汤剂对OA大鼠骨关节炎的影响,对大鼠免疫器官脏器指数进行了研究,结果见表3。与空白组相比,模型组胸腺指数、脾脏指数均高于空白组,但无显著性差异(P > 0.05);与模型组相比,大蝎子草标准汤剂组的胸腺指数和脾脏指数均低于模型组,其中低剂量组和高剂量组胸腺指数显著低于模型组(P < 0.05),低剂量组和中剂量组脾脏指数显著低于模型组(P < 0.05)。说明大蝎子草标准汤剂能够影响OA大鼠的免疫器官,降低OA大鼠胸腺及脾脏指数,不同剂量组之间的影响不同。

Table 3. Effect of standardized broth of Great Scorpion Grass on immune organs of OA rats (
, n = 6)
表3. 大蝎子草标准汤剂对OA大鼠免疫器官的影响(
, n = 6)
注:与空白组相比,*P < 0.05;与模型组相比,#P < 0.05,##P < 0.01。
4.3. 大蝎子草标准汤剂对OA大鼠膝关节病理变化的影响
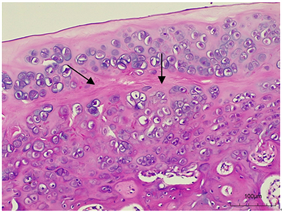
为了解苗药大蝎子草标准汤剂对OA大鼠骨关节炎的影响,对大鼠膝关节病理变化情况进行研究,结果如图1。空白组大鼠膝关节未见明显病理改变,表面软骨完整,平滑,未见明显组织增生、炎性细胞浸润等;与空白组相比,模型组大鼠发生病变,膝关节表面透明软骨出现明显纤维组织增生,出现大量炎性细胞浸润;各给药治疗组大鼠膝关节组织病变均有一定的改善,但仍出现膝关节表面透明软骨被破坏,部分区域纤维化,出现炎性细胞浸润等病理变化。


空白组(200×) 模型组(200×)纤维化(→)
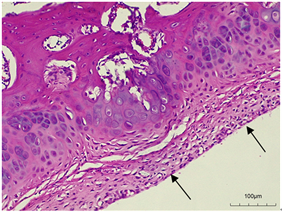 阳性组(200×)纤维化(→) 大蝎子草标准汤剂低剂量组(200×)纤维化(→)
阳性组(200×)纤维化(→) 大蝎子草标准汤剂低剂量组(200×)纤维化(→)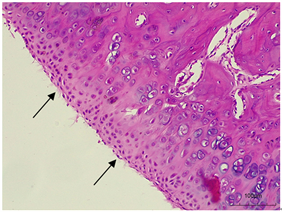
 大蝎子草标准汤剂中剂量组(200×)纤维化(→)大蝎子草标准汤剂高剂量组(200×)纤维化(→)
大蝎子草标准汤剂中剂量组(200×)纤维化(→)大蝎子草标准汤剂高剂量组(200×)纤维化(→)
Figure 1. Lesions in the knee joint tissues of rats in each group (HE, ×200)
图1. 各组大鼠膝关节组织的病变情况(HE, ×200)
4.4. 大蝎子草标准汤剂对OA大鼠膝关节滑膜组织中TNF-α、IL-1β水平的影响
为了解苗药大蝎子草标准汤剂对OA大鼠骨关节炎的影响,对大鼠膝关节滑膜组织中TNF-α和IL-1β水平情况进行研究,结果如表4。与空白组相比,模型组大鼠滑膜组织中两种炎症因子水平均极显著升高(P < 0.01);与模型组相比,各给药治疗组大鼠滑膜组织中两种炎症因子水平(除大蝎子草标准汤剂中剂量TNF-α水平外)均极显著降低(P < 0.01),大蝎子草标准汤剂不同剂量组大鼠膝关节滑膜组织中IL-1β水平呈剂量依赖性增加。以上结果暗示大蝎子草标准汤剂能降低OA大鼠膝关节滑膜组织的炎症因子的释放,减缓炎症反应,对OA大鼠的膝关节具有一定的治疗作用。

Table 4. Results of TNF-α, IL-1β levels in synovial tissue of rats in each group (
, n = 6)
表4. 各组大鼠滑膜组织中TNF-α、IL-1β水平结果(
, n = 6)
注:与空白组相比,*P < 0.05,**P < 0.01,***P < 0.001;与模型组相比,##P < 0.01,###P < 0.001。
4.5. 大蝎子草标准汤剂对OA大鼠膝关节软骨组织Sox-9、MMP13、Colx mRNA表达的影响
为了解苗药大蝎子草标准汤剂对OA大鼠膝关节骨关节炎的影响,对大鼠膝关节软骨组织Sox-9、MMP13、Colx mRNA表达情况进行研究,结果如表5。与空白组比较,模型组Sox-9 mRNA表达量极显著降低(P < 0.01),MMP13、Colx mRNA表达量极显著增加(P < 0.01);与模型组相比,除大蝎子草标准汤剂低剂量组外,中剂量组和高剂量组Sox-9 mRNA的表达均显著高于模型组(P < 0.05);各给药治疗组中MMP13、Colx mRNA表达量均极显著性低于模型组(P < 0.01)。以上结果暗示大蝎子草标准汤剂能提高软骨细胞中Sox-9 mRNA的表达,降低MMP13、Colx mRNA的表达,从而改善膝关节软骨组织炎症情况。

Table 5. Results of relative expression content of Sox-9, MMP13, and Colx in cartilage tissues of rats in each group (
, n = 6)
表5. 各组大鼠软骨组织中Sox-9、MMP13、Colx相对表达含量结果(
, n = 6)
注:与空白组相比,*P < 0.05,**P < 0.01,***P < 0.001;与模型组相比,##P < 0.01,###P < 0.001。
5. 讨论
骨关节炎(osteoarthritis, OA)是关节退行性疾病,以关节软骨纤维化、溃疡、破裂等造成的疼痛为主要表现,关节处会出现慢性肿、痛,僵硬,畸变等临床表现,使患者饱受病痛的折磨,阻碍患者的行动,影响患者的基本日常活动 [13] 。病理特征表现为软骨变性破坏、关节边缘骨质增生、滑膜病变、肌肉萎缩无力等 [13] 。可由多种因素诱发,目前尚未出现能治愈的医疗技术或手段,其致病机制的研究还有待深入。TNF-α和IL-1β是OA炎症反应中的主要促炎因子,在患者体内大量存在,两者具有协同作用,能够诱导多种趋化因子、其他炎症因子的产生,影响软骨细胞的合成、代谢,提高其他炎性因子活性、促进骨膜细胞产生前列腺素E2、基质金属蛋白酶等,抑制软骨基质胶原蛋白的合成,从多方面破坏膝关节软骨组织,可降解软骨基质进一步破坏关节 [14] [15] 。基质金属蛋白酶类(matrix metalloproteinase, MMPs)是机体中重要的一类酶,参与机体多项生物学过程及病理过程。与钙、锌等金属离子相结合后才能催化酶活性,降解细胞外基质的蛋白成分,与骨关节炎相关的MMP-13和MMP-3等对软骨基质降解有直接作用,通过分解蛋白多糖,多种骨连接蛋白II、IV、IX型胶原等多种物质,破坏软骨基质,损伤软骨组织,MMPs的过量表达是导致骨关节炎发病的关键病因 [15] [16] [17] 。Sox-9是软骨形成过程中的关键性转录因子,可调节软骨细胞外基质基因的表达,对软骨细胞的增殖至关重要 [18] 。Colx基因在OA患者软骨下层区域高度表达,多于肥大软骨细胞或钙化处特异性表达。Sox-9激活Colx基因的表达,抑制软骨细胞肥大表型,延缓骨关节炎软骨退行性改变,保护关节软骨,维持关节软骨的功能,其中ColX和ColXI、IX、II等胶原纤维交织成网在维持软骨表型稳定方面有重要意义 [19] 。
研究发现中药有效成分防治骨关节炎的作用机制主要包括减少炎症因子、降低氧化应激反应的发生、抑制基质降解酶活性、调控软骨细胞代谢及调控相关信号通路等方面 [20] 。现代研究发现,大蝎子草具有很好的抗炎镇痛作用 [21] [22] ,含有对羟基肉桂酸、总黄酮、芹菜素、山萘酚、多糖等多种有效成分 [23] ,其中总黄酮、山萘酚和多糖具有抗炎镇痛作用 [24] [25] [26] ,芹菜素具有调节骨质疏松、调节骨细胞的作用 [27] 。本研究实验结果表明,大蝎子草标准汤剂对大鼠骨关节炎具有一定治疗作用。不同剂量组的治疗效果不同,不同程度地改善OA大鼠毛色暗淡、关节红肿、运动受限、膝关节纤维组织增生,炎性细胞浸润等情况;滑膜组织中TNF-α和IL-1β炎性因子水平显著降低;软骨组织中Sox-9的mRNA的表达量增加,降低MMP13、Colx的mRNA表达含量显著。综上所述,大蝎子草对OA大鼠具有一定的治疗作用,其作用机制可能与增高软骨组织中Sox-9的mRNA的表达量和降低MMP13、Colx的mRNA的表达量有关,但具体哪些成分具有关键作用值得进一步研究。
基金项目
贵州省科技计划项目(黔科合后补助[2020]3003);国药集团同济堂(贵州)技术服务项目(JS-YF-KY-201912006)。
NOTES
*通讯作者。