1. 引言
非小细胞肺癌(Non-Small Cell Lung Cancer, NSCLC)是肺癌的主要组织学亚型,约占所有类型肺癌的85%。在我国发病率及死亡率均居前列。卡瑞利珠单抗是我国自主研发的PD-1抑制剂,于2019年5月29日,国家药品监督管理局(NMPA)批准上市 [1] ,是一种人源化抗程序性死亡因子-1 (Programmed Cell Death 1, PD-1)抗体,通过与PD-1结合从而阻断PD-1/PD-L1通路,继而激活免疫T细胞,产生持续抗肿瘤效应 [2] 。用于治疗至少经过二线系统化疗的复发或难治性经典霍奇金淋巴瘤。之后,相继获批肝癌、肺癌及食管癌适应症。
卡瑞利珠单抗上市后陆续有相关不良反应报道,根据中国临床肿瘤学会(CSCO)颁布的《免疫检查点抑制药相关的毒性管理指南(2023)》 [3] (下文称CSCO指南),与传统化疗药物和靶向药物不同的是,该药导致的不良反应以免疫相关不良事件为主,主要有皮肤、胃肠道、肺、心肌及内分泌系统最常见,主要以1~2级为主,大部分具有可逆性 [4] 。但是也可能出现严重不良反应,如若处理不及时可能会导致患者死亡,需要引起临床充分重视。
2. 病例资料
患者,男,57岁,既往体健,17年前有“外伤后胸11腰1脊髓损伤后截瘫”史。无过敏史。2018.11无明显诱因下出现咳嗽、咯血,至省肿瘤医院CT检查示肺占位,活检病理示:“右上叶开口:鳞状上皮高级别上皮内瘤,癌变,有浸润(鳞癌)”,诊断为肺鳞癌。同月开始“CPT-11 0.1g d1,8 + NDP 30mg d1~3,8~9”方案一周期化疗及第二周期上半程化疗。复查CT右肺上叶支气管狭窄伴肺门区肿块,右肺下叶软组织结节,上述均拟恶性病变,纵膈及右肺门多发肿大淋巴结,考虑合并转移,上腔静脉受侵狭窄,两肺肺气肿,两肺慢性炎症,疗效评价SD。后开始放疗,同步予“白蛋白紫杉醇200 mg”方案化疗1周期,因畏惧化疗副反应,拒绝后续化疗。期间出现放射性食管炎,予对症治疗后好转,疗效评价PR。后给予“白蛋白紫杉醇 + 卡铂 + 重组人血管内皮抑制素”方案化疗3周期,治疗期间副反应轻微。2019.8治疗方案调整为“卡瑞利珠单抗200 mg q2w + 阿帕替尼0.25 po (口服) qd + 白蛋白紫杉醇300 mg q21d”。后按期给予“卡瑞利珠单抗 200mg”方案免疫治疗6周期,复查评价PD,考虑假性进展,后继续按期免疫治疗2周期。2020.4.23胸 + 全腹增强CT:病变缩小;两肺炎症。病情评价SD,左肺炎症考虑免疫性肺炎,分级:1级,继续予“卡瑞利珠单抗200 mg”方案免疫治疗1周期,2020.5.13肺CT平扫:病变略有缩小;两肺炎症。嘱患者出院后口服激素治疗。2020.8复查,排除其他原因,免疫性肺炎诊断明确,2级,患者无气喘、咳嗽症状,给予地塞米松5 mg ivgtt治疗,2日后拟继续行免疫治疗。之后继续按计划免疫治疗。2020.12.18胸部 + 上腹部增强扫描两肺感染伴支气管稍扩张较前稍吸收。肝功能异常提示药物性肝损伤,予保肝药物对症治疗,病情评价SD。2020.1.22 ALT 79 U/L↑,AST 54 U/L↑,总胆红素正常,如前进行保肝治疗,嘱患者出院后序贯口服保肝药物,半月复查肝功能。药物性肝损伤治疗期间免疫治疗未暂停。2021.3.26肝功能好转。2021.4.20查CT示两肺炎症基本吸收,继续保肝治疗。2021.6.30检查肝功能正常,停止保肝治疗。治疗期间肺部CT及肝功能指标见下图1、图2。
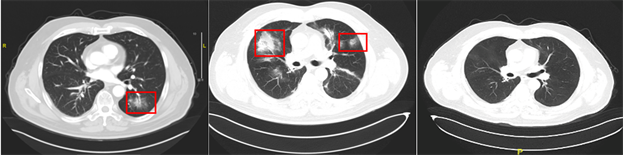 (a) (b) (c)注:(a):2020.4.23刚开始出现1级免疫性肺炎;(b):2020.8.13确诊2级免疫性肺炎;(c):2021.4.20免疫性肺炎恢复。
(a) (b) (c)注:(a):2020.4.23刚开始出现1级免疫性肺炎;(b):2020.8.13确诊2级免疫性肺炎;(c):2021.4.20免疫性肺炎恢复。
Figure 1. CT images of both lungs in different periods
图1. 不同时期双肺CT图
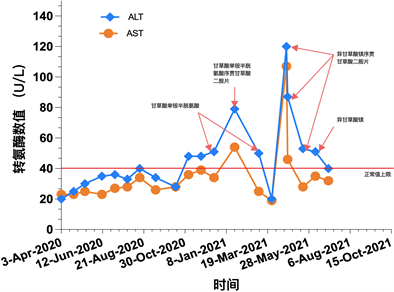 注:ALT:丙氨酸转氨酶;AST:天冬氨酸转氨酶。
注:ALT:丙氨酸转氨酶;AST:天冬氨酸转氨酶。
Figure 2. Schematic diagram of liver function indicators ALT, AST and treatment methods
图2. 肝功能指标ALT、AST与治疗方式示意图
3. 治疗经过
该老年患者一线使用化疗、放疗,后因不能耐受不良反应选择化疗联合抗血管生成与卡瑞利珠单抗免疫治疗,免疫联合治疗1周期、单药治疗8周期后病变缩小,但开始出现1级免疫性肺炎。卡瑞利珠单抗累计使用14个周期后确诊出现2级免疫性肺炎,患者未出现免疫性肺炎相关症状,严重时给予地塞米松5 mg静脉滴注,嘱患者出院后口服激素,激素治疗后肺炎好转,免疫治疗23个周期后两肺肺炎基本吸收。期间,卡瑞利珠单抗治疗19个周期后出现药物性肝损伤,最严重时为2级,先后给予甘草酸单铵半胱氨酸氯化钠200 mlqd ivgtt或异甘草酸镁150 mg序贯或者不序贯甘草酸二胺口服治疗,由于患者与家属治疗积极,期间免疫治疗未暂停。卡瑞利珠单抗治疗26周期后肝功能检查正常,之后均保持正常范围。
4. 讨论
首先,笔者根据国家药品不良反应中心药物不良反应关联性评价标准,认为:① 卡瑞利珠单抗说明书已提及免疫性肝炎与肺炎不良反应;② 两种不良反应与卡瑞利珠单抗存在时间先后关系;③ 使用激素后症状缓解最后消失;④ 影像学检查可证实免疫性肺炎的存在;⑤ 患者基线肝功能正常,故而可以判断该患者使用卡瑞利珠单抗与其发生免疫性肺炎与肝炎的关联性评价为可能。
其次,根据CSCO指南 [3] 中毒性分级评价标准,将免疫相关不良事件(irAEs)从轻度到重度分为5个级别(G1:轻度毒性;G2:中度毒性;G3:重度毒性;G4:危及生命的毒性;G5:与毒性相关的死亡)。患者开始免疫性肺炎病变局限于左肺(<25%肺实质),未出现相关症状,属于G1期。严重时病变累及多于一个肺叶或25%~50%肺脏受累,无气喘、咳嗽症状,属于G2期。患者ALT最高达120 U/L,为3倍ULN,免疫性肝炎属于G2期。
4.1. 免疫性肺炎
4.1.1. 发生率及时间线
有研究报道显示 [5] ,NSCLC患者的肺部毒性通常要高于其他癌种患者,发生率约为3%~5%。卡瑞利珠单抗引起的免疫性肺炎的发生率为1%~6.7% [6] [7] 。真实世界由于患者治疗方案、基线条件复杂,患者出现肺部毒性的概率可能更高。卡瑞利珠单抗说明书记录免疫性肺炎发生的中位时间为3.6个月,范围0.0~27.9个月,持续的中位时间为2.7个月。本病例免疫性肺炎发生的时间为卡瑞利珠单抗用药后约8个月,持续时间为12个月,持续时间较长可能由于患者长期卧床、肺功能基线条件较差,及激素治疗未足量、免疫治疗未暂停导致。
4.1.2. 危险因素
有研究报道 [5] ,使用免疫抑制剂后发生免疫性肺炎的危险因素可能有性别、年龄、吸烟状态、肿瘤病理类型、放疗史等。在Suresh等人 [8] 的一项研究中,男性免疫性肺炎的发病率高于女性,鳞状细胞的发病率高于其他组织学类型。高龄(>70岁)患者出现免疫性肺炎的概率较高 [9] ,这可能是因为高龄患者肺功能下降、肺部基础疾病(如肺部感染、肺气肿、慢阻肺、间质性肺病等)较多引起。患者的吸烟状态也可能影响免疫性肺炎的发病率。使用PD-L1抑制剂出现免疫性肺炎的概率低于使用PD-1。PD-1/PD-L1抑制剂与多种不同药物也与肺炎风险相关,表明多种药物对肺毒性的叠加效应 [10] ,并且一部分由ICI引起的CIP可能转变为慢性CIP [11] 。
4.1.3. 潜在机制
免疫性肺炎在非小细胞肺癌中的发生是多种因素联合作用的结果。通过PD-1/PD-L1单抗阻断PD-1-PD-L1通路,会上调和促进Th1和Th17细胞,下调和抑制Th2细胞和Treg细胞 [12] 。如果不对Th2细胞和Treg细胞进行免疫抑制,Th1和Th17细胞的过度免疫反应和细胞因子分泌会引起肺等正常组织的自身免疫性损伤。此外,活化的T细胞分泌的促炎细胞因子促进炎症细胞的浸润 [13] 。在IL-6的刺激下,肝脏产生的CRP会促进炎症反应,增强自身免疫 [14] 。肠道微生物群通过“肠–肺轴”调节肺内免疫微环境 [15] 。总之,PD-1/PD-L1阻断引起的免疫失调导致了免疫性肺炎的发生发展。
4.1.4. 治疗
根据CSCO指南推荐,不管是免疫性肺炎还是肝炎,治疗上很大程度依赖于激素,当毒性来势凶险使用大剂量激素时,为了防止毒性的复发,临床通常逐步减少激素的用量。其他治疗免疫性肺炎的药物有静脉注射免疫球蛋白(IVIG)、英夫利昔单抗等。本病例患者免疫性肺炎严重时处于G2期,指南推荐的治疗方法有:① 暂停免疫检查点抑制剂(ICIs)治疗,直至降至≤G1;② 静滴甲泼尼龙治疗,48~72 h后若症状改善,激素在4~6周内按照每周5 mg~10 mg逐步减量;若症状无改善,按G3~G4反应治疗;如果不能排除感染,需考虑加用经验性抗感染治疗;③ 3~4周后复查CT;④ 临床症状和影像学缓解至≤G1,评估后可继续使用免疫药物。考虑到患者积极要求抗肿瘤治疗,并且无相关症状,给予G2期患者小剂量激素治疗,推迟免疫治疗但未暂停。
4.2. 免疫性肝炎
4.2.1. 发病率及时间线
肝脏是人体重要的药物代谢器官。与卡瑞利珠单抗相关的肝脏不良反应主要包括AST、ALT、胆红素、γ-谷氨酰转移酶、碱性磷酸酶等升高,其中大多数是1级或2级 [16] 。有临床研究报道,纳武利尤单抗治疗出现免疫性肝炎的发病率为6.9% [17] 。近日,日本药品和医疗器械管理局(PMDA)宣布增加帕博利珠单抗有关暴发性肝炎和肝衰竭的提示。可见其他同类免疫抑制药物治疗过程中也可能出现免疫性肝炎。卡瑞利珠单抗说明书记录在临床研究中10.5%的患者发生免疫性肝炎,至免疫相关性肝炎发生的中位时间为1.6个月,范围为0.0~32.5个月,持续的中位时间的1.5个月,范围为0.0~34.8个月。本病例患者出现免疫性肝炎的时间为开始使用卡瑞利珠单抗后16个月,持续时间约为6.4个月。
4.2.2. 危险因素
根据现有的研究报道,免疫性肝炎的危险因素可能为基础肝病:肝硬化、病毒性肝炎。考虑到我国合并病毒性肝炎(HBV/HCV感染)患者较多的现况,CSCO指南指出应将HBV-DNA控制在2000 U/ml以下再开始免疫治疗,并且治疗过程中需定期监测。
4.2.3. 潜在机制
卡瑞利珠单抗导致免疫性肝炎的机制尚不明确,与此相关的单独研究较少,有假说认为,PD-1/PD-L1信号通路的中断使肝脏易受细胞毒性T淋巴细胞的攻击 [18] 。
4.2.4. 治疗
根据指南推荐,与免疫性肺炎一样,免疫性肝炎的治疗也以激素为主,当效果不佳时可加用麦考酚酯。与免疫性肺炎不同的是,免疫性肝炎治疗时不推荐使用英夫利昔单抗,因为其本身就可能存在肝脏毒性。本病例患者免疫性肝炎最严重时属于G2期,CSCO指南推荐治疗原则为:① 暂停ICIs治疗;② 0.5 mg/kg/d~1.0 mg/kg/d泼尼松龙口服或等效剂量。由于患者及家属强力要求积极进行肿瘤治疗,未静脉使用激素,而使用保肝药物对症处理,患者预后良好。
5. 结论
随着免疫检查点抑制剂的广泛应用,特别是国家将该类药品纳入医保目录以来,免疫相关不良反应越来越受到临床的重视。本研究报道了一例非小细胞肺癌使用卡瑞利珠单抗后相继出现免疫性肺炎与免疫性肝炎的病例,可以观察到卡瑞利珠单抗对非小细胞肺癌具有抑制作用,并且不良反应为轻度且可控,但是临床出现免疫相关不良反应具有一定的滞后性,对于免疫性肺炎与肝炎的早期预测与快速诊断则需要进一步进行深入的机制研究。
致谢
感谢肿瘤科副主任医师张猛提供的支持,感谢药学部主任史友锦的大力支持,感谢家人的精神支持,谢谢大家!
基金项目
连云港市卫生科技项目(QN202313)。