1. 引言
普通生物学课程作为生物类专业基础必修课程,在整个教学环节中具有重要作用。具有涉及多种学科,包括植物学、动物学、微生物学、生态学、细胞学、遗传学、分子生物学和进化生物学等,是一门综合性非常强的基础课程 [1] 。相对应的生物学实验课程具有较强的实践性和操作性,是生物学科生存和发展的基础。普通生物学实验课程在培养学生能力、拓展学生知识面、提升学生综合素质方面具有重要的作用,也为后续课程的学习打下良好的基础,因此普通生物学课堂教学质量的好坏将直接影响学生对生物科学的兴趣及后续专业课程的学习。
实验教学操作性和实践性较强,是学生从理论学习到感性认识的转换,将理论运用于实践的重要课程 [2] 。然而很多高校,尤其是地方院校,存在一些无法克服的客观原因,比如经费预算紧张、缺乏大型实验仪器等,普通生物学实验课程涉及的范围广,但多数实验是以验证性、演示型实验为主,以小组为单位合作开展实验,学生缺乏系统性的思考和连续性的观察 [3] 。无法锻炼学生独立思考、探究和解决问题的能力。在教学上,学校和教师虽然花费了大量的时间和精力,但是学生对演示型实验缺乏兴趣和主动性,参与意愿不强,尤其分组实验,部分同学只是在看别人做,自己像个局外人,认为实验课不会挂科,实验报告敷衍了事,最终导致教学效果差,达不到开设本实验课程的培养目的。众多高校一线教师非常关注如何通过实验教学培养理论与实践能力相结合的高素质人才问题,也进行了诸多探索和尝试 [4] [5] 。现将普通生物学实验教学过程中存在的一些问题进行总结,并对这些问题的解决办法进行了积极的思考和探讨。
为了在实验教学中激发学生的学习兴趣和操作的主动性,培养学生独立思考和科研能力,提高本科教学质量,笔者尝试将亚细胞定位技术引入到地方高校普通生物学实验教学中,让学生在老师的引导下,熟悉实验方案,主导整个实验,全程亲自参与实验的各个步骤,以学生为主体的培养方式,既提高学生的实验操作能力,又培养了学生独立工作和创新思维能力。
2. 亚细胞定位的实验教学方案
2.1. 实验原理
细胞是构成生物体的基本结构单位和功能单位,是生命的物质基础。细胞作为生命的基本单位,其内在存在着复杂的生命过程,而这一过程与细胞内功能特化的细胞器有关。细胞器将细胞内的空间进行区域化,高效而精确的运行,是细胞能完成分类、增殖、呼吸、衰老和凋亡、在物质合成、分选、运输、降解及信号转导等方面有序而精确的控制着 [6] 。细胞的结构复杂精巧且高度有序,亚细胞是比细胞结构更细化的结构,细胞内部结构依据功能和空间分布的不同,可以进一步划分为不同的细胞区域或细胞器,即亚细胞,电子显微镜(EMs)是用来研究亚细胞结构的常用工具。它们的特点是在细胞内,功能和空间相互隔离,又共同协调维持完整的细胞功能。在一定范围内,亚细胞结构等同于细胞器,不过像细胞膜虽然可以叫亚细胞结构,但不是细胞器 [7] 。每种亚细胞结构中都存在一组特定的蛋白质,亚细胞结构为这些蛋白质行使功能提供了相对独立的生命活动场所。同时也只有在相同或相近的亚细胞位置上蛋白质间才会有相互作用。蛋白质是生物生命活动的物质基础和体现者,了解蛋白质在细胞中的分布和亚细胞定位是研究其分子功能的基础。
亚细胞定位即指某种生物大分子物质或脂类在细胞内存在的具体位置。在细胞质中合成的蛋白质,由蛋白质分选信号引导而被转运到特定的亚细胞结构中参与细胞的各种生命活动,该过程称为蛋白质亚细胞定位。蛋白质的功能、代谢以及相互作用等都与其亚细胞定位密切相关,成熟蛋白质必须在特定的亚细胞结构中才能发挥正确稳定的生物学功能,如果定位发生偏差,将对细胞功能甚至生命产生重大影响,因此对蛋白质亚细胞定位的研究具有重要意义 [6] 。亚细胞定位技术是分子生物学中最常用的技术之一。能够对生物大分子在细胞内的具体存在的位置进行定位,如细胞核内、细胞质内、细胞膜、线粒体和叶绿体中等。当前已开发出众多的荧光标记可对目标蛋白进行标记。
利用GFP、RFP等荧光蛋白具有的独特荧光性质和灵敏性,来示踪细胞内的蛋白 [7] 。将目标蛋白与荧光蛋白的N端或者C端融合,通过瞬转或稳转,使该融合蛋白在受体材料细胞内表达,目标蛋白会牵引荧光蛋白一起定位到目标细胞器,经过激光共聚焦显微镜激光照射,荧光蛋白会发出荧光,通过观察荧光蛋白在细胞内显示的位置,从而可以确定目标蛋白的亚细胞定位情况,即可对蛋白质进行精确定位。
绿色荧光蛋白GFP是从发光水母(Aequorea victoria)中分离出来的一个约有238个氨基酸组成的蛋白质,从蓝光到紫外线都能激发其发出绿色荧光 [8] 。GFP作为一种广泛应用的遗传标志物和基因标记物,具有分子量小,与其他质粒构建序列相比,不会降低转化效率;对细胞和组织的生长过程没有损伤;检测方法简便迅速;GFP基因的表达与细胞类型、位置和种类无关。GFP的主要优点在于它无毒,可以在活细胞中表达,从而能够研究动态的生理过程。
2.2. 实验目的
本实验以毛竹SnRK基因为研究对象,实验设计包括毛竹RNA的提取、反转录cDNA、SnRK基因的克隆、载体构建、农杆菌转化、烟草侵染等。绿色荧光蛋白在激光共聚焦显微镜下能够激发出绿色荧光,直观快速的观察目标蛋白在细胞中的亚细胞定位情况。
2.3. 实验材料
2.3.1. 生物材料与试剂
本生烟草幼苗、毛竹笋、大肠杆菌DH5α、农杆菌GV1301、TRIzol Reagent (Invitrogen)、All-in-One First-Strand Synthesis MasterMix (with dsDNase)反转录试剂盒、LA Taq酶、pM19-T载体、凝胶回收试剂盒、质粒提取试剂盒、pCAMBIA2300-35S-eGFP质粒、Kpn I快切酶、琼脂糖、卡那霉素、氨苄青霉素、利福平、农杆菌侵染缓冲液(10 mmol/L MgCl 2、10 mmol/L MES、200 μmol/L乙酰丁香酮)、LB培养基等。
2.3.2. 实验仪器
激光共聚焦显微镜、移液器、离心管、PCR仪、电泳仪及电泳槽、水浴锅、凝胶成像仪、离心机、恒温培养箱、摇床、超净工作台、电子天平、培养皿、烧杯、玻璃棒、PH计、一次性注射器等。
2.4. 方法与步骤
2.4.1. 融合蛋白载体获得
1) 目的基因克隆。使用TRIzol试剂对毛竹笋样品总RNA进行提取,cDNA第一链的合成,根据All-in-One First-Strand Synthesis MasterMix (with dsDNase)试剂盒进行。根据筛选的PheSnRK1.4基因的CDS序列设计克隆全长的引物F:5'-ATGGAGGGAGCCGGCA-3',R:5'-TCAAAGGACTCTCAGCTGAGTTAGA-3'。依照TaKaRa LA-Taq酶的说明书进行基因克隆,体系设置为50 μL。将PCR回收的产物与pMD19-T载体连接,42℃热激90 s转化大肠杆菌DH5α、37℃过夜培养,挑取白色斑点进行菌落PCR。将有目标条带的菌液送Sanger测序,将测序结果比对正确的转化子保存备用。
2) 载体连接。将克隆得到的PheSnRK1.4基因作为模板,根据载体和目的基因序列设计含同源臂的引物F:5'-GTTCATTTCATTTGGAGAGGACAGGATGGAGGGAGCCGGCA-3',R:5'-TCGACTCTAGAGGATCCCCGGGTTCAAAGGACTCTCAGCTGAGTTAGA-3',将PCR产物与pCAMBIA2300-35S-eGFP载体连接。连接亚细胞定位载体时,需要去掉目标基因的终止密码子。参照内切酶说明书(1068S)用KpnI对载体进行酶切,载体通过无缝克隆构建,具体步骤参照CV1021说明书。
3) 转化农杆菌。用质粒提取试剂盒将构建好的含有目标基因与eGFP标签的载体质粒从大肠杆菌中提取出来,通过冻融法转化农杆菌GV1301。
2.4.2. 烟草培养
1) 准备培养土。将蛭石和营养土按照1:1的比例混匀,分装至9 × 9 cm的培养盒中,并使培养土保持足够湿润。2) 播种。在烟草培养间(温度为24℃,光照强度为140 μmol∙photons∙m−2∙s−1,相对湿度为70%,光周期为16 h光照/8 h黑暗)均匀播撒烟草种子于培养土表面,大约需要5~7天即可出芽。3) 移苗。待烟草子叶展开后,用镊子将烟草移至单个9 × 9 cm的培养盒中。大约每隔一周加一次植物营养液。待4~6周左右,烟草即可用于瞬时表达实验(图1)。

Figure 1. Tobacco seedling growth status
图1. 烟草苗生长状态
2.4.3. 农杆菌侵染
将农杆菌(含有目的质粒)接种于10 ML含有相应抗生素的LB液体培养基中,28℃,200~220 rpm培养过夜至OD600 = 0.6~2.0 (OD600为0.8时最佳)。室温下,2800 ×g离心10 min,收集菌体。用烟草注射液(10 mM∙MES, pH 5.6, 10 mM∙MgCl2, 200 μM∙acetosyringone)重悬菌体,并再次于室温下,2800 ×g离心10 min,收集菌体。重悬菌体于烟草注射液中并调整农杆菌OD600至0.8~1。室温静置农杆菌2~4 h。采用1 ML注射器进行烟草注射。浇水保持培养土湿润,并置于弱光条件下培养48 h,以利于蛋白表达。
2.4.4. 激光共聚焦显微镜观察
将已进行农杆菌侵染并在弱光下培养48 h左右的烟草叶片剪下来,用蒸馏水清洗掉叶片上的灰尘,用滤纸吸干表面的水分,并在载玻片上滴一滴蒸馏水,剪一小块注射位点附近的组织,将其反面放在载玻片上制成临时装片,倒置在激光共聚焦显微镜下观察。激光共聚焦显微镜的参数设置为:激发波长448 nm将撕下的烟草表皮将在激光共聚焦显微镜下对eGFP荧光进行拍照。
2.5. 实验结果与分析
在注射含有目的基因的农杆菌后的48 h内,用激光共聚焦显微镜观察注射叶片的荧光信号(图2)。阳性对照是35S::eGFP标签的载体,靠近注射部位组织中观察到大量的荧光信号,距离注射位置越远,荧光信号越弱甚至观察不到荧光信号。荧光信号在单个细胞中显示定位在细胞膜细胞核及细胞质中都有,而目标基因只在细胞质和细胞核中强烈表达。实验结果表明,目的基因已经连上eGFP标签,并且融合蛋白定位在细胞质和细胞核中。
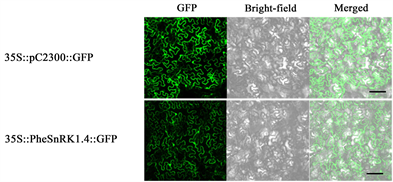
Figure 2. Diagram subcellular localization of PheSnRK1.4
图2. PheSnRK1.4的亚细胞定位
2.6. 注意事项
1) 本生烟草的生长周期不宜过长,培养3~4周左右即可用于烟草的农杆菌侵染,最好不要让烟草开始抽薹后再使用。
2) 移植5~7天后,可将保鲜膜揭去(在晚上揭去,不然苗子会因为湿度变化太大而蔫掉)。托盘中水干掉以后隔2~3天后再加水,长时间让托盘有水的话会长藻类。
3) 农杆菌侵染液的OD 600值在0.8~1.0左右,侵染效率较高。
4) 侵染缓冲液要现配现用,有利于农杆菌的渗透性。
5) 注射不同基因时,要更换新的注射器,避免交叉污染。
2.7. 思考题
1) eGFP显示目标蛋白亚细胞定位的原理是什么?为什么要设置eGFP空载的对照实验?
2) 为什么液氮法可以将目的片段进行农杆菌转化?平板上为什么要添加相应的抗生素?
3) 如果本生烟草已经抽薹,还能不能进行侵染?为什么?
4) 注射农杆菌时,为什么要在叶子的下表皮进行注射?
5) 为什么48小时左右观察荧光效果最好?时间太长为什么就观察不到荧光信号了?
3. 教学预期效果
与传统的验证性和演示型实验相比,利用GFP融合蛋白进行亚细胞定位的实验具有探究性、综合性,实验过程具有系统性和连续性,是一个小型的完整的科研过程。在整个实验过程中,由学生主导,教师辅助指导,学生的积极性非常高。在参与的过程中,学生需要对自己的实验结果负责和合理安排,每一步实验结果的成败都决定着下一步实验能否顺利开展。如基因克隆和载体连接如果做不好,就无法进行农杆菌转化和侵染,也就不能进行后续的荧光观察。但是,经过实验的失败和自己的努力,最终在激光共聚焦显微镜中观察到绿色的荧光信号时,学生是十分激动和兴奋的。此时的成就感会让学生对生物研究充满好奇和兴趣。经过实验的训练,学生已经掌握了分子生物学研究的基本实验操作,如基因克隆、载体构建、农杆菌转化及侵染,照料温室里的烟草。激光共聚焦显微镜属于大型贵重仪器,一般地方高校因经费限制,无法购置这类仪器,学生在这个实验过程中,可以熟悉仪器并进行独立操作。因此该实验的设置是对学生综合素质的训练,为其以后进行生命科学相关的研究奠定良好的基础。
4. 结语
GFP亚细胞定位技术将目标基因与GFP序列相连产生融合蛋白,在激光共聚焦显微镜下能够观察到绿色荧光,对目标蛋白进行细胞定位,将该实验技术引入到本科实验教学中,有利于学生对实验原理知识的理解和吸收,理论和实践相结合的训练方法,不仅拓展了学生的创新思维和提高学生的科研能力,也为学生今后的长远发展打下良好的基础。
致谢
感谢对本研究提供建议和支持的所有人。
基金项目
乐山师范学院高层次人才引进科研启动项目(RC2023019)。
NOTES
*第一作者。
#通讯作者。