1. 引言
胃溃疡(gastric ulcer, GU)是消化性溃疡(peptic ulcer disease, PUD)的一种,是由于胃黏膜间的平衡失常,使胃酸侵蚀胃部的黏膜肌层(muscularis mucosae),造成发炎、出血、穿孔(perforation)的状况 [1] 。常见GU症状为上腹闷痛(epigastric pain)、心口烧灼感(heart burn)、及钝痛(dull pain)等。胃酸的功用除了帮助蛋白酶分解与吸收矿物质外,亦可抵抗肠胃道受细菌感染;然而过多胃酸分泌会使胃部黏膜屏障失衡,引发GU [2] 。造成胃溃疡的原因,主因多为胃幽门螺旋杆菌(Helicobacter pylori)感染与非类固醇消炎药(non-steroidal anti-inflammatory drugs, NSAIDs)过度使用,次要因素还有不良饮食习惯及心理压力等刺激引起 [3] 。H. pylori会分泌尿素酶(urease),造成胃部pH值上升,因而使胃部细胞增加胃泌素(gastrin)分泌,过多胃酸进而破坏保护胃与十二指肠的黏膜层,引起胃炎反复发作 [4] [5] [6] ;NSAIDs具止痛、解热、抗发炎效果,以阿司匹林(Aspirin)、伊布洛芬(Ibuprofen)、萘普生(Naproxen)最为常见非处方止痛用药 [7] 。NSAIDs的止痛作用机制是通过抑制两种环氧合酶COX-1及COX-2,减少促发炎的前列腺素(prostaglandin, PG)合成,达到缓解疼痛之效果 [8] [9] ;然而PG又可分为前列腺素E1 (PGE1)和前列腺素E2 (PGE2),其中PEG1为胃黏膜保护因子,可抑制胃酸分泌、增加黏膜耐受性及屏障完整性,因此当PGE1受到抑制则使胃壁保护及血液凝集等功能减弱,胃酸增多造成胃不适的副作用严重则引起胃溃疡 [10] 。
鼠李糖乳酸杆菌GKLC1 (Lacticaseibacillus rhamnosus,旧名Lactobacillus rhamnosus)在胃酸耐受性试验中具有80%以上的存活率 [11] ,且已经证实益生菌(probiotics)的潜力,对人体的机能性功效包含肾脏保护、肝脏保护等 [12] [13] 。在先前的一项研究指出,菌株GKLC1可缓解酒精诱发酒精性脂肪肝疾病(alcoholic fatty liver)小鼠的肠胃道损伤 [13] ;因此本研究将进一步探讨鼠李糖乳酸杆菌GKLC1对于胃部保护的作用。分别以临床常见的病原微生物以及NSAIDs引起的胃溃疡探讨益生菌菌株GKLC1的保护效果。
2. 材料与方法
2.1. 鼠李糖乳酸杆菌GKLC1来源与培养
鼠李糖乳酸杆菌(Lacticaseibacillus rhamnosus)菌株GKLC1分离自台湾妇女母奶,并寄存于台湾食品工业发展研究所生物资源中心(Bioresource Collection and Research Center, BCRC, Taiwan),寄存编号为BCRC 910988。试验用菌株GKLC1的制备来自挑取单一菌落培养于MRS肉汤培养基(BD, USA)中,经37℃、16小时活化培养2次后,接种3 ml于5 L发酵槽(发酵体积3 L)中,以37℃、16小时培养。量化培养后之发酵液以13,000 rpm于4℃离心10分钟,收取上清液以121℃热处理3分钟,供体外试验用。另外收取上述离心之菌泥(pellet),并混入5%脱脂奶粉,经冷冻干燥后取得菌株GKLC1粉末样品。每克粉末含有活菌数1 × 1011 CFU (conloy forming unit),并保存于4℃供动物试验使用。
2.2. 胃幽门螺旋杆菌来源与培养
胃幽门螺旋杆菌(Helicobacter pylori)菌株26695 (ATCC 700392)、v633、v1354皆由台湾长庚大学(Chang Gung University, Taiwan)赖志河老师提供。其中抗药菌株v633、v1354为临床分离株,经证实皆对抗生素甲硝唑(metronidazole)和克拉霉素(clarithromycin)具抗药性 [14] 。H. pylori于37℃、5% CO2与10% O2供给下,48小时培养于含10%羊血之布鲁氏琼脂(Brucella blood agar)平板中。
2.3. 琼脂纸锭扩散试验(Disk Diffusion Test)
将H. pylori悬浮液(1 × 108 CFU/ml)涂抹于10%羊血的M-H培养基平板(Mueller Hinton agar plates, BBL, Sparks, Maryland, USA)上,并于平板中央放上灭菌纸锭,随后于纸锭上加入测试之菌株GKLC1发酵上清液。平板于37℃、微需氧环境下,培养72小时后,观察抑制圈(inhibition zone)大小,并以直径(mm)纪录之。试验以未接菌的MRS肉汤培养基为空白对照组(control);L. rhamnosus GG (ATCC 53103)为阳性对照组(positive control)。
2.4. 试验动物
试验动物使用8周龄SPF级ICR雄鼠共25只,购自乐斯科生物科技股份公司(BioLASCO Taiwan Co. Ltd., Taiwan),小鼠进驻后皆先行观察5天,确认无任何异状后,才进行试验分组与试验执行。动物房条件控制在温度23℃ ± 2℃、湿度55% ± 5%、以及光/暗周期12 h/12h。饲料及逆渗透水均任由小鼠自由取用。本试验之试验小鼠经台湾农业科技研究院(Agriculture Technology Research Institute, ATRI)之实验动物照护及使用委员会(Institutional Animal Care and Use Committee, IACUC)审查同意,取得IACUC号码110075。
2.5. NSAIDs引起GU之试验设计
以随机方式分为5组,每组5只小鼠,分别为正常对照组(Normal control, Normal)、负对照组(Gastric ulcer, GU)、奥美拉唑组(Omeprazole)及2组益生菌实验组GKLC1-L、GKLC1-H组。试验时,Normal组、GU组每日管喂投予饮用水;Omeprazole组每日管喂投予10 mg/kg胃溃疡临床治疗用药奥美拉唑(Omeprazole);实验组GKLC1-L、GKLC1-H组每日管喂投予益生菌GKLC1粉末,投予剂量分别为5.12 mg/kg/day及20.4 mg/kg/day。给予Omeprazole或益生菌28天后,除Normal组外,各组皆于第29天连续10天每日管喂阿司匹林(Aspirin) 500 mg/kg诱发胃溃疡,于第40天牺牲,观察小鼠的胃部溃疡情形及组织病理变化。
2.6. GU胃部状态分析
利用Image J软件圈选胃部组织的溃疡病灶,以计算每只小鼠的胃部溃疡灶面积(mm2)。另外,依据溃疡面积的分级加成评分(表1),计算溃疡指数(Ulcer index, UI) (1)及治愈率(Curative ratio) (2)。
(1)
(2)
2.7. GU組織病理分析
小鼠胃部组织以Hematoxylin & Eosin (H & E)染色,于光学显微镜下观察黏膜溃疡深度、黏膜溃疡区域、炎症细胞浸润、以及黏膜上皮再生情形。病理程度分级判定标准如表2,参考Shackleford等人(2002)与Schafer等人(2018)发表文献内的判定标准 [15] [16] 。

Table 2. Grading of gastric ulcer tissue lesions
表2. 胃溃疡组织病变程度分级
2.8. 统计分析
本试验所得数据以平均值 ± 标准偏差(mean ± SD)表示,使用Graphpad Prism 6统计分析软件,进行one-way analysis of variance (one-way ANOVA)分析,以p < 0.05具有统计上的显著性差异。在病理结果统计上,比较各组别间组织病变严重度则以Kruskal-Wallis test的Uncorrected Dunn’s事后检定。
3. 结果
3.1. 菌株GKLC1对于H. pylori的抑制效果
L. rhamnosus GG不论是对标准病源株H. pylori 26695,抑或是抗药菌株v633、v1354,皆可观察到明显的抑制圈,抑制效果分别为8.0 ± 0.0 mm、9.5 ± 0.7 mm、以及8.3 ± 1.1 mm (表3);而空白对照组(MRS)在三种不同的H. pylori抗菌测试上均无观察到抑制圈(1.0 ± 0.0 mm)。益生菌菌株GKLC1的对标准病源株H. pylori 26695并无抑制效果,另外测试抗药菌株v633、v1354也无明显抑制圈(图1)。

Table 3. Inhibition zone (mm) of L. rhamnosus against different H. pylori strains
表3. L. rhamnosus对不同H. pylori菌株的抑制圈(mm)
数据(n = 3)以mean ± SD呈现。
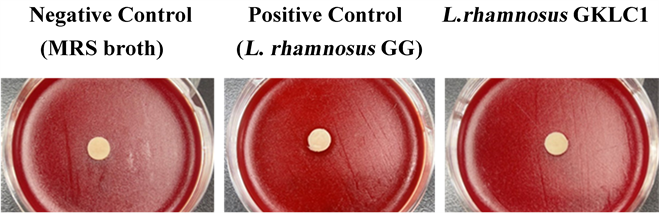
Figure 1. The inhibition effect of strain GKLC1 on H. pylori 26695
图1. 菌株GKLC1对H. pylori 26695的抑制效果
3.2. 菌株GKLC1对NSAIDs引起的GU
3.2.1. GU小鼠胃溃疡面积
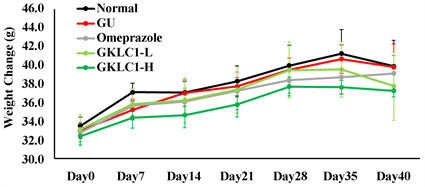
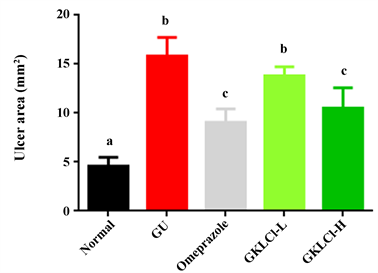
试验期间,所有小鼠体重变化皆无组间统计差异(图2)。投予阿司匹林10天之GU组胃部观测到溃疡面积为15.83 ± 1.91 mm2;而预先喂食28天之Omeprazole组可观测到GU的面积为9.05 ± 1.37 mm2。菌株GKLC1亦有减少胃溃疡面积的趋势,其中以高剂量效果显著改善(p < 0.01),观测到GU面积为10.51 ± 2.07 mm2 (图3)。
 数据(n = 5)以mean ± SD呈现。
数据(n = 5)以mean ± SD呈现。
Figure 2. Body weight change (g) in GU mice model
图2. GU小鼠模式中的体重变化(g)
 数据(n = 5)以mean ± SD呈现。不同字母表示具显着差异。
数据(n = 5)以mean ± SD呈现。不同字母表示具显着差异。
Figure 3. Area of gastric ulcer (mm2) in mice
图3. 小鼠胃溃疡面积(mm2)
3.2.2. GU小鼠胃溃疡指数与治愈率
表4为依据溃疡面积的分级所计算出的胃部溃疡指数与治愈率。菌株GKLC1随介入的剂量提高,胃部溃疡指数显著降低,尤其高剂量的菌株GKLC1以20.4 mg/kg/day摄入对胃部保护的效果接近于摄入10 mg/kg/day的Omeprazole。以治愈率来分析,菌株GKLC1高剂量(20.4 mg/kg/day)下的治愈率比低剂量(5.12 mg/kg/day)的菌株GKLC1治愈效果约多3倍,可达49%以上。

Table 4. Ulcer index and curative ratio
表4. 胃部溃疡指数(UI)与治愈率
数据(n = 5)以mean ± SD呈现。不同字母表示具显着差异。
3.3. NSAIDs引起的GU胃部病理分析
GU小鼠胃组织病理切片结果如图4所示。Normal组的小鼠胃黏膜上皮完整,腺体紧密排列,形状大小正常,无发生胃黏膜溃疡、炎症细胞浸润与黏膜上皮再生等病变现象;而GU组在黏膜上皮细胞结构紊乱且有坏死情形(图4红色星号处),胃组织病变程度最严重;在GKLC1-L组中,仍有观察到腺体排列紊乱及炎症细胞浸润情形;Omeprazole组、GKLC1-H组的腺体排列则与Normal组相近,且可观察到GKLC1-H组的胃部切片仍维持胃黏膜上皮完整性,Omeprazole组则在黏膜下层偏薄稍不平整。
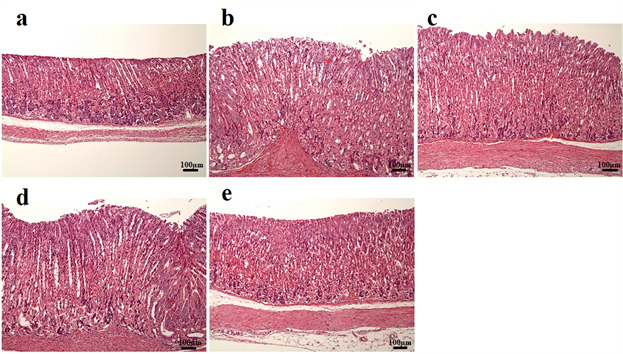
Figure 4. Morphological changes in gastric tissue of GU mice; (a) Normal; (b) Gastric ulcer (GU); (c) Omeprazole; (d) Low dose of strain GKLC1 (GKLC1-L); (e) High dose of strain GKLC1 (GKLC1-H). H & E staining, 100× magnification. (Red asterisk: area of degeneration and necrosis of mucosal epithelial cells)
图4. GU小鼠的胃组织型态学变化;(a) 正常对照组(Normal);(b) 胃溃疡组(GU);(c) 奥拉美挫组(Omeprazole);(d) GKLC1-L组;(e) GKLC1-H组。H & E染色,放大倍率100倍。(红色星号:黏膜上皮细胞变性坏死区域)
依小鼠的黏膜溃疡深度、黏膜溃疡区域、炎症细胞浸润、以及黏膜上皮再生共四项指标进行评分,结果如表5所示。相较于GU组,Omeprazole与菌株GKLC1皆可显著降低黏膜溃疡深(p < 0.001),且低剂量(5.12 mg/kg/day)的菌株GKLC1即可有效减少胃黏膜溃疡的组织面积(p < 0.001)。针对胃组织炎症细胞浸润、以及黏膜上皮细胞再生的状况,菌株GKLC1亦有减缓的趋势,即使尚未有统计显差。
数据(n = 4)以mean ± SD呈现。不同字母表示具显着差异。
4. 讨论
排除消化道病变严重需要施行手术之外,消化性溃疡大多系经由药物治疗,透过减少或中和胃酸分泌、增加消化道屏障以达治愈目的 [17] 。Omeprazole为氢离子帮浦阻断剂(proton pump inhibitors, PPIs),可在胃的壁细胞转变成活化态,绑定氢/钾三磷酸腺苷酶(H+/K+-ATPase),减少胃酸分泌,进而减少溃疡发生、加速胃壁愈合,因此已广泛使用在治疗胃食道逆流(gastroesophageal reflux)、PUD等胃部疾病 [18] 。然而其缺点除了药价贵以外,长期使用可能造成无胃酸症(hypochlorhydria)的副作用,当无胃酸屏障时,胃部受感染的机会提升;此外PPI经肝脏代谢,对于合并肝病的患者是一负担;近期亦有其他研究指出PPIs可增加骨折、低血镁症(hypomagnesemia)、以及肾损伤等风险 [19] 。
益生菌可藉由不同方式保护肠胃道,因此不像PPIs仅针对胃酸分泌做调控,更是以生理系统性调控的方式改善胃部机能 [20] 。例如嗜酸乳杆菌(L. acidophilus)能透过减少发炎物质COX-2与TNF-α,并抑制NF-ĸB讯息传递,改善胃发炎 [21] ;植物乳杆菌(L. plantarum) 299v可刺激MUC3基因分泌黏液素,保护胃黏膜并减少病原菌附着 [22] ;L. rhamnosus GG对胃黏膜及肠道定殖力佳,可透过调控表皮生长因子(epidermal growth factor, EGF)及血管内皮生长因子(vascular endothelial growth factor, VEGF),减弱细胞凋亡与细胞增值比率、增加血管生成提升胃壁愈合能力,减少溃疡复发率 [23] 。
本试验以常见H. pylori感染以及NSAIDs诱因胃溃疡探讨L. rhamnosus GKLC1对于胃部保护的效果。针对H. pylori感染诱因,主要根治方式是抑制H. pylori的过度繁殖,以及强化胃部结构。然而,菌株GKLC1的分泌物对于常见H. pylori标准病原菌株并无抑制效果(图1)。另外,若是因H. pylori感染,临床上通常藉由合并使用特定抗生素来做治疗,而过度依赖抗生素使H. pylori抗药性产生,杀菌不完全又使H. pylori处于潜伏状态,以致治疗失败率增加 [24] 。因此我们亦测试菌株GKLC1对于临床H. pylori抗药性分离株的抗菌效果,结果亦无观测到抑菌圈(表3),说明菌株针对微生物感染引起之GU较无效果。
胃溃疡诱因比例以NSAIDs诱因较H. pylori感染诱因高,尤其在已开发国家中 [25] [26] 。我们透过Aspirin的慢性给予方式促使胃溃疡在小鼠模式中发生。在胃溃疡最直观的指标中,观察到菌株GKLC1对于减缓溃疡面积有显著效果(图3、表4)。进一步地,针对菌株GKLC1对胃组织保护作用以减少溃疡深度、降低炎症细胞浸润为主(表5),因此推估菌株GKLC1在NSAIDs诱因下的胃溃疡具抗发炎、降低细胞凋亡的机制。此抗炎机制可能与前述文献提到的L. acidophilus抑制NF-ĸB讯息传递类似,而预防胃细胞凋亡可能与Bax/Caspase-3讯息传递有关,尚须更进一步的实验验证 [12] [21] 。
5. 结论
本试验以常见胃溃疡诱因探讨Lacticaseibacillus rhamnosus GKLC1对于胃部保护的效果。结果显示菌株GKLC1对胃幽门螺旋杆菌引起的胃溃疡较无保护的效果,然而针对非类固醇消炎药引起的胃溃疡则有显著护胃的功效。此外,在小鼠施予益生菌GKLC1高剂量(20.4 mg/kg/day)下,其NSAIDs的胃溃疡治愈效果相当于市售常见胃药Omeprazole (10 mg/kg/day)。本篇经实验证实护胃的机能益生菌与其适应症,未来可考虑应用菌株GKLC1以保健预防方式,减少因NSAIDs引起胃溃疡的族群,或以合并治疗方式针对NSAIDs引起的胃溃疡做处置,进而降低常见胃药使用所带来的副作用。
NOTES
*通讯作者。