摘要:
目的:采用问卷调查的方式对参加GCP培训的学员进行培训效果调研,通过对问卷结果进行收集和整理,分析GCP培训中的教学不足和学员知识掌握的薄弱环节。方法:利用Excel和GraphPad Prism5.0对问卷调查结果的正确率、分数分布等结果进行整理和分析。结果:本次问卷调查共计回收491份问卷,其中有效问卷487份,有效问卷率99.18%。487份问卷中,有87.89%的学员问卷得分在80分以上,仅有2.05%的学员问卷得分不及格。此次培训总体效果良好,但仍存在部分知识点薄弱环节,后期我们将通过优化课程设计,丰富培训形式等措施增加培训的实践性以及互动性,从而进一步提升培训效果。结论:举办相关培训可以有效提高GCP从业人员的理论水平与实践能力,促进GCP事业发展。
Abstract:
AIM: Questionnaire survey was used to investigate the training effects of the students who participated in the GCP training. Through collecting and sorting out the questionnaire results, the weak links in the teaching and students’ knowledge mastery in the GCP training were analyzed. METHODS: Excel and GraphPad Prism5.0 were used to analyze the accuracy of the questionnaire results, score distribution and other results. RESULTS: A total of 491 questionnaires were collected, including 487 valid questionnaires, and the valid questionnaire rate was 99.18%. Among the 487 questionnaires, 87.89% of the students scored above 80 points, and only 2.05% of the students failed the questionnaire. Our results showed that the GCP training could substantially improve the quality of personnel of students, whereas there were still some weak links in the knowledge points. Therefore, the course design and training forms should be optimized to increase the practicality and interactivity of the training. CONCLUSION: Relevant training can effectively improve the theo-retical level and practical ability of GCP practitioners, and promote the development of GCP career.
1. 引言
随着我国健康产业的不断发展,全国药物临床试验事业也迅速扩大。为进一步加强临床药物试验的管理,规范药物临床试验的开展,国家药品监督管理总局与国家卫生健康委员会于2020年4月26日联合颁布新版《药物临床试验质量管理规范》(Good clinical practice, GCP),并宣布新版GCP将于2020年7月1日起正式施行 [1] [2]。相比既往版本,新版GCP在总体框架和章节内容上均做出较大调整,对药物临床试验的开展提出了更高的要求 [3]。新版GCP中进一步对临床试验实施的相关人员的资质提出要求,规定指出:相关人员必须具备的临床试验所需的专业知识、培训经验和项目实施能力。为配合新版GCP的颁布与施行,加强临床试验从业相关人员对GCP知识的掌握和理解,提高临床试验的管理和实施水平,贵州省药学会药物临床试验专业委员会与我院国家药物临床试验机构共同主办贵州省《2021年药物临床试验质量管理规范培训班》,为我省相关从业人员进行系统培训。为深入了解学员的培训效果,我们采用问卷调查的形式对参加此次培训的学员进行GCP知识调查。本研究通过收集和整理问卷调查结果,对问卷相关数据进行统计分析,并根据分析结果提出相应改进措施,为之后更好地开展GCP培训工作提供参考依据。
2. 材料与方法
研究对象:本次问卷收集以参加2021年5月贵州医科大学附属医院国家药物临床试验机构举办的GCP培训学员为对象(共计498人),其职业类型包括:临床医学、护理、医技、科学研究/临床试验管理人员、临床协调员和监查员等。
调查方法:采用自制的电子问卷进行调查,调查对象通过微信实时扫码参与问卷调查。此次问卷调查共回收491份,其中有效问卷487份,有效问卷率99.18%。问卷的基本调查内容包括:姓名、职业、工作单位等基本信息。问卷的专业知识调查内容共有18道单选题及2道多选题(每题5分,问卷总计100分,其中多选题多选或少选均不得分),涉及到药物临床试验相关术语及定义、药物临床试验中研究者职责、知情同意的过程和要素、安全性事件的记录和报告、质量控制以及药物临床试验中人类遗传资源的管理等方面。本调查问卷所有题均为必答题,全部完成后方可提交问卷。
统计学方法:应用Excel和GraphPad Prism5.0软件进行问卷调查结果的正确率、分数分布等结果的数据导入和分析,利用频数及百分比对调查结果进行统计描述。
3. 结果
3.1. 基本情况
参与此次考核答题的487名学员均为来自贵州省各地区的卫生健康事业相关从业人员,其中临床医学专业326人,占66.9%。此次参加培训的临床医学从业人员中排名前五的专业为:神经内科、血液科、肿瘤科、儿科和精神科(见表1)。此外,参加此次培训的护理人员有62人,占培训总人数的12.7%。这表明研究护士在临床研究中的参与度以及自身学习意识在不断加强。本次培训主要从项目立项、研究者职责、知情同意、AE/SAE的记录及报告、人类遗传资源的管理以及GCP学术论文发表等方面开展临床试验实施实践性较强的培训。培训结束后针对培训内容进行了考核问卷的发放,问卷回收情况显示:87.89%的学员问卷得分在80分以上,2.05%的学员问卷得分不及格(见图1)。这表明大部分学员对于相关培训知识点的掌握情况较佳,同时这也从侧面反映此次培训的效果较好。

Table 1. The professional distribution of participants in this training
表1. 参加培训的学员专业分布情况
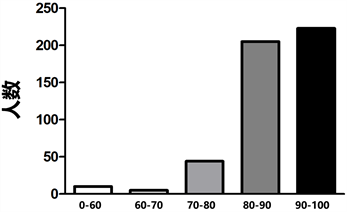
Figure 1. The score distribution of questionnaire
图1. 问卷答题的成绩分布图
3.2. 知识点掌握相对薄弱的原因分析
通过对问卷的答题情况进行分析,我们的结果显示大部分学员的答题情况较好,答题时间也较为迅速(平均答题时间为7.26 ± 5.20分钟)。但部分学员对于部分知识点的掌握仍相对较弱,答题正确率不高,例如:特殊人群知情同意过程、临床试验相关术语和定义以及临床试验全流程等。我们将针对上述几个薄弱内容进行分析,讨论学员对相关知识点掌握不理想可能的原因,为后续GCP培训提供帮助。
3.2.1. 特殊人群的知情同意过程掌握不佳
本次培训学员在“无民事行为能力的受试者,其知情同意过程不涉及的内容”一题中错误率较高,其答题正确率仅为65.50%,这反映出学员对于特殊人群的知情同意的知识要点把握不佳。新版《药物临床试验质量管理规范》中对于研究者应如何实施知情同意有详细规定,例如:研究者在面向缺乏阅读能力的受试者、无民事行为能力的受试者及儿童受试者进行知情同意时应注意的关键点。本次培训过程中,我们的培训讲师也通过实例分享的形式对以上各类情况进行了详细讲解,并分享本机构对特殊人群知情同意的标准操作程序。我们分析学员的答题正确率偏低可能原因为:学员自身专业能力水平以及项目实践经验不同,部分学员自身对于特殊人群知情同意过程较陌生,实际操作经验不足,无法快速掌握操作过程中应注意的要点事项。
3.2.2. 药物临床试验相关术语及其定义
本次培训针对药物临床试验当中相关的术语及其定义做了充分培训和解读,但学员就关于临床试验的定义答题的正确率仅为63.1%,而关于药物不良反应的定义问题答题正确率仅有33.88%。我们进一步的分析结果表明:学员容易将药物不良反应和不良事件混淆。新版《药物临床试验质量管理规范》中临床试验的定义为:以人体(患者或健康受试者)为对象的试验,意在发现或验证某种试验药物的临床医学、药理学以及其他药效学作用、不良反应、或者试验药物的吸收、分布、代谢和排泄,以确定药物的疗效与安全性的系统性试验;药物不良反应的定义为:临床试验中发生的任何与试验用品可能有关的对人体有害或者非期望的反应。试验用药品与不良事件之间的因果关系至少有一个合理的可能性,即不能排除相关性。而不良事件的定义为:受试者接受试验用药品后出现的所有不良医学事件,可以表现为症状体征、疾病或者实验室检查异常,但不一定与试验用药品有因果关系。正确及准确的理解药物临床试验当中相关术语及其定义,是确保药物临床试验规范开展的重要和必备前提,我们也将在后续的培训中进一步加强相关内容的教育。
3.2.3. 临床试验全流程理解不清晰
本次调查结果还发现,大部分学员对于药物临床试验开展的全过程掌握情况不佳。早在2003年颁布的《药物临床试验质量管理规范》的总则中第二条就明确指出:临床试验的全过程包括方案设计、组织实施、监查、稽查、记录、分析、总结和报告。而2020年颁布的新版《药物临床试验管理规范》中也保留了这一定义。经过对各选项答题情况进行分析,我们发现学员容易误选的答案为:方案设计、批准、组织实施、监查、稽查、记录、分析、总结和报告(约占52.57%)。这也说明学员对于临床试验全流程中的组织实施过程理解不足。
4. 讨论
随着我国生物医药技术的不断发展,药物临床试验的机构数量增多,各机构对于GCP相关知识的培训需求也在不断增加 [4]。新版GCP的总则部分的第六条以及第四章研究者部分的第十六条中均指出,所有参与临床试验实施的人员都应该具备临床试验开展所需的专业知识、培训经验以及能力。同时,临床试验实施人员的专业程度以及工作能力、对相关法规的掌握程度都将直接决定临床试验的质量 [5]。此外,《药物临床试验机构资格认定复核检查标准》中也对临床试验相关从业人员的培训经验(研究医生、研究护士、协调研究者、药物管理员等)有一定的资质要求,如:必须经过规范、系统的GCP及相关法规、药物临床试验技术培训等 [6]。因此,针对药物临床试验从业人员进行高质量的培训十分必要。本次培训中临床医学从业人员中排名前五的专业为:神经内科、血液科、肿瘤科、儿科和精神科,这在一定程度上反映出贵州省内药物临床试验的热门方向。这提示我们后续可以根据专业不同举办针对性更强的培训,进一步满足药物临床试验专业从业人员不断学习的需求 [7] [8]。
通过对本次培训进行问卷调查,我们发现了培训过程中的不足,并对后续GCP培训的开展提出如下建议:
1) 收集存在的问题,“对症”培训:不同的专业背景、学历背景的学员在临床研究实施过程中所承担的角色不一样,其实际操作中所遇到的问题也不一致。培训前期,可以通过问卷调查收集学员在专业知识和操作过程中存在的疑问,通过对问题进行归纳梳理,分版块进行授课培训或者经验交流 [9] [10]。这种有针对性的培训更能提高学员的积极性以及学习成就感,进而能获得更好的培训效果。
2) 理论与实践相结合,丰富培训形式及内容:我们的培训在保证一定基础的理论知识的同时,可以适当增加实践性课程的培训。进一步利用案例分享的形式,对GCP规范以及相关药物临床试验技术进行深入浅出的讲解,增加培训的实操性。此外,培训形式不应局限于讲座,可以采用案例分享讨论会、临床试验实操经验分享沙龙以及你问我答等以实际问题为导向的互动讨论模式。通过相互的交流讨论体验临床试验中不同角色的研究者的工作内容,学习与受试者交流的沟通技巧,总结实际操作中的经验等。互动讨论既可以增加学员的参与感也能在一定程度上激发学员的自主学习能力,从而达到较为满意的培训效果,也有助于解决临床试验实施中的实际问题。
定期举行优质高效的培训一直是药物临床试验机构的重点工作,随着越来越多的新机构在临床试验管理平台成功备案,通过实践性的GCP培训及医疗机构间的临床试验沟通交流,有利于快速提高临床试验工作者临床试验执行能力,促进临床试验行业发展。通过总结本次培训的效果并进行相应分析,找到需要加强改进的切入点,为今后机构培训工作的开展提供了新的思路和方向。
基金项目
贵州省贵阳市科技局科技计划项目(筑科合同[20151001]社80号)。
NOTES
*共一作者。
#通讯作者。