1. 引言
慢性萎缩性胃炎(chronic atrophyic gastritis, CAG)是目前临床环境中常见的一种疾病,是以多种治病因素造成的胃粘膜层变薄、腺体萎缩等病理现象为特点的消化系统疾病 [1] 。患者表现主要为上腹胀痛、暧气、贫血以及消化功能障碍等症状 [2] 。患有CAG情况严重者甚至会发展成胃癌,因此这一疾病已被世界卫生组织列为胃癌的癌前疾病 [3] 。在目前的临床诊治中,西医治疗的效果并不能达到理想状态。而中医药具有毒副作用小、适应症广、成本低等特点,日渐被应用于CAG的临床治疗 [4] 。半夏泻心汤是东汉时期著名医家张仲景写于《伤寒论·辨太阳病脉证并治方》中的方剂 [5] 。原方常被用于治疗小柴胡汤证误下所导致的脾胃受损,胃气痞塞,寒热错杂的病症。随着现代分析仪器的不断发展,对半夏泻心汤进行现代药理学的深入探究,发现其含有黄酮、皂苷以及生物碱等多种天然有效产物 [6] ,在胃肠道疾病、内分泌疾病等系统疾病中有着显著的治疗效果。
本研究拟考察对传统名方半夏泻心汤进行加减化裁得到的颗粒剂—夏苍和胃颗粒剂(后文简称“该颗粒剂”)是中医院结合多年临床经验,以半夏泻心汤这一经典方剂为基础开发出的协定处方胃炎颗粒,在治疗包括CAG等各型胃炎胃溃疡疾病中展现出较好的治疗效果。但颗粒剂对治疗CAG的相关作用机制尚不明确,因此本研究拟采用网络药理学以及分子对接技术相结合的手段,对颗粒剂治疗CAG的作用机制进行探讨,为研究该颗粒剂治疗CAG提供可靠依据。
2. 资料与方法
2.1. 颗粒剂主要活性成分筛选及潜在靶点预测
夏苍和胃颗粒剂主要成分包含半夏、苍术、陈皮、党参、佛手、甘草、干姜、厚朴、黄连、黄芩、麦芽、木香、旋覆花13味中药。通过中药系统药理学数据库和分析平台(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform, TCMSP) (https://tcmsp-e.com/tcmsp.php)对这13味中药的化学成分进行检索 [7] ,得到相应的活性成分。再以口服利用度(oral bioavailability, OB) ≥ 30%和药物类药相似性(drug likeness, DL) ≥ 0.18这两个药动学参数作为筛选条件 [8] ,筛选得到颗粒剂的主要活性化合物。继续利用该数据库预测活性成分所对应的潜在靶点,并将所得到的靶标信息通过Uniprot数据库(https://www.uniprot.org/)转化为人类对应的基因名,从而得到颗粒剂有效成分的靶标基因。
2.2. CAG颗粒剂疗法靶点的识别
在GeneCards数据库(http://www.genecards.org/)中将检索关键字设置为“chronic atrophic gastritis”,以此得到CAG的疾病靶点。筛选颗粒剂主要活性成分的作用靶标与CAG疾病靶点取交集,获得颗粒剂治疗CAG的有效靶点。
2.3. “疾病–中药–主要成分–关键靶点(基因)”的网络图构建
在通过取交集得到有效靶点的基础上对颗粒剂的化合成分进行整合筛选,得到包含交集靶点的主要活性成分。向Cytoscape 3.9.1软件中导入共有的有效靶点以及主要活性成分来进行“CAG–颗粒剂–主要成分–关键靶点(基因)”网络图的绘制和构建。并且通过软件内“Tools”中包含的“Network Analyzer”功能进行拓扑分析。
2.4. 筛选共有靶点蛋白互作(PPI)网络分析
将取交集筛选得到有效靶标导入到STRING数据分析平台(http://string-db.org/),在数据分析模式中选择“Multiple proteins”,并将物种限定为“Homo sapiens”,以此获得共有靶点的蛋白与蛋白之间相互作用关系。将上述关系保存为后缀“.tsv”的格式文件导入到Cytoscape 3.9.1软件,绘制构建PPI网络图,并进行可视化处理。通过软件中的“Tools”的“Network Analyzer”功能进行网络拓扑学分析。
2.5. 基因本体(GO)分析和京都基因和基因组百科全书(KEGG)通路富集分析
将颗粒剂治疗CAG有效靶点导入Metascape数据分析平台(https://metascape.org/),限制物种为“H. sapiens”,在设定P < 0.01的基础上开展GO功能富集分析及KEGG通路富集分析。在微生信平台(http://www.bioinformatics.com.cn/)中以数据结果为基础分别开展“富集气泡图”和“BP,CC,MF三合一”柱状图的可视化分析。
2.6. 分子对接验证
在基于“CAG–颗粒剂–主要成分–关键靶点(基因)”网络图中选择Degree值排名靠前的活性成分,并将其导入到PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)来获取有效成分的2D结构的SDF格式文件。使用Chem3D软件对活性成分的结构进行优化处理,以获得能量最低化的对接配体。并且将颗粒剂-CAG的PPI网络分析结果中Degree值前几的关键靶点导入到PDB数据库(https://www.rcsb.org/)来检索蛋白结构。在筛选过程中以“Homo sapiens”为参照物种,且具有配体蛋白的条件来下载分辨率较高的蛋白结构。利用PyMOL软件对蛋白结构进行预处理,包括删除水分子和配体蛋白,以获得对接受体。在此基础上运用Autodock Vina软件开展分子对接验证,并将上述验证结果通过PyMOL软件以可视化的方式呈现。
3. 结果
3.1. 颗粒剂的主要活性成分及颗粒剂——CAG相关靶点分析
利用TCMSP数据库对颗粒剂的组成成分进行了检索,在筛选条件为OB ≥ 30%和DL ≥ 0.18的基础上共得到245种活性成分,包括半夏13种、佛手5种、陈皮5种、木香6种、麦芽18种、黄连14种、甘草92种、旋覆花19种、干姜5种、黄芩36种、厚朴2种、苍术9种、党参21种。其中31种成分未查询到相应的靶标数据。去除重复值后,得到217种活性成分和275个靶点。在GeneCards数据库中得到和CAG相关的致病基因818种。将颗粒剂的靶点与疾病基因进行对比筛选,得到100个交集基因。详见图1。
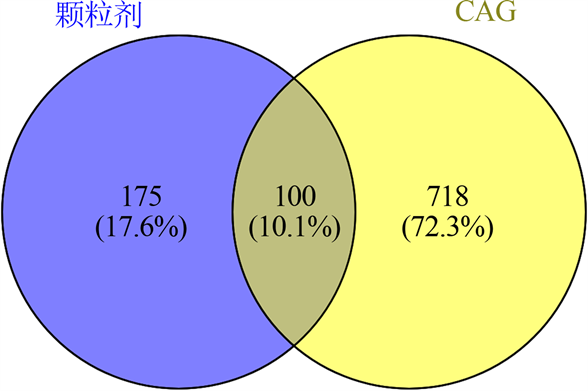
Figure 1. Venn’s diagram of disease gene-herbs target gene
图1. “疾病基因–中药靶标基因”韦恩图
3.2. 构建PPI蛋白互作网络
将颗粒剂与CAG交集基因导入到STRING数据分析平台,进行PPI蛋白相互作用关系的构建。利用Cytoscape 3.9.1软件对PPI图进行构建和美化,详见图2。通过Cytoscape 3.9.1软件进行网络拓扑分析,得到的PPI网络中涵盖100个节点和2212条边。节点的饱和度越高、面积越大,代表该节点Degree数值越高,意味着其在网络中越重要 [9] 。利用Tools工具对Degree数值的大小进行排序,筛选得到互作关系排名前8的蛋白作为关键核心靶点,其升序排序为:环加氧酶2 (PTGS2)、信号传导与转录激活因子3 (STAT3)、半胱氨酸蛋白水解酶3 (CASP3)、血管内皮生长因子A (VEGFA)、肿瘤坏死因子(TNF)、白介素-6 (IL6)、肿瘤蛋白P53 (TP53)、苏氨酸蛋白激酶(AKT1)。
3.3. 构建“疾病–中药–主要成分–关键靶点(基因)”的网络关系
去除颗粒剂中不包含交集基因的化学成分后,筛选得到相关的活性成分202种,其中包括半夏9种、苍术4种、厚朴2种、旋覆花16种、陈皮5种、佛手4种、党参13种、黄连9种、黄芩30种、甘草86种、木香5种、麦芽14种、干姜5种。将相关活性成分、交集靶点、颗粒剂组成成分导入到Cytoscape 3.9.1软件中进行“疾病–中药–主要成分–关键靶点(基因)”网络关系的可视化分析,详见图3。
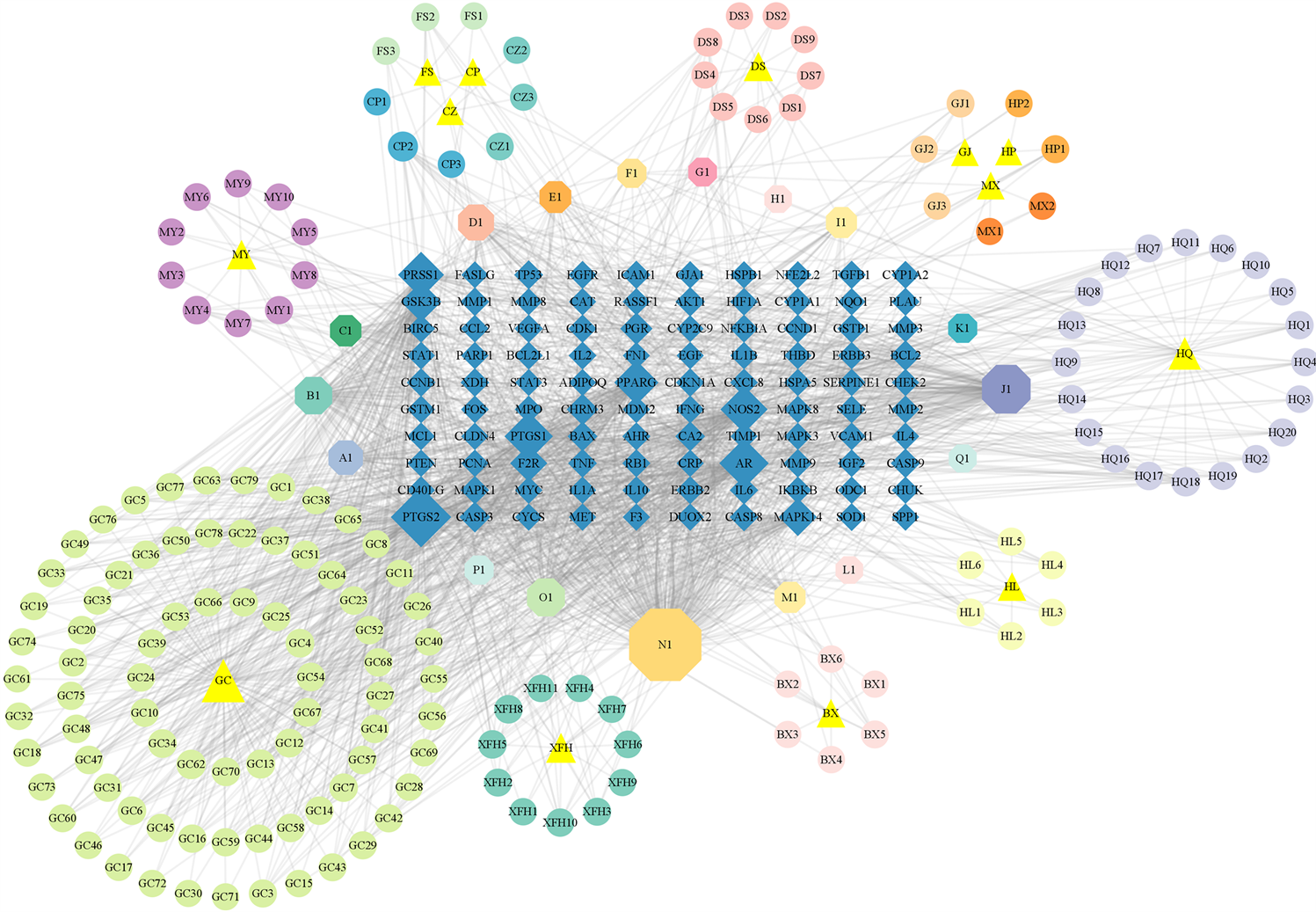
Figure 3. Network diagram of “Disease-Traditional Chinese Medicine-Main Component-Critical Target (Gene)”
图3. “疾病–中药–主要成分–关键靶点(基因)”网络图
3.4. GO功能富集分析结果
通过Metascape平台对100个药物–疾病的交叉靶标进行GO功能富集分析,设置P < 0.01并且限制物种为“H. sapiens”。结果显示,颗粒剂治疗CAG的有效靶点涉及到434条GO注释,其中包括227条与生物学过程(biological process, BP)相关,主要涉及对脂多糖的反应、对辐射的反应、细胞运动正调节以及细胞对压力反应的调控、对外来生物刺激的反应等;122条GO注释与分子功能(molecular function, MF)相关,包括细胞因子活性、DNA-结合转录因子结合、蛋白质同源二聚化活性、激酶结合以及泛素样蛋白连接酶结合;85条GO注释与细胞组成(cellular component, CC)相关,主要包括脂筏、囊泡腔、转录调节复合物以及Bcl-2家族蛋白复合物等。利用微生信平台将显著性排名靠前的条目进行“BP、CC、MF三合一”柱状图的可视化分析,详见图4。
3.5. KEGG通路富集分析结果
在筛选得到的100个交集靶点的基础上,利用Matescape数据分析平台进行KEGG通路富集分析,得到191条相关的信号通路信息。排除疟疾这一疾病通路,发现主要涉及癌症通路、脂质与动脉粥样硬化通路、糖尿病并发症晚期糖基化终末产物及其受体信号通路(AGE-RAGE)、前列腺癌、磷脂酰肌醇–3-羟激酶–蛋白激酶B信号通路(PI3K-Akt signaling pathway)、癌症的转录失调通路(Transcriptional misregulation in cancer)、Janus激酶–信号传导及转录激活因子1信号通路(JAK-STAT signaling pathway)、坏死性凋亡(Necroptosis)、同种异体移植排斥(Allograft rejection)、化学致癌-DNA加合物(Chemical carcinogenesis-DNA adducts)、自然杀伤细胞介导的细胞毒性(Natural killer cell mediated cytotoxicity)、长寿调节通路(Longevity regulating pathway)、核因子-κB (NF-κB)通路(NF-kappa B signaling pathway)、Hippo信号通路(Hippo signaling pathway)、松弛素信号通路(Relaxin signaling pathway)以及5-羟色胺能突触信号通路(Serotonergic synapse)、化学致癌–受体激活通路(Chemical carcinogenesis-receptor activation)等。利用微生信平台根据P值大小,将排名靠前的20个相关条目进行“富集气泡图”的可视化分析,详见图5。
3.6. 分子对接验证

Table 1. Docking binding energy between active ingredient and critical target in granules
表1. 颗粒剂中活性成分与关键靶点对接结合能
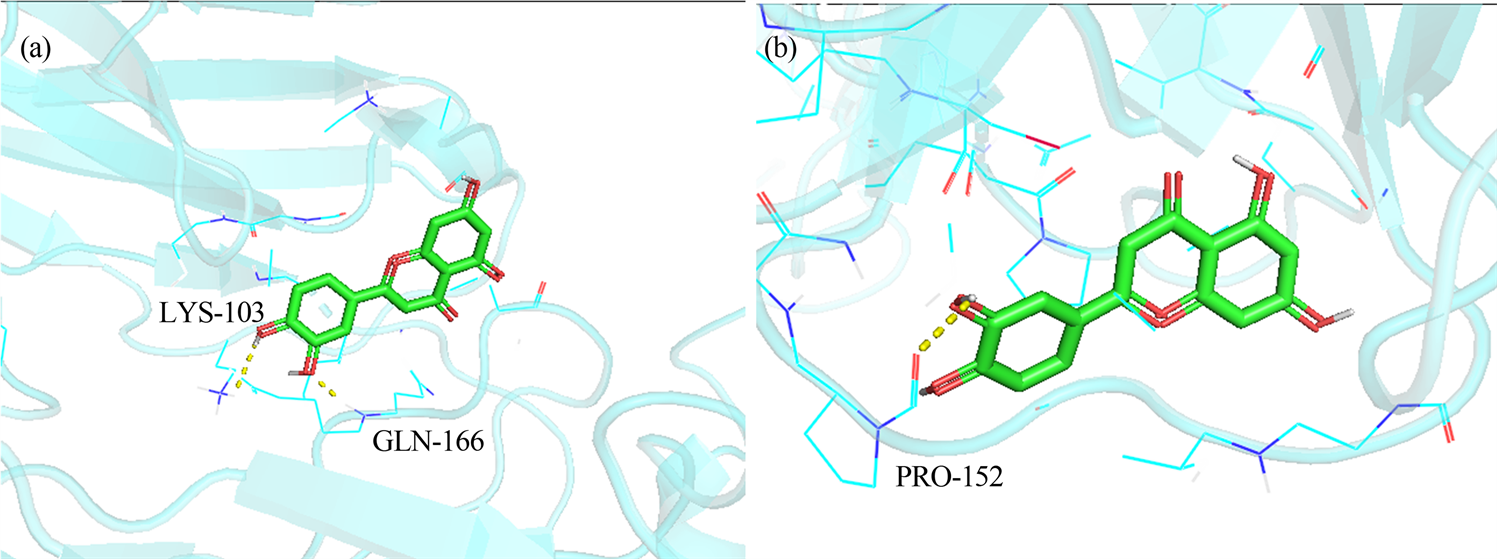
Figure 6. Docking diagram of Luteolin with IL6 and TP53
图6. 木犀草素和IL6、TP53对接图
为了更进一步地探究颗粒剂活性成分与关键靶标之间的相互作用关系,选取“疾病–中药–主要成分–关键靶点(基因)”网络中活性成分Degree值前5位:槲皮素(quercetin)、木犀草素(luteolin)、山柰酚(kaempferol)、β-谷甾醇(beta-sitosterol)、汉黄芩素(wogonin)、黄芩素(Baicalein)以及PPI蛋白互作网络中关键靶点Degree值排名前4的AKT1、TP53、IL6、TNF,采用分子对接技术进行验证。分子对接过程中,在结合能低于0的基础上认为两者能够自发结合。通常情况下,受体与配体相互结合过程中所放出的能量越低,越有可能发生作用,对接的效果越高。当结合能 ≤ −5.0 kcal/mol时,发现两者结合能力良好;当结合能 ≤ −7.0 kcal/mol时,发现配体与受体之间具有较强的结合活性 [10] 。结果表明,木犀草素与TP53、IL6的对接现象表现最佳,详见表1、图6。
4. 讨论
中药复方作为治疗疾病的一种手段,承载“多成分、多途径、多靶点”的协同效应。目前,为了更好地建立合理的中医药整体研究方法、解决中药活性成分不清楚、药物质量难以控制的缺点 [11] ,“网络药理学”这一门新学科伴随着分子生物学、大数据算法等技术的引入和发展应用而生。全面研究中药方剂在治疗疾病时参与作用的相关靶点、化合物和信号通路,对中药方剂分子层面的作用机制做进一步阐释,为现代中药研究的推进提供了新的发展思路、为研究中药复方药物的作用机制提供了方向。在CAG的流行病学研究中发现慢性胃炎患者中有
患有萎缩性病变,其中年龄超过50岁的患者的胃萎缩率可高达50% [12] ,严重情况下甚至会导致胃癌的发生。相对于西医缺乏专门的治疗手段,中医药具有的独特优势包括肝肾损害风险小、复发率低等,已经成为目前治疗CAG的热点 [13] 。
本研究采用网络药理学方法以及分子对接技术进行分析验证,得到汉黄芩素、山奈酚、β-谷甾醇、槲皮素、黄芩素、木犀草素等颗粒剂有效活性成分,作为治疗CAG的物质基础发挥作用。其中槲皮素、木犀草素以及山奈酚等都属于天然黄酮类化合物。在这中间槲皮素作为具有胃保护活性、抗炎、抗肿瘤的活性已被广泛认可,Hu等 [14] 利用化学发光探针观察得到槲皮素通过减弱胃黏膜损伤中活性氧的产生从而降低胃部损伤,发挥了保护胃粘膜的作用。并且耿威等 [15] 通过检测浓度不同的槲皮素组对胃癌细胞的增殖、侵袭情况,发现胃癌细胞增殖能力的下降可能是槲皮素降低了Cav-1的表达。木犀草素具有抗肿瘤、抗病毒等 [16] 药理学作用,研究发现 [17] 其受到JAK/STAT信号通路的调控,进而促使胃癌细胞的凋亡、抑制胃癌细胞增生来发挥治疗作用。山奈酚、汉黄芩素以及黄芩素可以通过多种途径发挥抗肿瘤作用,涵盖抑制肿瘤细胞的增殖、抑制肿瘤的血管形成等 [18] [19] [20] 。β-谷甾醇是一种具有抗菌、抗炎等多种生物功能的四环三萜类化合物,研究表明 [21] 其能够缓解幽门螺旋杆菌感染性胃炎小鼠的胃部炎症状况,对改善胃肠道的健康有帮助。以上成分均属于“疾病–中药–主要成分–关键靶点(基因)”网络的核心活性成分,表明这些活性成分在颗粒剂治疗CAG发挥关键作用。
由PPI蛋白互作网络图以及分子对接验证的结果可知,颗粒剂治疗CAG所涉及到的重要靶点包括AKT1、TP53、IL6、TNF等。其中AKT作为一种1丝氨酸/苏氨酸蛋白激酶在细胞的增值和迁移过程中有着重要地位 [22] ,通过进一步的动物实验观察发现化浊解毒汤中包含的某些组分能够有效抑制CAG中的AKT1的表达,以此来缓解胃癌前病变的严重程度 [23] 。TP53作为一种重要的抑癌基因,有相关研究发现胃癌组织中TP53蛋白的高度表达与其组织分化程度和肿瘤的进展有关 [24] 。IL-6属于一种促炎因子,相关研究表明,升阳益胃汤可以缓解慢性胃炎大鼠胃黏膜的病理性损伤,相关作用机制之一为调控IL-6及其他炎症因子的分泌 [25] 。另外有研究发现半夏泻心汤及有效成分能降低血清中TNF-α水平来缓解胃粘膜的炎症反应,从而保护胃黏膜 [26] 。通过GO功能富集分析图得到颗粒剂主要通过细胞对应激反应的调节、对激素的反应、蛋白质均二聚活性、激酶结合、囊腔、脂筏等生物学过程对CAG产生治疗效果。通过KEGG富集分析得到,颗粒剂治疗CAG主要涉及化学致癌-DNA加合物、癌症通路、Hippo信号通路、前列腺癌、磷脂酰肌醇–3-羟激酶(PI3K)–蛋白激酶B(Akt)信号通路等。其中PI3K-Akt信号通路涉及到细胞的生长繁殖、自噬凋亡等过程,在疾病的发展过程中起到了重要的调控作用 [27] 。
综上,本研究构建了颗粒剂中有效成分集,筛选挖掘出了药物作用于CAG的有效靶点,并且对关键靶标基因进行PPI蛋白相互作用关系的分析以及富集分析,在此基础上进行分子对接验证。分析了对传统名方半夏泻心汤进行加减化裁所制成的颗粒剂治疗CAG作用机制。表明了颗粒剂通过“多种化合物、多个作用靶点、多条信号通路”对CAG产生治疗效果,发挥出了天然药材的优势,为研究该颗粒剂治疗CAG的临床应用提供有效的理论依据。
基金项目
本文由2022年度沈阳市科学技术计划(22-321-33-98)和辽宁大学“大学生创新创业训练计划项目”资助。
NOTES
*第一作者。
#通讯作者。