1. 引言
中药桑螵蛸的来源于螳螂科昆虫巨斧螳螂Hierodula patellifera (Serville)、小刀螂Statilia maculata (Thunberg)、大刀螂Tenodera sinensis Saussure的干燥卵鞘 [1],始载于《神农本草经》,被列为上品 [2]。桑螵蛸具有助阳、补肾、固精、缩尿的功效,常用于治疗遗精、早泄、赤白带下、阳痿、白浊、遗尿、小便频数等疾病 [3],主产于广西、云南、湖北、四川、安徽、甘肃、贵州、湖南、山东、浙江、江苏等地 [4] [5]。桑螵蛸主要含蛋白质、氨基酸、磷脂类、脂肪、糖、粗蛋白、粗纤维、铁钙胡萝卜素样色素、微量元素和宏量元素等成分 [6] [7] [8]。氨基酸是生物维持生命活动的基本组成要素,其中酪氨酸是人体必需氨基酸,在桑螵蛸药材中含量较高;人体中酪氨酸酶催化酪氨酸合成L-多巴,在神精调节、抗氧化、增强皮肤的保护功能方面具有重要的作用,与桑螵蛸的药理作用具有一定的关联性,因此酪氨酸被认为桑螵蛸质量控制成分 [9]。合理的质量标准是规范药材市场、保证药材质量及临床疗效的关键,然而目前桑螵蛸药材的质量研究尚不完善。2020版《中国药典》缺乏浸出物、薄层色谱鉴别等定性定量指标,难以保证桑螵蛸药材的质量。桑螵蛸药材的质量以个大者为佳,浸出物、水分、灰分等是用来评价药材质量优劣的指标之一,水分过多会使药材变质,影响药材的运输和贮藏,灰分和浸出物含量体现了药材的优劣 [10] [11] [12]。薄层色谱法和紫外分光光度法是中药定性鉴别的常用方法之一,具有操作简单、快捷、方便,应用广泛等特点,适用于化学成分复杂的药物的质量控制 [13]。为进一步完善桑螵蛸的质量控制,本实验以桑螵蛸为研究对象,使用性状鉴别法和显微鉴别法观察桑螵蛸的专属性特征,筛选出桑螵蛸最佳的浸出物测定方法,测定其浸出物、水分、总灰分,并采用薄层色谱法和紫外分光光度法分析比较不同产地桑螵蛸的异同,为桑螵蛸的质量研究提供参考。
2. 实验仪器及试药
2.1. 实验仪器
游标卡尺、显微镜(重庆澳浦光电技术有限公司)、盖玻片、载玻片、电热恒温鼓风干燥箱(上海博讯公司GZX-9070MBE)、分析天平(瑞士梅特公司XS205)、数显恒温水浴锅(上海双捷实验设备有限公司DRHH-S8)、电子天平(贵阳东新化工有限公司BM-2200)、打粉机(温岭市林大机械有限公司)、托盘、烧杯、漏斗、蒸发皿、锥形瓶(250 ml)、称量纸、移液管(20 ml、25 ml)、滤纸、冷凝管、量筒、电热恒温鼓风干燥箱(上海博讯公司GZX-9070MBE)、干燥器、扁形称量瓶、马弗炉(长沙市华光电机厂SRJX3-9)、坩埚、电炉、硅胶薄层板(青岛海洋化工有限公司)、超声波清洗机(天津奥泰)、暗箱式紫外分析仪(北京顺科科技有限公司)、点样管(上海长城科学仪器商店经销)、UV-6100S紫外可见分光光度计(上海元析仪器有限公司)、熔融石英比色皿。
2.2. 实验试剂
纯净水(娃哈哈)、无水乙醇(国药集团化学试剂有限公司)、50%乙醇(国药集团化学试剂有限公司)、薄层层析硅胶G粉(青岛海洋化工有限公司)、羧甲基纤维素钠(国药集团化学试剂有限公司)、茚三酮(国药集团化学试剂有限公司)、色谱甲醇(国药集团化学试剂有限公司)、分析甲醇(国药集团化学试剂有限公司)、酪氨酸对照品(如吉生物科技公司)、冰醋酸(上海申博化工有限公司)、三氯甲烷(上海申博化工有限公司)。
2.3. 药材及来源
实验样品购买于贵州省贵阳市太升中药材名品特产市场,产地分别是贵州,四川,甘肃,安徽,经贵州中医药大学药学院钟可副教授鉴定为螳螂科昆虫大刀螂Tenodera sinensis Saussure的干燥卵鞘。将桑螵蛸除去杂质,置于烘箱中60℃干燥,粉碎过2号筛,标记好放干燥容器中备用。
3. 方法
3.1. 性状鉴定
对贵州、四川、甘肃、安徽四个产地的桑螵蛸药材进行长、宽、厚的测量,每个产地随机测量50个药材。
3.2. 显微鉴定
将桑螵蛸药材进行粉碎处理并过60目筛,取桑螵蛸粉末适量于载玻片上,滴加2滴纯净水进行装片,在显微镜下进行观察并拍照记录。
3.3. 浸出物测定
3.3.1. 水溶性浸出物测定
水溶性冷浸法:取中药材桑螵蛸粉末(安徽产)约4 g,精密称定重量,计数值,于250 ml的锥形瓶中,加入100 ml的水密塞好以后开始冷浸,在前面的6小时需要时时振摇,振摇后需静置18个小时,等时间到了以后用漏斗迅速过滤,用移液管量取20 ml的续滤液于已干燥至恒重的蒸发皿中,将蒸发皿放置在水浴锅上进行蒸干,再放入105℃的烘箱内干燥3小时,快速将蒸发皿放在干燥器中冷却30分钟,精密称定重量。计算供试品浸出物含量的百分值(%)。
水溶性热浸法:取中药材桑螵蛸粉末(安徽产)约4 g,精密称定重量,计数值,将称好的药材放入250 ml的锥形瓶中,往锥形瓶中加入100 ml的水,密塞好以后称定重量,将其放好静置1小时,锥形瓶连接回流冷凝管,用水浴锅进行加热并保持微沸1小时。取下锥形瓶,密塞,放冷,再称定重量,对减失的重量用水进行补重并摇匀,用漏斗快速的过滤,用移液管量取25 ml滤液装在已干燥至恒重的蒸发皿中,将蒸发皿放置于水浴锅上蒸干,然后在105℃的烘箱内干燥3小时,迅速的移至干燥器中冷却30分钟,精密称定重量。计算供试品浸出物含量的百分值(%) [14]。
3.3.2. 醇溶性浸出物测定
醇溶性冷浸法:选择乙醇的浓度分别为10%、20%、30%、50%、70%、80%、90%、100%,每种浓度下设三组平行组,其余实验步骤按照3.3.1的冷浸法操作。
醇溶性热浸法:设置乙醇的浓度分别为10%、20%、30%、50%、70%、80%、90%、100%,每种浓度下设三组平行组,其余实验步骤按照3.3.1的热浸法操作。
3.3.3. 浸出物的含量测定
实验所用溶剂为50%乙醇,其余实验步骤按照3.3.1的热浸法操作。
3.4. 桑螵蛸药材水分测定
根据2020版《中国药典》第四部通则0832中的烘干法来测定含水量(%) [14]。
3.5. 总灰分测定
根据2020版《中国药典》第四部通则2302中的总灰分测定法测定总灰分的含量(%) [14]。
3.6. 薄层色谱研究
取不同产地桑螵蛸粉末2 g,加乙醇20 ml,浸泡24 h,超声提取30 min,滤过,滤液蒸干,残渣加甲醇1 ml使溶解,取上清液作为供试品溶液。另取少量酪氨酸作为对照品,加甲醇稀释。根据2020版《中国药典》第四部(通则0502)中的薄层色谱法,吸取上述溶液各2 μl,分别点于同一硅胶G薄层板上,以氯仿–甲醇–冰醋酸–水(10:10:1:2)为展开剂,展开,取出晾干,喷以茚三酮显色剂显色 [13]。
3.7. 紫外分光光度法研究
实验所用溶剂为色谱纯甲醇,其余药材提取步骤按照3.6操作。照紫外–可见分光光度法(通则0401),扫描区间为200~400 nm [13]。
3.8. 数据分析方法
性状鉴别实验的数据处理采用SPSS 26版进行分析,分析的结果以均值 ± 标准差(Mean ± SD)来进行表示。对测量的多个药材数据进行单因素方差分析,若其结果不服从正态分布,数据不满足方差分析的条件时,则对测量的数据进行多个相关样本的非参数检验,运用Friedman秩和检验(M检验),对不同产地的桑螵蛸药材的长、宽、厚进行分析,由分析结果来推断桑螵蛸药材的长、宽、厚与产地分布是否有差异。以浸出物、水分、总灰分的百分含量的平均值,薄层色谱斑点Rf值的差异,紫外分光光度计吸光度的差异,评价不同产地桑螵蛸的质量。
4. 结果
4.1. 性状鉴定
不同品种的桑螵蛸性状差异较大,不同产地的团螵蛸性状相似,结果见表1,图1~6。

Table 1. Characteristics of Mantis egg-case
表1. 桑螵蛸性状鉴别特征

Figure 1. Cross section of Mantis egg-case
图1. 团螵蛸剖面图

Figure 2. Comparison of three kinds of Mantis egg-case
图2. 三种桑螵蛸对比图

Table 2. Difference analysis of characters of Mantis egg-case from different producing areas
表2. 不同产地团螵蛸药材性状差异分析
注:**和*分别表示相关极显著和显著。
从表2可知,团螵蛸药材以安徽产团螵蛸最长为30.10 mm,安徽产团螵蛸最宽为24.28 mm,四川产团螵蛸最厚为21.69 mm。桑螵蛸以个头越大质量越佳,由此可以看出安徽产桑螵蛸药材较其他产地更好。四个产地桑螵蛸药材的长度在27.09 mm~30.10 mm,不同产地桑螵蛸药材的长度有极显著性差异(p < 0.01);四个产地桑螵蛸药材的宽度在22.41 mm~24.28 mm,不同产地桑螵蛸药材的宽度有极显著性差异(p < 0.01);四个产地桑螵蛸药材的厚度在20.59 mm~21.69 mm,不同产地桑螵蛸药材的厚度有显著性差异(p < 0.05)。
4.2. 显微鉴定
团螵蛸的粉末颜色呈浅黄棕色,卵鞘外层碎片的色泽较浅,形状不规则,周边由断续的半圆形空腔环绕(见图7),上面带有少量的枸橼酸钙柱晶(见图8);团螵蛸卵鞘内层碎片是不规则的形状(见图9),有的碎片可见许多类圆形孔腔,缀有大量枸橼酸钙柱晶明显多于外层碎片,且通常排列密集,有的碎片则无类圆形孔腔而有大量的枸橼酸钙柱晶(见图10);卵碎片的形状为类圆形或不规则形,其上有颗粒状物质(见图11)。

Figure 7. Micrographs of outer sheath of Mantis egg-case (4 × 10)
图7. 团螵蛸卵鞘外层显微图(4 × 10)
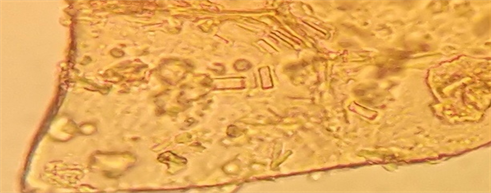
Figure 8. Micrographs of outer sheath of Mantis egg-case-showing calcium citrate columnar crystal (4 ×10)
图8. 团螵蛸卵鞘外层显微图-示枸橼酸钙柱晶(4 × 10)

Figure 9. Micrograph of inner layer fragments sheath of Mantis egg-case (4 × 10)
图9. 团螵蛸卵鞘内层碎片显微图(4 × 10)
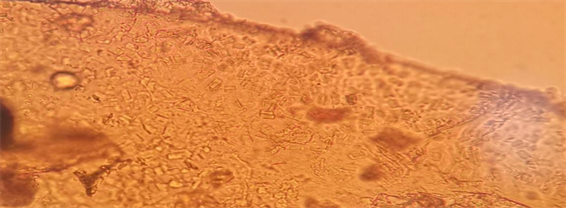
Figure 10. Micrograph of inner layer fragments sheath of Mantis egg-case-showing calcium citrate columnar crystal (4 × 10)
图10. 团螵蛸卵鞘内层碎片显微图-示枸橼酸钙柱晶(4 × 10)
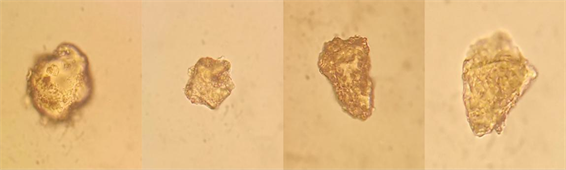
Figure 11. Micrograph of Mantis egg-case-showing egg fragments (10 × 40)
图11. 团螵蛸卵显微图-示卵碎片(10 × 40)
4.3. 浸出物测定
4.3.1. 水溶性浸出物测定

Table 3. Determination results of water-soluble extract by cold leaching method (n = 3)
表3. 水溶性浸出物冷浸法测定结果(n = 3)

Table 4. Determination results of water-soluble extract by hot leaching method (n = 3)
表4. 水溶性浸出物热浸法测定结果(n = 3)
从表3可知,水溶性冷浸法浸出物的含量为9.73%。由表4可知水溶性热浸法浸出物含量为9.24%。因此对于桑螵蛸药材,水溶性浸出物含量测定冷浸法效果较热浸法更佳。
4.3.2. 醇溶性浸出物测定

Table 5. Determination results of alcohol soluble extract by cold leaching method (n = 3)
表5. 醇溶性浸出物冷浸法测定结果(n = 3)

Table 6. Determination results of alcohol soluble extract by hot leaching method (n = 3)
表6. 醇溶性浸出物热浸法测定结果(n = 3)
由表5可知,醇溶性冷浸法浸出物含量最高的提取方法是70%乙醇为溶剂提取,含量为12.42%。由表6可知,醇溶性浸出物热浸法浸出物含量最高的含量最高的提取方法是50%乙醇为溶剂提取,含量为14.37%。因此在醇溶性浸出物测定中,50%乙醇为溶剂的热浸法效果更佳。
根据以上桑螵蛸的水溶性和醇溶性浸出物的测定结果来看,选用热浸法以50%乙醇作为溶剂的浸出物含量,比水溶性冷浸法的浸出物含量更高。因此桑螵蛸浸出物的最佳测定方法为50%乙醇为溶剂的热浸法。
4.3.3. 浸出物的含量测定
表7中浸出物含量测定结果表明,不同产地的桑螵蛸浸出物含量以安徽产最高,为14.27%。浸出物含量以四川产最低,为8.98%。

Table 7. Determination results of Mantis egg-case extract from different producing areas (n = 3)
表7. 不同产地桑螵蛸浸出物测定结果(n = 3)
4.4. 水分测定的含量测定

Table 8. Moisture determination results of Mantis egg-case from different producing areas (n = 3)
表8. 不同产地桑螵蛸水分测定结果(n = 3)
由表8可知,用烘干法测定桑螵蛸水分含量,以安徽产含水量最大,为9.20%,四川产含水量最低,为6.08%。2020版药典规定桑螵蛸药材水分不得超过15.0% [1],以上产地桑螵蛸药材水分均符合标准。
4.5. 总灰分测定的含量测定

Table 9. Determination results of total ash of Mantis egg-case from different producing areas (n = 3)
表9. 不同产地桑螵蛸总灰分测定结果(n = 3)
由表9可知,桑螵蛸总灰分测定中总灰分含量最高的是甘肃产,含量为7.41%;含量最低的是贵州产,为2.91%。2020版药典规定桑螵蛸药材总灰分不得超过8.0% [1],以上产地桑螵蛸药材总灰分均符合标准。
4.6. 薄层色谱法研究
于日光灯下观察,安徽和贵州产地的薄层斑点均有3个荧光,四川产地和甘肃产地的薄层斑点分离度不好,有拖尾现象。在与对照品色谱相应的位置上,显相同的紫红色斑点,结果见图12,表10。
 (S1:酪氨酸对照品;S2:四川产地;S3:甘肃产地;S4:安徽产地;S5:贵州产地)
(S1:酪氨酸对照品;S2:四川产地;S3:甘肃产地;S4:安徽产地;S5:贵州产地)
Figure 12. TLC diagram of Mantis egg-case from different producing areas
图12. 不同产地桑螵蛸TLC图

Table 10. Rf values of Mantis egg-case from different producing areas
表10. 不同产地桑螵蛸的Rf值
4.7. 紫外分光光度法研究
安徽产地的吸收峰在215 nm、222 nm、224 nm,贵州产地的吸收峰在229 nm、213 nm、216 nm、272 nm、340 nm、371 nm,四川产地的吸收峰在210 nm、270 nm、340 nm,甘肃产地的吸收峰在216 nm、228 nm、340 nm、371 nm;四个产地桑螵蛸吸收峰的位置有差异,表明不同产地化学成分的组成略有差异,结果见图13。

Figure 13. UV spectra of Mantis egg-case from different habitats (Red line in the figure: methanol; Blue line: Anhui origin; Green line: Guizhou origin; Yellow line: Sichuan origin; Black line: Gansu origin)
图13. 不同产地桑螵蛸UV图(图中红线:甲醇;蓝线:安徽产地;绿线:贵州产地;黄线:四川产地;黑线:甘肃产地)
5. 结论
四个产地桑螵蛸药材的长度在27.09 mm~30.10 mm,宽度在22.41 mm~24.28 mm,均有极显著性差异(p < 0.01);四个产地桑螵蛸药材的厚度在20.59 mm~21.69 mm,有显著性差异(p < 0.05)。桑螵蛸药材以个头越大,质量越好,团螵蛸药材以安徽产团螵蛸最长为30.10 mm,安徽产团螵蛸最宽为24.28 mm,实验结果表明安徽产桑螵蛸质量较其他产地更佳。团螵蛸粉末浅黄棕色,卵碎片上有颗粒状物质,形状类圆形或不规则形。卵鞘的碎片形状呈不规则形,桑螵蛸卵鞘中含有枸橼酸钙柱晶,而卵鞘内层的枸橼酸钙柱晶较卵鞘外层更多,卵鞘内层枸橼酸钙柱晶常密集,枸橼酸钙柱晶可作为桑螵蛸显微鉴别的指标特征。
本研究考察水溶性热浸法和水溶性冷浸法浸出物的含量,结果表明水溶性冷浸法浸出物的含量(9.73%)比水溶性热浸法浸出物的含量(9.24%)高,因此选择热浸法作为提取方法较好。醇溶性浸出物采用10%、20%、30%、50%、70%、80%、90%、100%乙醇对溶剂进行考察,结果表明冷浸法浸出物含量在8.25%~12.42%,乙醇浓度70%的浸出物含量最高(12.42%);热浸法浸出物含量在9.86%~14.37%,乙醇浓度50%浸出物含量最高(14.37%);醇溶性浸出物测定乙醇浓度50%的热浸法浸出含量比水溶性浸出物冷浸法的浸出含量高,因此对于桑螵蛸药材浸出物含量测定的最佳方法是乙醇浓度为50%的热浸法。测定不同产地桑螵蛸药材浸出物含量,测定结果表明四个产地的桑螵蛸药材浸出物含量在8.98%~14.27%;以安徽产浸出物含量最高,为14.27%;四川产浸出物含量最低,为8.98%。含水量在6.08%~9.20%之间;以安徽产含水量最大,四川产含水量最小。2020版《中国药典》规定桑螵蛸药材水分不得超过15.0%,以上四个产地桑螵蛸药材水分均符合标准。四个产地的桑螵蛸药材总灰分含量在2.91%~7.41%之间,以甘肃产总灰分含量最大,贵州产总灰分含量最低。2020版《中国药典》规定桑螵蛸药材总灰分不得超过8.0%,以上四个产地桑螵蛸药材总灰分均符合药典标准。本文以酪氨酸为对照品,建立了桑螵蛸的薄层色谱法和紫外分光光度法,以酪氨酸为对照品的薄层色谱法可作为中药桑螵蛸的鉴别方法,紫外分光光度法结果显示安徽产地的吸收峰在215 nm、222 nm、224 nm,贵州产地的吸收峰在229 nm、213 nm、216 nm、272 nm、340 nm、371 nm,四川产地的吸收峰在210 nm、270 nm、340 nm,甘肃产地的吸收峰在216 nm、228 nm、340 nm、371 nm,四个产地桑螵蛸吸收峰的位置有差异,表明不同产地化学成分的组成略有差异。
本实验通过对收集到的四个不同产地收集到的桑螵蛸进行性状鉴别、显微鉴别和浸出物、水分、总灰分的测定,并采用薄层色谱法和紫外分光光度法进行定性研究,对不同产地桑螵蛸的质量进行了综合考察,为中药桑螵蛸的质量研究提供参考方法和参考依据。
基金项目
贵州中医药大学药用动物(昆虫类)研究中心平台项目(2019-15)。
NOTES
*通讯作者。