1. 引言
综合化学实验作为一门高年级化学及相关专业的必修实验课程,一方面要求其内容明显有别于模块化的基础化学实验,另一方面又要求实验课程能够帮助高年级学生巩固之前所学的基础知识,同时为学生的实习、毕业设计、工作、升学深造提供一定的帮助 [1] [2]。为充分发挥综合化学实验承上启下的作用,国内部分高校鼓励教师将科研或者产业研究的成果融入实验教学,帮助学生快速的建立科研思维,提升科研能力,为学生今后独立开展工作奠定基础 [3] [4]。
新能源和新材料不仅是化学相关专业研究的重要领域,也是本专业学生就业的热门方向 [5]。无论是升学深造,还是去企业工作,许多学生依旧从事与新能源和新材料相关的研究或工作。综合考虑人才培养目标、学校现有平台和自身研究方向,选择将二硫化钒–生物质衍生的氮掺杂碳复合纳米材料的制备及储锂性能测试简化设计为综合化学实验。实验以生物质明胶为骨架,氯化钠为造孔剂,将二者与偏钒酸铵充分混合,在惰性气氛下先高温煅烧,然后洗涤制备前驱体,后续加入硫脲原位制备二硫化钒–生物质衍生的氮掺杂碳复合材料。之后利用各类大型仪器对复合材料的结构和组成进行表征,将材料制备成电池后通过电化学工作站测试材料的储锂性能。在课程安排方面,综合考虑教学计划、实验内容等因素将实验设计为16个学时,通过该实验使学生能够初步学习开展研究工作的方法和思路,同时对新能源和新材料相关领域有更深入的认识。
2. 实验课程内容
2.1. 实验目的
1) 提升查阅、梳理科研文献及相关资料的能力。
2) 掌握二硫化钒–生物质衍生的氮掺杂碳的制备方法,同时了解相关表征常用的大型仪器。
3) 学会组装电池并使用电化学工作站对其电化学性能进行测试。
4) 能够运用专业软件进行数据处理并撰写科学规范的实验报告。
2.2. 实验原理
二硫化钒(VS2)是一种典型层状材料,其层间距较大,层与层之间的分子间作用力较小,因此锂离子能够在其中快速可逆脱嵌 [6]。二硫化钒纳米粒子作为锂负极材料在理想状态下具有较高容量,但由于其在单独使用时通常会产生严重的团聚现象,使其容量大幅降低 [7]。此外二硫化钒的电子迁移率较低,不利于电子的快速传递。为此,实验从改善团聚、增加材料比表面积及容量、提高电子迁移速率等方向入手,以生物质材料明胶衍生的氮掺杂碳包覆二硫化钒,一方面能够防止二硫化钒的团聚,增大材料的容量和比表面积;同时在复合材料中引入碳元素,提高电子在充放电过程中的转移效率,使复合材料具有更好的电化学性能。
2.3. 实验试剂及仪器
试剂:偏钒酸铵、明胶、硫脲、氯化钠、丙酮、N-甲基-2-吡咯烷酮等均为分析纯。蒸馏水、导电炭黑(super P)、聚偏氟乙烯粘结剂、铜箔。
仪器:X射线粉末衍射仪(Thermo X’TRA)、扫描电子显微镜(SEM,JEOL 7500F)、高分辨率透射电镜(Talos F200X)、X射线光电子能谱仪(Perkin-Elmer PHI5000c)、比表面积测定仪(Quantachrome NOVA 2000e)、冷冻干燥机(北京博医康,FD-1A-50)、管式炉(天津中环,SK-G06123K)、电化学工作站(CHI 760E)、真空手套箱(米开罗那,Super系列)、充放电仪(LAND,CT-2001A)、交流阻抗仪(Gamry Reference 600+)、真空干燥箱、超声波清洗机、冰箱、高速离心机、分析天平、磁力搅拌器、玛瑙研钵等。
2.4. 实验步骤
2.4.1. 二硫化钒–氮掺杂碳复合纳米材料的制备
取1 mmol的偏钒酸铵、0.54 g的明胶和6 g氯化钠溶于30 ml去离子水中,磁力搅拌至溶液完全透明。将上述溶液冷冻干燥,得到混合均匀的前驱体。将前驱体倒入石英舟内,置于充满氮气气氛的管式炉中,氮气的流量为20 mL·min−1,升温速率为5℃·min−1,于600℃高温煅烧2 h,并将煅烧后的样品反复水洗去除氯化钠,真空干燥,得到氧化钒/氮掺杂碳复合纳米材料。
按照质量比为10:1,将硫脲和氧化钒/氮掺杂碳材料分别放入石英舟内,分别置于管式炉的上、下游,氮气的流量为20 mL·min−1,升温速率为5℃·min−1,于300℃硫化2 h即可得到最终产品。为了对比起见,以硫脲和偏钒酸铵为反应物,采用相同的热处理方法制备单纯的二硫化钒样品(VS2)。
2.4.2. 电极的制备和模拟电池的组装
将制备好的活性物质VS2-NC或单纯的VS2、导电剂乙炔黑和粘结剂聚偏氟乙烯(PVDF)按照质量比70:15:15制备电极糊。先将PVDF溶于N-甲基-2-吡咯烷酮(NMP)中,然后依次将乙炔黑和活性物质加入到上述溶液中,充分混合。然后将电极糊均匀的涂覆在直径约1.2 cm的圆形铜箔上,并在100℃的烘箱中烘干4 h,取出后在双滚辊压机上压牢,保证活性物质与集流体的紧密接触。根据铜片的增重计算电极材料的质量,活性物质质量一般在1.0~2.0 mg之间。
模拟电池采用钮扣模拟电池(CR2025)。金属锂箔为对电极和参比电极,隔膜为聚丙烯薄膜(Celgard-2400),电解液为1.0 M LiPF6的EC/DMC溶液(体积比1:1)。将电极片和超声清洗干净的模拟电池在120℃真空干燥箱内干燥12 h,然后转移至充满氩气的手套箱中进行装配。
2.4.3. 储锂性能测试
模拟电池的容量和循环性能测试采用LAND CT-2001A系列电池程控测试仪在室温下进行。充放电电流为100~1000 mA/g,电压截止区间为开路电压3.0 V~0.005 V。循环伏安(Cyclic Voltammogram, CV) 测试在CHI760E电化学工作站(上海辰华有限公司)上进行,电压区间为3.0~0.0 V,扫描速度为0.5~10 mV·s−1。
2.5. 实验结果与讨论
2.5.1. 组成、形貌及结构分析
图1为VS2及VS2-NC的X射线粉末衍射谱图(XRD)。结果表明,VS2及VS2-NC具有类似的衍射峰,二者的衍射峰归属于六方晶系的VS2,与标准卡片(No. 36-1139)一致。此外,与VS2相比,VS2-NC在2θ = ~22˚处有一个突起的宽峰,说明VS2-NC中的碳是无定形的。

Figure 1. XRD patterns of (a) VS2 and (b) VS2-NC
图1. X射线粉末衍射图谱(XRD):(a) VS2;(b) VS2-NC
VS2及VS2-NC的电镜图如图2所示。图2(a)中纯VS2纳米颗粒出现严重的团聚现象,这不利于电解质进入其内部空间。而制备得到的VS2-NC复合材料(图2(b))则含有丰富的连续孔道,具有三维的蜂窝状结构,从图2(c)中可以观察到VS2纳米颗粒均匀分布在碳纳米片表面,图2(d)中的TEM图像清楚地表明,VS2纳米颗粒可以很好地嵌入到分层的碳片中。三维蜂窝状多孔结构有助于缓解VS2纳米颗粒在电化学过程中的体积变化。同时,氮掺杂的碳骨架可以加强充放电过程中电子和离子的传递效率,从而提升复合材料的储锂性能。

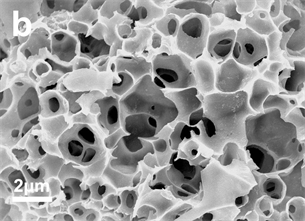

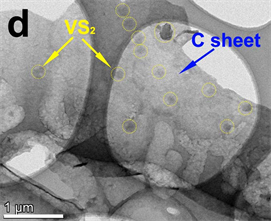
Figure 2. SEM images of (a) VS2; (b) (c) VS2-NC; (d) TEM image of VS2-NC
图2. 扫描电镜(SEM)图:(a) VS2;(b) (c) VS2-NC;透射电镜(TEM)图:(d) VS2-NC
为进一步确定VS2-NC中VS2的含量,采用热重分析法对该复合材料进行研究。从图3中可知,在200℃时,复合材料出现了一个小的质量损失,这是由吸附在材料中的水蒸发引起。随着温度从300℃升高至600℃,由于大量碳元素的氧化,样品产生较大的质量损失。在600℃时,样品中的碳元素完全被氧化,VS2完全转化为V2O5。由于样品在200℃~600℃的质量损失为50.53%,经过换算可知复合材料中的VS2含量为62.52 wt%。
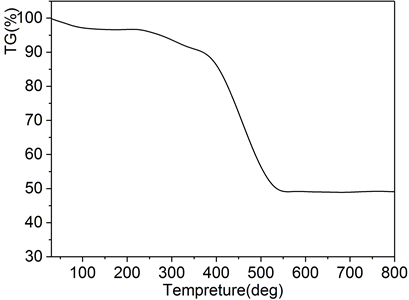
Figure 3. Thermogravimetric profile of VS2-NC
图3. VS2-NC复合材料的热重曲线
通过等温吸附–脱附法测定VS2和VS2-NC的比表面积。由图4(a)和图4(b)可知,两个样品的吸附–脱附曲线均具有典型的IV型等温线特征,在0.6~1.0 (P/P0)的压力范围内可以观察到明显的滞回环,表明了材料中介孔的存在。经测量,VS2-NC复合材料的比表面积约为69.72 m2·g−1,超过VS2 (15.59 m2·g−1)。VS2-NC复合材料具有更大的比表面积,有利于提供丰富的储锂活性中心,降低离子的扩散电阻,从而有效地提高其电化学性能。
2.5.2. 储锂性能分析
图5展示了纯VS2和VS2-NC复合材料的电化学储锂性能。图5(a)是在0.5 mV−1下,进行前三次扫描时VS2-NC电极的循环伏安图。在第一次阴极扫描中可以观察到在1.59 V处有明显的还原峰,这是由于Li插入VS2层间形成插层化合物LixVS2,随着扫描的继续进行,还原峰转移至1.45 V附近。在1.05 V附近出现另外一个还原峰,这个峰主要是由LixVS2转换成V和LixS、电解质分解和生成固体电解质界面(SEI)引起,当循环继续时,这个峰移至0.50 V附近。此外,在小于0.1 V附近的还原峰则与锂离子插入复合材料的碳层有关。第一次阳极扫描中有三个明显的氧化峰,其中1.91 V和2.34 V这两个氧化峰分别对应重新形成LixVS2及Li从LixVS2中脱出的过程。2.73 V的氧化峰则对应LixS被氧化生成硫的过程。在第二次和第三次循环过程中,循环曲线基本重叠,表明锂离子在VS2-NC复合材料中的嵌入与脱出可逆性良好。
通过连续恒电流充放电试验进一步验证纯VS2和VS2-NC复合材料循环稳定性,并对两种样品的比容量和循环性能进行比较。图5(b)表明纯VS2可逆比容量小,循环不稳定,其电化学储锂性能较差。在第一次充放电过程中VS2的放电容量为1191 mAh·g−1,充电容量为869 mAh·g−1,首次库伦效率为73%,随着循环次数的不断增加,其容量大幅度衰减,当循环次数达到100次时,容量仅为110 mAh·g−1。由于复合材料VS2-NC的结构得到改善,因此其可以比容量和循环稳定性均优于纯VS2。在第一次放电过程中VS2-NC的放电容量为1625 mAh·g−1,充电容量为1120 mAh·g−1,虽然首次库伦效率为69%,但在循环3次之后其库伦效率高达94%,且经过100次循环之后还可以保持1061 mAh·g−1的高容量。
图5(c)比较了纯VS2和VS2-NC复合材料的倍率性能。随着电流电流密度的增加,纯VS2的容量大幅度衰减,当电流密度从0.2增加到1.0 A·g−1,纯VS2的可逆容量分别为564、315和149 mAh·g−1。与之相比,VS2-NC电极在高倍率下容量衰减较小。当电流密度从0.2增加到1.0 A·g−1,其可逆容量分别为890、778和636 mAh·g−1。此外,图5(d)显示,在1.0 A·g−1下循环400次后,VS2-NC的容量仍然保持在548 mAh·g−1。
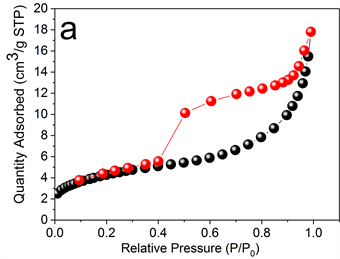
Figure 4. Isothermal adsorption (black)/desorption (red) curves of (a) VS2 and (b) VS2-NC
图4. 等温吸–脱附曲线:(a) VS2;(b) VS2-NC
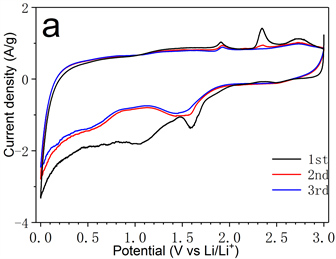

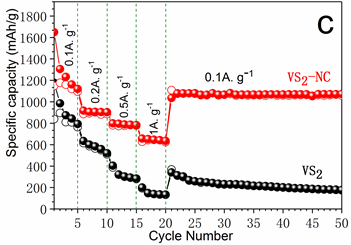
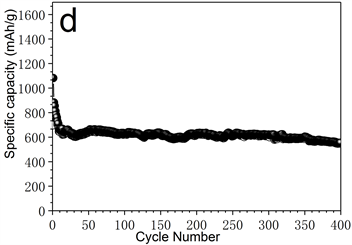
Figure 5. (a) Cyclic voltammograms obtained in the first three cycles with scan rate of 0.5 mV·s−1; (b) Cycle stability test of the two sample electrodes at 100 mA·g−1; (c) Rate capability test of the two sample electrodes; (d) Long-period durable test at 1000 mA·g−1 of VS2-NC electrode
图5. (a) 0.5 mV·s−1下VS2-NC电极前三个循环的循环伏安图;(b) 100 mA·g−1下两个样品的循环性能;(c) 两个样品的倍率性能和(d) 在1000 mA·g−1下VS2-NC的循环性能
为更好的探究复合材料储锂性能的优势,我们对材料的电化学反应动力学进行研究。在图6(a)和图6(b)中,以不同扫描速率获得的CV曲线形状基本相似。电荷在电极中的存储机制可分为扩散控制过程和电容控制过程,这与电极表面的双电层和法拉第过程有关 [8]。
(1)
式(1)用于描述峰值电流密度(i)与扫描速率(v)之间的关系,其中a和b是经验参数。b值决定了电极储锂机制的类型。如果扩散控制过程占主导地位,则b值接近0.5。而在电容控制过程的储锂机制下,b值等于1.0。对于纯VS2电极,图6(c)中其还原峰(R1)和氧化峰(O1)的b值分别是0.55和0.59,证明了其电化学储锂主要是由扩散过程控制。对于VS2-NC电极,还原峰(R2)和氧化峰(O1)的b值分别为0.90和0.84,b值接近1.0,表明其电化学储锂主要是电容控制过程。
(2)
使用式(2)来估计电容贡献的比例,其中k1和k2是一定电位下的参数。k1v值表示由电容控制过程引起的电流,k2v0.5值表示由扩散控制过程诱导产生的电流。图6(d)描述了VS2-NC电极在1.0 mV·s−1扫描速率下的电容对电池容量的贡献为69.23%。如图6(e)和图6(f)随着扫描速率从0.2 mV·s−1上升到1.0 mV·s−1,电容对电池容量贡献逐渐增加,与VS2电极相比,电容过程对VS2-NC电极的容量贡献更大,这主要是因为复合材料具有三维的多孔结构和高表面积以及碳材料的引入。
此外,通过电化学阻抗谱(EIS)可以研究电极内部阻抗。电极的奈奎斯特图及其等效电路图如图7(a)所示,图形由高频区和中频区的两段圆弧和低频区斜线组合而成。在高、中频内的圆弧主要与SEI膜的电阻(Rf)和电荷转移电阻(Rct)有关。根据等效电路图,通过数据模拟计算元件参数可知VS2 Rf和Rct的值分别为222.3、302.7 Ω,而VS2-NC的Rf和Rct为9.15、86.94 Ω。参数结果表明与VS2相比,复合材料VS2-NC具有更低的阻抗,能够加快体系电荷传递,强化电化学反应过程。低频区的斜线与离子扩散阻力(Ws)有关,斜率越大,离子迁移越快。在低频区,VS2-NC的斜率比VS2的大,表明在VS2-NC中锂离子扩散更快,这是由于VS2-NC具有丰富的孔道和较大的比表面积。通常可以通过扩散系数(DLi+)评估电极中锂离子的传输速率,一般认为,DLi+与σ的平方成反比。σ是Warburg系数,可以通过线性拟合Zreal和ω−1/2由拟合直线斜率得出,其中Zreal是阻抗的实部,ω是低频场的角频率。从图7(b)可以看出,VS2的σ为521.41 S−1·s−1/2,VS2-NC的σ为81.52 S−1·s−1/2,因此,VS2-NC的扩散系数是VS2的40倍,进一步证明了锂离子能够在VS2-NC电极中快速扩散。
3. 实验教学流程及建议
课程主要采用小班教学模式,每组人数不超过3人。实验教学流程如下:
实验相关背景介绍(1学时)→复合材料的制备(4学时)→材料表征(3学时)→电池的组装及电化学性能测试(8学时)。
在实验课程开始前,由老师提前介绍实验题目,学生以分组形式完成相关研究背景的调研,采用简短的PPT形式进行汇报。材料制备过程中应着重注意高温仪器的安全操作讲解。材料表征所用的大型仪器原理、操作可由教师提前录制视频,供学生反复学习。电池组装和电化学性能测试阶段,教师着重就电池组装的技巧,电化学测试数据的分析与处理进行讲解,并结合之前大型仪器的表征数据引导学生撰写规范的实验报告。
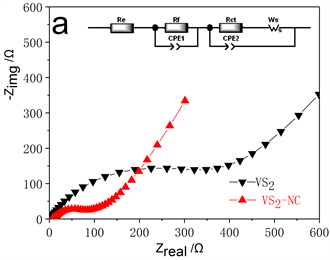
Figure 7. (a) Nyquist plots of bare VS2 and VS2-NC, inset is the circuit model; (b) The fitted straightlines of Zreal and ω−1/2
图7. (a) 样品电极的奈奎斯特图;插图为对应的等效电路;(b) 阻抗的实部Zreal对低频区交流电频率ω−1/2作图拟合的直线
4. 结语
科研型综合化学实验是培养学生创新能力,提升学生实验技能,增强学生学科素养的重要手段。本实验通过将教师科研成果二硫化钒–生物质衍生的氮掺杂碳复合纳米材料的制备和储锂性能测试等相关内容转化成难度适中且操作简单的综合化学实验,实验将复杂的科研实验进行逐步拆解简化,帮助学生初步掌握开展科研工作的方法。此外,实验知识点涵盖无机化学、物理化学、结构化学及仪器分析的相关知识点和实验技能,帮助学生做到“知识–实验–知识”的学习闭环从而提高学生的学科素养。在实验内容方面,选择学生就业和升学深造涉及最多的新能源和新材料方向,使学生对该方向有更深入的了解,为其后续发展提供一定的帮助。
NOTES
*通讯作者。