1. 引言
日益严重的环境污染迫使人们寻找新的解决方法,用来检测环境中痕量的污染物。在众多的有机污染物中,硝基酚(p-NP)因其对人类、动物和植物的毒性作用而引起了人们的极大关注。这些污染物在生产、运输、使用过程中将排放到环境中,包括土壤、湖泊、河流和地下水等。氮氧化物经光化学反应生成硝基苯酚衍生物 [1]。p-NP很容易通过皮肤和粘膜进入体内,对哺乳动物胚胎、脏器均有毒性 [2]。此外,p-NP由于结构稳定,不易降解,因此,寻找有效可靠的方法对环境样品中的p-NP在低浓度水平下进行分析。
传统检测p-NP的方法包括色谱法 [3]、毛细管电泳法 [4]、荧光法 [5] 和分光光度法 [6],但这些通常需要大型的仪器,分析过程冗杂,分析时间长。在这种情况下,电化学分析法由于其便利、可以原位检测和分析快速等各种优点,在p-NP的检测中受到了广泛的关注。Zhou等 [7] 提出了一种电化学传感器用来检测p-NP。合成了(2-羧基甲基)硫代-β-环糊精(AcSCD),并将其修饰金纳米粒子(AcSCD-AuNPs),将AcSCD-AuNPs引入介孔碳上制备了一种新型电极材料用于检测p-NP。结果表明:线性范围为0.1~10 μM和10~350 μM,检测限为3.63 μgmL−1。Chaudhary [8] 报道了通过合成氧化钆纳米粒子,作为一种高效的电催化材料用于p-NP的检测。Anbumannan [9] 制备了一种基于多壁碳纳米管/二氧化锰的纳米复合材料,用于水介质中微量p-NP检测的电化学传感器。其线性范围是30~475 μM,检测限为0.64 μM。
本文选取爆米花作为优质碳源,采用化学活化一步合成多孔生物质碳材料(PCMPC),用于p-NP的测定。利用循环伏安法(CV)等方法研究了PCMPC/GCE的选择性和稳定性。该研究有望用于测定实际水样中的p-NP。
2. 实验部分
2.1. 试剂及仪器
对硝基酚从阿拉丁化学试剂公司购入。其他化学品均为分析级化学品,使用时无需进一步净化。实验用水来自UIUPURE(UPC-I-10T)系统。
实验使用的是上海辰华CHI660E电化学工作站。在室温下(约300 K),在含有10 mL PBS溶液的电解槽中进行。采用传统三电极系统,工作电极为裸或修饰的玻碳电极(上海辰华,d = 3 mm),对电极选取铂丝,参比电极则是饱和甘汞电极(上海雷磁)。用pH-3c数字pH计(上海雷磁)测量缓冲液的pH值。X射线光电子能谱(XPS)在扫描X射线微探针PHI Quantera II (Ulvac-PHI, INC)和C60枪上进行。用X射线衍射仪(XRD, Bruker-D8-advance, Cu kα辐射k = 0.15418 nm)研究其结构。用扫描电子显微镜(SEM, Gemini SEM 300)和透射电子显微镜(TEM, je-2100hr)对其形貌进行表征。
2.2. 修饰电极的制备
焦糖味爆米花购买于当地超市,直接粉碎后过筛。称取一定质量的KOH也用研钵碾碎,按照质量比KOH:C = 1:3的放置在瓷舟中,然后在氮气环境下,管式炉中进行直接碳化。升温速率为4℃ min−1,氮气的流速为15 mL min−1。碳化结束先后用2 M HCI和超纯水清洗3次。然后,室温干燥36 h。将此法得到的材料记作PCMPC,控制不加KOH的对照组记为未活化PCMPC。取1 mg PCMPC超声分散在1 mL DMF中,并在后续实验中确定最优修饰量为4 μL。
依次用1.0,0.3和0.05 μm的氧化铝粉末对玻碳电极进行反复抛光。将4 μL浓度为1 mg mL−1的PCMPC均匀悬液滴到抛光后的玻碳电极上,并在室温下干燥以供进一步使用。
3. 结果与讨论
3.1. PCMPC的表征

Figure 1. SEM(a) and TEM(b) of PCMPC
图1. PCMPC的扫描电镜 (a)和透射电镜(b)
用SEM和TEM对PCMPC的形貌进行了表征。如图1所示,PCMC呈现圆盘状,观察到不均匀的内部塌陷,可能为p-NP提供运输的通道,且表面的杂质不能通过碳化和后处理去除干净。
PCMPC和未活化PCMPC的XRD图谱如图2所示。在2θ = 24˚处均出现宽而弱的鼓包峰,在43˚有弱100晶面的特征峰,说明制得的多孔碳材料仍为无定形碳为主。
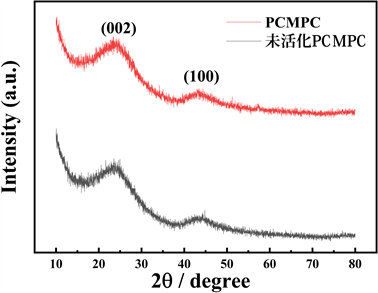
Figure 2. XRD patterns of PCMPC and unactivated PCMPC
图2. PCMPC和未活化PCMPC的XRD图谱
用XPS分析PCMPC表面的元素组成。如图3a所示,样品表面主要含有C、O。图3b和3c中,分别对C1s、O1s进行分析,碳主要有:C-OH (284.5 eV)、C-O-C (285.4 eV)、C=C (286 eV)和π-π* (287.1 eV)等形式 [10]。光谱在531.2 eV、532 eV、533.4 eV和533.8 eV处的峰分别为O=C-OH、C-OH、C-O-C、H2O的形式 [11]。
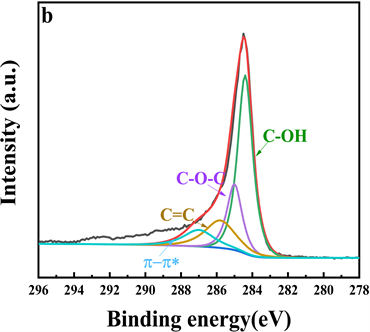
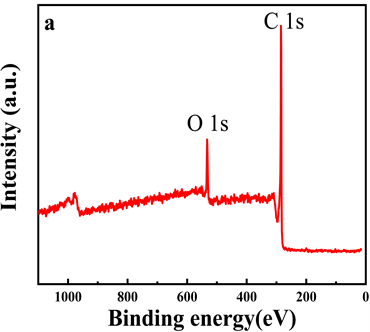
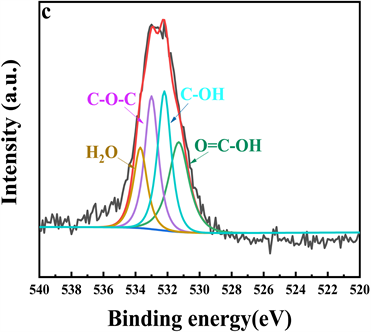
Figure 3. (a) XPS spectra of PCMPC. (b) XPS C1s spectrum of the PCMPC. (c) XPS O1s spectrum of the PCMPC
图3. PCMPC的XPS图(a),C1s的分峰图(b),O1s的分峰图(c)
3.2. 不同电极的电化学行为研究
图4为PCMPC/GCE上p-NP在0.2 μM PBS中氧化还原的CV图。
由图4可见,该曲线由−0.7 V处的一个还原峰和0.1 V左右的一对可逆峰组成。可能是因为硝基苯的自由基阴离子相对稳定。自由基的进一步还原、质子化和羟基的损失得到芳基亚硝基化合物。由于亚硝基的不稳定性,O和N之间的双键容易质子化形成苯基羟胺中间体,随后还原生成对芳基羟胺 [12]。PCMPC/GCE在空白PBS溶液中没有任何峰出现(曲线b),同比在含有200 μM p-NP的PBS中有上述三个峰出现(曲线c),说明PCMPC/GCE可以对p-NP有电化学响应,与同等条件下的GCE峰电流(曲线a)相比,电流明显增强,这可能与表面存在的含氧基团有关。
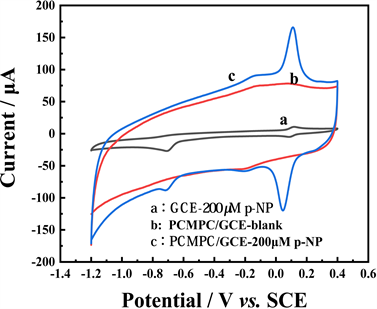
Figure 4. Cyclic voltammetry of the GCE(a) and PCMPC/GCE(c) in 0.2 M PBS containing 200 μM p-NP. Cyclic voltammetry of PCMPC/GCE(b) in 0.2 M PBS
图4. 玻碳电极GCE(a)和修饰电极PCMPC/GCE(c)在含有200 μM p-NP的0.2 M PBS中的CV曲线,修饰电极PCMPC/GCE(b)在空白PBS中的CV曲线,扫描速率:100 mV s−1
3.3. pH的影响
为了研究pH对p-NP氧化还原的影响,采用PCMPC/GCE工作电极在不同pH的PBS溶液中进行循环伏安法测试。电流响应在pH值4~7之间逐渐增加,在7~9之间下降(图5a)。
如图5a所示,随着pH值的增加,氧化还原峰电位向负值移动。在这个范围内,pH与峰电位之间存在关系如图5b。方程为:Epa = −0.08457pH + 0.6431,R2 = 0.9904,Epc = −0.06714pH + 0.4481,R2 = 0.9907。
如图5c所示,pH值为7时,峰电流达到最大值。但当pH低于7时,硝基的还原可能会受到H+的干扰。
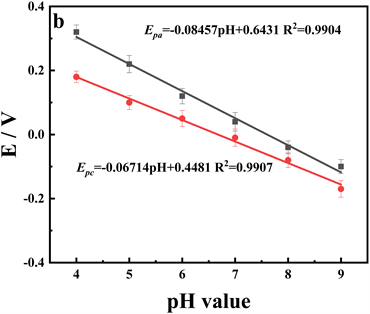
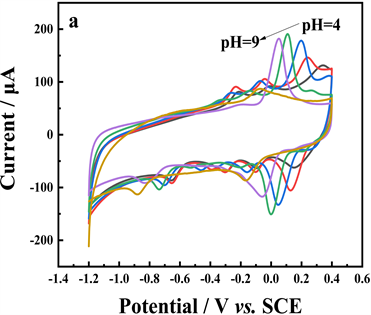
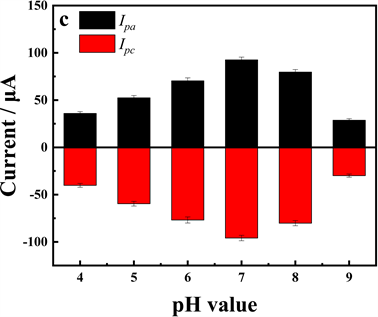
Figure 5. (a) CVs at PCMPC/GCE in PBS with different pH containing 200 μM p-NP. (b) Effect of pH value on the peak potentials. (c) Effect of pH value on the peak currents
图5. 在不同pH的 PBS溶液中,200 μM p-NP在PCMPC/GCE上的CV曲线(a);pH值与氧化还原峰电位的关系(b);pH值与氧化还原电流的关系(c)。扫描速率:100 mV s−1
3.4. 扫描速率的影响
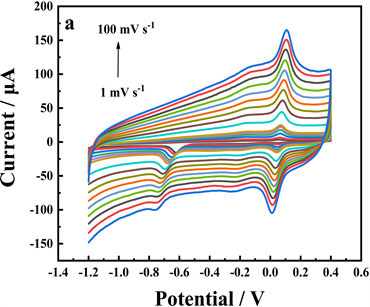
Figure 6. (a) CVs of 100 μM p-NP in PBS (pH 7.0) on the PCMPC/GCE with different scan rates ranging from 1 mVs−1 to 100 mVs−1. (b) The dependence of peak current of p-NP on scan rate with different scan rates ranging from 1 mVs−1 to 100 mVs−1
图6. 不同扫速下100 μM p-NP在PCMPC/GCE上的CV曲线(a);扫速与氧化还原峰电流之间的关系(b)
为了进一步研究PCMPC/GCE的电化学性能,用CV法测试了电极不同扫速对p-NP峰电流的影响(图6a)。图6b为−0.2~0.2 V之间的氧化还原峰电流强度与扫速之间的线性关系。Ipa = 0.4953v + 15.31,R2 = 0.9997,Ipc = −0.5136v − 19.43,R2 = 0.9995。可得,p-NP在PCMPC/GCE上,在−0.2 ~ 0.2 V之间的反应为表面吸附控制。
3.5. p-NP的定量检测
在优化的实验条件下,利用CV得到PCMPC/GCE对p-NP的分析曲线。如图7a所示,p-NP在不同浓度下CV曲线。氧化峰电流随p-NP浓度增大而增大。在1~200 μM之间存在良好的线性关系:I = 0.5324c + 11.03,R2 = 0.9968 (图7a)。根据LoD = 3 S/m,p-NP的检测限为0.23 μM,表明PCMPC/GCE电化学传感器可以灵敏稳定检测p-NP,效果令人满意。

Figure 7. (a) CVs of PCMPC/GCE in 0.2 M PBS containing p-NP with the concentration ranging from 1 to 200 μM. (b) The dependence of peak currents on the concentrations of p-NP
图7. 不同浓度p-NP在PCMPC/GCE上的CV曲线(a);还原峰电流与浓度的关系(b)
3.6. 选择性和稳定性
选择性的研究是通过添加10倍浓度有机化合物和100倍无机离子后的氧化峰电流对比发现,在含 p-NP的PBS中加入咖啡酸、多巴胺、对苯二酚、对乙酰氨基酚、香草醛及各种无机离子等。在酚类物质存在情况下,p-NP的响应电流几乎未收到影响(图8a,无机离子的干扰图中未展示),表明PCMPC/GCE具有较好的选择性。在含有p-NP的PBS中,用同一修饰电极进行了30次连续的CV测量。PCMPC/GCE的重现性和稳定性令人满意(图8b)。
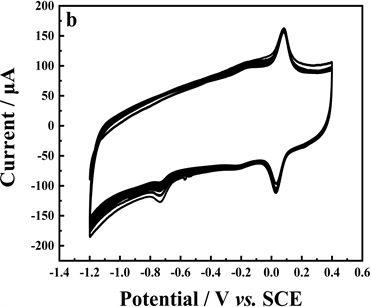
Figure 8. (a) Effect of different interferents. (b) The cyclic voltammetry curves for 30 cycles of PCMPC/GCE
图8. p-NP中加入不同干扰物的电流状图(a);同一电极扫描30次的CV曲线(b)
4. 结论
以焦糖爆米花为原料,采用化学活化一步法制备多孔生物质碳PCMPC。以PCMPC修饰玻碳电极,得到对硝基酚传感器。采用循环伏安法研究了对硝基酚在制备的传感器上的电化学响应。结果表明,在1~200 μM之间对硝基酚的氧化峰电流与其浓度呈很好的线性相关,检测限为0.23 μM。继续对材料制备工艺进行优化,本文提出的电化学传感器有望在实际中进行应用。
基金项目
南通市社会民生科技项目资助(编号:MS12021052);南通大学大学生创新训练项目资助(202110304018Z)及南通大学大型仪器开放基金资助。